Ressonância magnética nuclear
As técnicas de Ressonância Magnética Nuclear (RMN) são um instrumento indispensável para a química, bem como para outros ramos da ciência. Com a espectroscopia de RMN é possível identificar moléculas (Figura um espectro), determinar sua estrutura ou estudar processos dinâmicos. Por exemplo, tem sido fundamental na determinação da estrutura de proteínas em solução e, por outro lado, as técnicas de imagem por RMN são uma ferramenta indispensável no diagnóstico médico, conforme ilustrado na (Figura b).
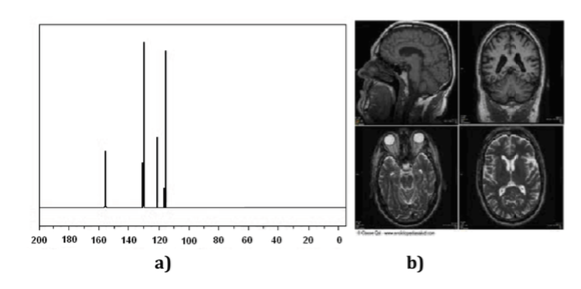
A RMN é baseada em três elementos:
a) O caráter magnético dos núcleos das moléculas em estudo:
Muitos núcleos atômicos, devido ao spin nuclear, possuem características magnéticas. De certa forma pode-se considerar que os núcleos se comportam como pequenos imãs.
b) A aplicação de um campo magnético intenso:
Quando as moléculas em estudo são imersas em um campo magnético, os níveis nucleares se desdobram em vários níveis de energia. Cada um dos níveis de energia que aparecem correspondem a diferentes orientações dos spins dos núcleos (pequenos ímãs) em relação ao campo magnético.
c) Iluminação da amostra com radiação eletromagnética:
Como em outras técnicas espectroscópicas, a iluminação da amostra com a frequência de radiação adequada fará com que os núcleos passem de um nível para outro. A frequência da radiação necessária para produzir esse salto de nível dependerá do tipo de núcleo, de seu ambiente químico, do tipo de núcleos presentes em sua vizinhança e do campo externo aplicado. Ao longo deste tópico, serão estudados os fundamentos físicos desta técnica, e serão explicadas as técnicas experimentais que permitem a obtenção dos espectros, analisando também as causas que tornam os espectros das várias moléculas diferentes.
Noções básicas de RMN:
Spin nuclear e momento angular do spin nuclear
Os núcleos atômicos são formados por prótons e nêutrons. Ambos os núcleons têm momento angular orbital e momento angular de spin (prótons e nêutrons têm spin 1/2). A resultante da soma vetorial de todos os momentos (orbital e spin) de todos os prótons e nêutrons do núcleo dá como resultado o momento angular do spin nuclear e é simbolizada por I e suas unidades são J s. De acordo com a mecânica quântica, a magnitude do momento angular do spin nuclear, |I|, é quantizada, com um valor I(I+1)h onde I é o número quântico do spin nuclear ou spin nuclear e ħ é h/2p(que no sistema internacional vale 1,05457·10-34J·s). O valor de I é uma característica fixa de cada tipo de núcleo atômico e pode assumir um valor inteiro ou semi-inteiro (0,1, 2, 3,… ½ , 3/2 , 5/2…).
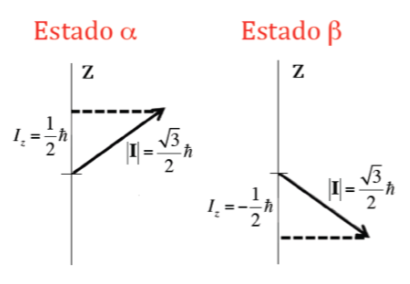
Além do módulo, também é importante conhecer a componente do momento angular em torno do eixo z, Iz. Este também pode assumir valores quantizados dados pela expressão m I h onde m I é o número quântico associado à componente z do momento angular do spin nuclear e que pode assumir os seguintes valores: –I, (‐I+1) , ... , (I-1), I. Assim, para um dado núcleo, com valor I, existem (2I+1) orientações do momento angular do spin nuclear. Por exemplo, considere o núcleo atômico do isótopo mais comum do átomo de hidrogênio, 1H, que é formado por um próton e sabe-se que seu spin nuclear, I , é 1/2, e portanto m I pode assumir dois valores +1/2 e -1/2 (em RMN, o isótopo 1H é muitas vezes referido como próton). O próton, portanto, tem dois estados nucleares possíveis, um chamado a com m I =+1/2 e o outro b com m I =‐1/2. A Figura abaixo mostra as duas possíveis orientações do momento angular de spin nuclear correspondentes aos estados a e b, que são energeticamente equivalentes.
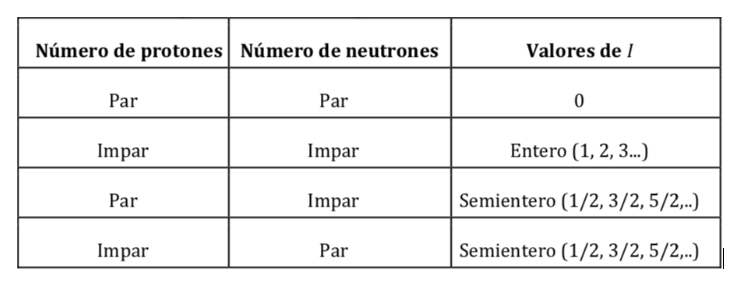
Valores de I de acordo com o número de prótons e nêutrons no núcleo:
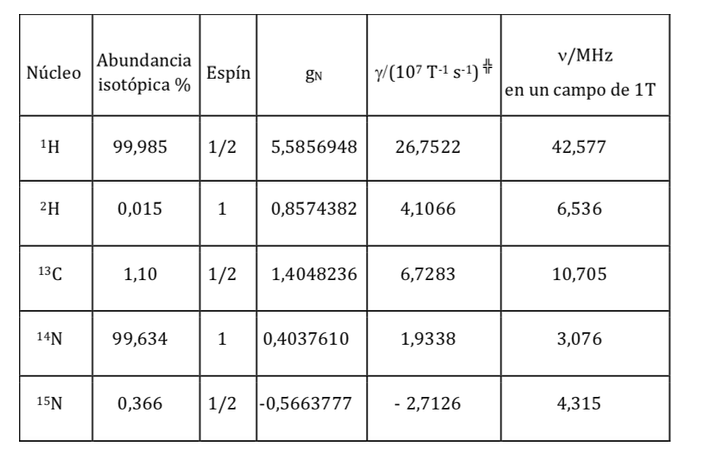
Propriedades magnéticas de vários núcleos:
Momento de dipolo magnético nuclear (magneton nuclear, razão giromagnética):
Assim como o elétron tem um momento de dipolo magnético, alguns, mas não todos, os núcleos atômicos têm um momento de dipolo magnético. Conforme indicado, os núcleos se comportam como pequenos ímãs, sendo a origem desse caráter magnético o momento angular do spin nuclear. O momento angular de spin nuclear, I, dá origem a um momento de dipolo magnético nuclear mI que é dado por:
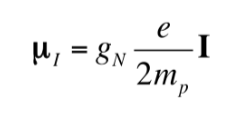
onde gN é o fator g nuclear. Observe que essa expressão usa a massa e a carga do próton (mp ye) por definição, em vez da massa e da carga do núcleo em questão. As diferenças de um núcleo para outro estão incluídas no fator gN nuclear. O valor de gN não pode ser obtido teoricamente, por isso é determinado experimentalmente. As unidades de mI são JT-1
A relação entre mI e I também pode ser expressa da seguinte forma:
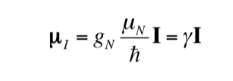
com
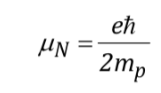
sendo uma constante com valor de 5.050 10-27J T-1 chamada de magneton nuclear e g é a relação giromagnética (T-1s-1).Nas tabelas anteriores já foram mostrados valores dessas magnitudes para alguns isótopos. Embora na maioria dos casos mI e I tenham o mesmo sentido, às vezes é oposto, como pode ser deduzido dos valores negativos do fator gN e g para o isótopo 15N, por exemplo.
No caso do próton onde foram observadas duas orientações possíveis do momento angular, haverá duas orientações possíveis do momento magnético do dipolo, conforme ilustrado na figura a seguir, sendo ambas as orientações energeticamente equivalentes, pois a escolha de uma direção z é arbitrário.
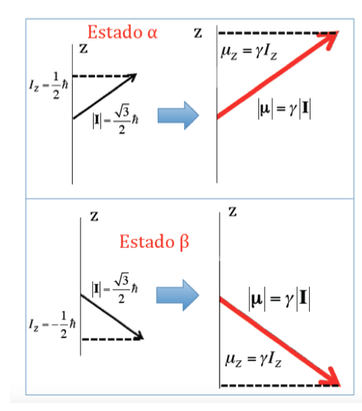
Energia de interação do campo magnético com o momento magnético nuclear:
Se uma molécula for introduzida em um campo magnético, com densidade de fluxo ou campo magnético B, o momento magnético dipolar de cada um de seus núcleos irá interagir com ela, conforme ilustrado na figura a seguir, sendo a energia da interação expressa por:
![]()
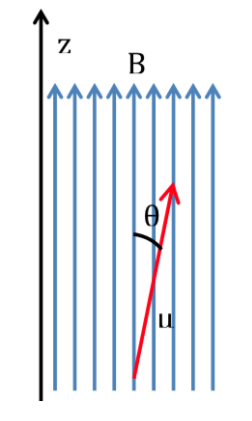
De acordo com a física clássica, todas as orientações de um dipolo magnético dentro de um campo magnético são permitidas e, portanto, q pode assumir qualquer valor entre 0 e 180o. Dependendo da orientação do dipolo, a energia será maior ou menor:
A interação mais favorável ocorre quando ambas as magnitudes têm a mesma direção: q=0 e, portanto, cos q=1 e :
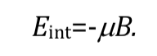
No entanto, de acordo com a mecânica quântica, nem todas as orientações do dipolo magnético nuclear são permitidas, as orientações são quantizadas e apenas certos valores de q são possíveis. Existem tantas orientações permitidas quantos valores Iz ou mI (‐I, ‐I+1,..., I‐1, I), ou seja, 2I+1 orientações. Obviamente, o número de orientações do momento de dipolo varia com o tipo de núcleo atômico. Para definir as orientações, toma-se como referência para o eixo Z a direção e direção do campo B.
Assim a energia de interação do campo magnético externo B e o dipolo nuclear será dada por: j
frequência de Langmor
Se um campo magnético externo de intensidade B atua sobre o núcleo, o dipolo magnético nuclear experimenta um par de forças conforme mostrado na seguinte fórmula dada por:
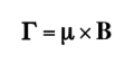
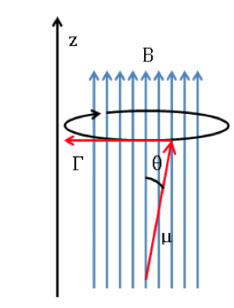
que tende a alinhar o dipolo com o campo magnético. Como o dipolo magnético não pode ser alinhado com o campo magnético, o sistema é incapaz de dissipar essa energia e precessão, chamada de precessão de Larmor, em
sobre a direção do campo aplicado. A frequência dessa precessão é chamada de frequência de Larmor, com um valor:
esquema langmor:
Espectroscopia de RMN
A chave de qualquer técnica espectroscópica baseia-se na possibilidade de que a molécula em estudo possa estar em mais de um nível de energia, de forma que, ao fazer com que a radiação eletromagnética (rem) de frequência apropriada a afete, ela possa passar para o nosso sistema. .(molécula) de um nível de energia para outro. Como visto na seção anterior, o núcleo de um próton, imerso em um campo magnético, pode ocupar dois níveis diferentes associados ao spin nuclear, fazendo com que um feixe rem de frequência apropriada caia sobre um núcleo de 1H que está ocupando o nível inferior, pode ser passado para o nível superior. Este tipo de transições é o que dá origem à Espectroscopia de Ressonância Magnética Nuclear (NMR). A partir de agora vamos nos concentrar no caso do próton 1H, pois é a espectroscopia mais utilizada, embora tudo indicado seja aplicável a outros núcleos. Na verdade, mais e mais variedade de núcleos são usados.
Frequência de ressonância:
A frequência que causa a transição é obtida aplicando a condição de ressonância:
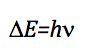
Como a diferença de energia entre dois níveis consecutivos é:
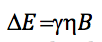
igualando ambas as expressões e isolando n:
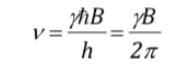
que, como pode ser visto, coincide com a frequência de precessão de Larmor.
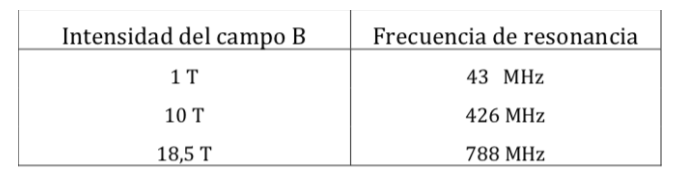
Frequências de ressonância de NMR de prótons para várias intensidades de campo:
Regras de seleção:
As regras de seleção estudadas em outras espectroscopias correspondem à interação do dipolo elétrico com o campo elétrico da radiação. Por outro lado, em RMN a interação ocorre entre o dipolo magnético do núcleo e o campo magnético variável da radiação. Para determinar as regras de seleção, deve-se lembrar da expressão geral que determina a probabilidade de passagem entre dois estados:
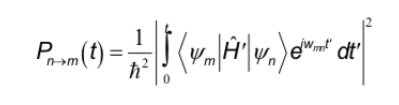
O hamiltoniano, neste caso, é o produto do operador do campo magnético oscilante da radiação pelo operador do momento de dipolo do núcleo.
![]()
Pode-se mostrar que para haver uma transição entre dois níveis a regra de seleção correspondente é:
mI = ± 1
Força do sinal (níveis de população):
A intensidade do sinal está diretamente relacionada com a população de níveis envolvidos na transição. De acordo com a lei de distribuição de Boltzman, para um sistema de dois níveis, como o próton, a razão entre a população do nível superior, Nb, e a população do nível inferior, Na, é dada por:
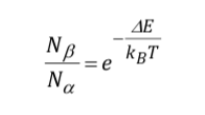
Descrição do equipamento NMR:
Qual procedimento experimental é usado para obter o espectro? Geralmente na espectroscopia varia-se a frequência da radiação incidente, até que a absorção seja observada. Porém, na espectroscopia de RMN também existe a opção de manter fixa a frequência da radiação e variar o espaçamento entre os níveis, variando a magnitude do campo B aplicado até que seja observada absorção. Na figura a seguir é apresentado um esquema de um equipamento de RMN. A amostra é colocada em um tubo, que às vezes é girado rapidamente para obter homogeneização no sinal, embora o uso de rotação esteja atualmente em discussão, pois pode introduzir erros. O tubo, por sua vez, está localizado entre dois polos magnéticos que são os que geram o campo magnético. Existe um transmissor e um receptor de radiofrequência. O sinal do emissor pode ser controlado para fazer uma varredura de frequência. Com bobinas de varredura, uma varredura do campo pode ser controlada. Os atuais equipamentos de RMN quase não utilizam mais:
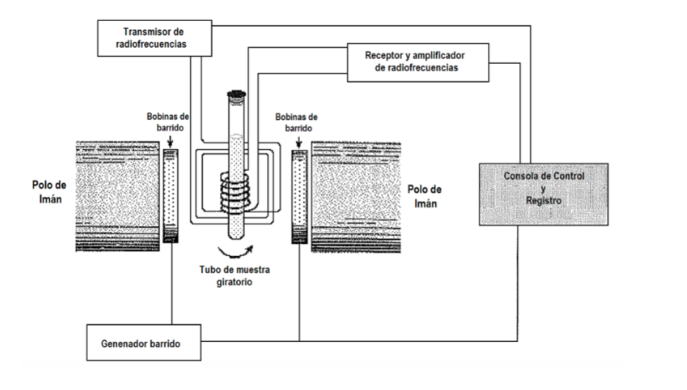
procedimentos anteriores, mas são baseados no uso de técnicas de transformada de Fourier. B é mantido estacionário e a amostra é iluminada com um pulso de radiofrequência de alta potência e tempo limitado com frequência nrad, um valor fixo na faixa de frequência de NMR do tipo de núcleo que está sendo estudado. O pulso dura vários microssegundos, então pode ser mostrado matematicamente por uma técnica chamada análise de Fourier que o pulso de radiofrequência é equivalente a uma faixa de frequências ∆n em torno de nrad e excita todas as ressonâncias NMR possíveis. O sinal observado no detector conterá todas as frequências ressonantes e é analisado por um computador usando técnicas de transformada de Fourier. Este procedimento permite altíssima resolução e trabalhar com núcleos que com os procedimentos anteriores tinham sinais muito fracos.
Blindagem nuclear:
Na Ressonância Magnética, são utilizados núcleos com momento angular de spin diferente de zero, como 1H e 13C. No entanto, as frequências de ressonância não são as mesmas para todos os núcleos de hidrogênio ou carbono, elas dependem do ambiente químico que envolve cada núcleo. Isso se deve ao fato de que os elétrons que envolvem cada núcleo geram um campo magnético oposto ao aplicado, diz-se que os núcleos são blindados, onde σ é a constante de blindagem.
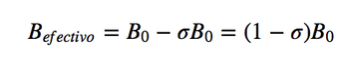
Bef é o campo magnético resultante atuando no próton; B0 é o campo magnético aplicado; σ é a constante de blindagem, independente do campo aplicado. Nessa nova situação, com os núcleos blindados pela densidade eletrônica que os envolve, a frequência de ressonância torna-se
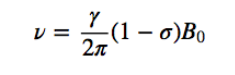
Núcleos com diferentes ambientes químicos possuem diferentes constantes de triagem, gerando diferentes sinais no espectro de RMN.
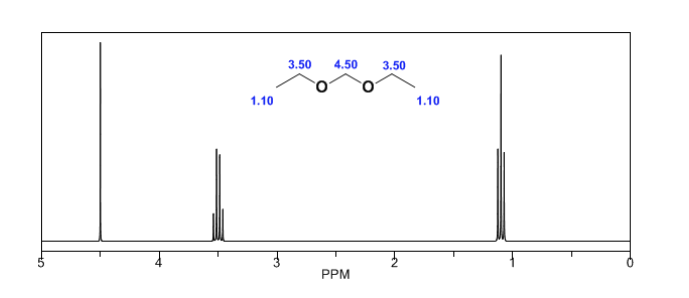
espectro de etanol:
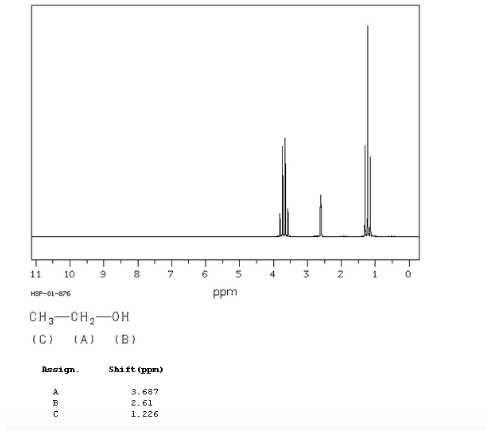
No espectro de RMN do etanol, três sinais diferentes são observados, devido à existência de 3 tipos de hidrogênios com ambientes químicos diferentes. Os hidrogênios A são mais desprotegidos do que C devido à presença de oxigênio (átomo eletronegativo que remove a densidade de elétrons). O ambiente químico do hidrogênio B, diretamente ligado ao oxigênio, também é diferente, ressoando em uma frequência diferente das anteriores.
mudança química
Os sinais no espectro de NMR são medidos em uma escala independente do campo magnético aplicado, chamado de deslocamento químico e representado pela letra δ. Independentemente do campo magnético em que o espectrofotômetro trabalha, os sinais de um composto químico são sempre obtidos nos mesmos valores de δ:

Tabela de deslocamento:
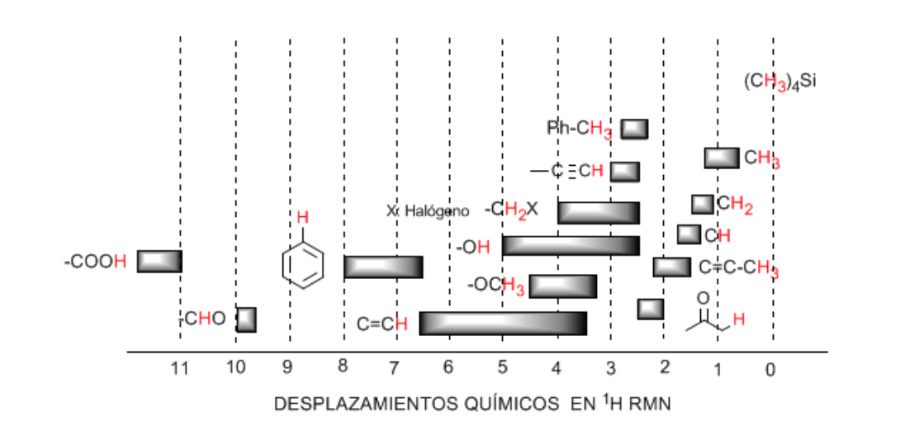
Os hidrogênios localizados nas cadeias alifáticas apresentam valores de δ próximos a 1. Isso aumenta um pouco quando se passa de carbonos primários para carbonos secundários ou terciários.
Os hidrogênios alílicos estão localizados entre 1,5 e 2,1.
Hidrogênios alfa em relação a carbonilas e derivados de ácidos estão entre 2 e 2,5.
Os hidrogênios benzílicos entre 2,3 e 2,7.
O hidrogênio dos alcinos terminais entre 2,5 e 3.
Hidrogênios ligados a carbonos com halogênios entre 2,5 e 4 dependendo da eletronegatividade do halogênio
Os hidrogênios do grupo hidroxila entre 2,5 e 5. Gama muito ampla devido à formação de pontes de hidrogênio.
Hidrogênios de carbono ligados a oxigênio tipo éter entre 3,3 e 4,5.
Hidrogênios olefínicos entre 3,5 e 6,5.
Hidrogênios ligados a sistemas aromáticos entre 6,5 e 8.
Aldeído hidrogênio 9,5-10
Hidrogênio do grupo ácido carboxílico acima de 11.
Os grupos eletronegativos desblindam os núcleos:
Os substituintes eletronegativos removem a densidade de elétrons, desprotegindo os hidrogênios e deslocando o sinal para valores δ altos.
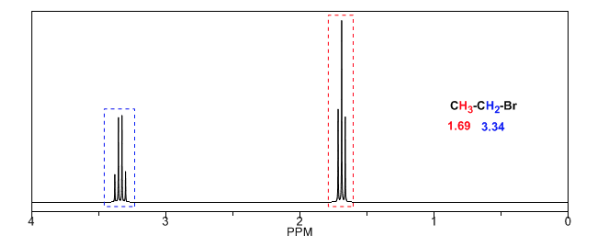
Na tabela a seguir você pode ver a influência de diferentes átomos no sinal dos hidrogênios metílicos.
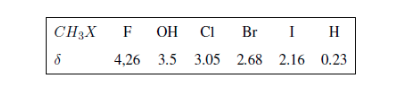
Nos espectros a seguir, podem ser observados os efeitos acima mencionados nos deslocamentos químicos.
Anisotropia magnética:
Os prótons próximos a ligações duplas e anéis aromáticos são especialmente desprotegidos devido ao campo magnético induzido pelas correntes eletrônicas desses sistemas. O campo induzido se soma ao aplicado, produzindo um deslocamento maior que o esperado.
Na imagem a seguir podemos ver a circulação eletrônica (curvas em negrito) e o campo magnético induzido (linhas tracejadas) para um alceno e uma carbonila. Observe como na região do próton o campo magnético induzido tem a mesma direção e direção do aplicado.
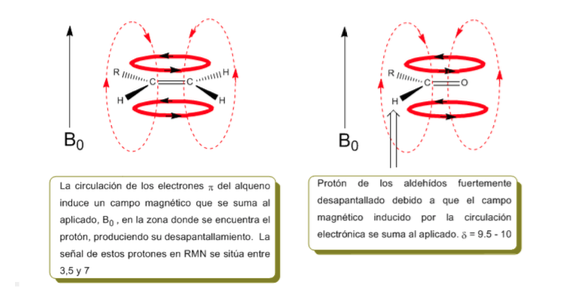
Uma situação semelhante é observada no caso do benzeno. Já nos alcinos, a circulação eletrônica induz um campo magnético oposto ao aplicado na área do próton. Os hidrogênios acetilênicos são protegidos com sinais no espectro de NMR em deslocamentos baixos.
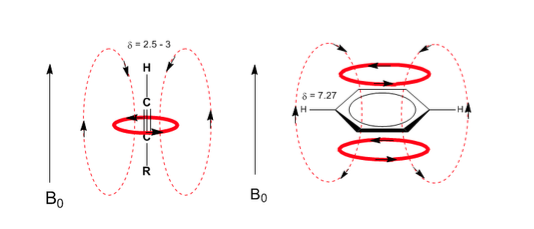
Observe como os campos induzidos aumentam consideravelmente os deslocamentos do próton olefínico, sendo as posições alílicas também afetadas.
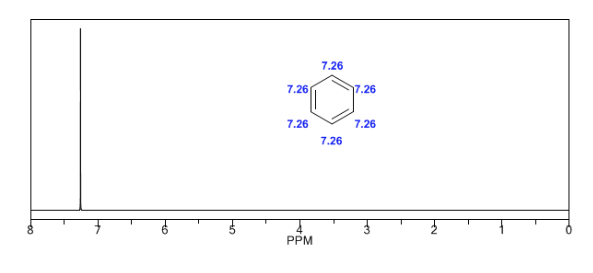
Os hidrogênios aromáticos são fortemente desprotegidos devido ao campo induzido pelas correntes do anel.
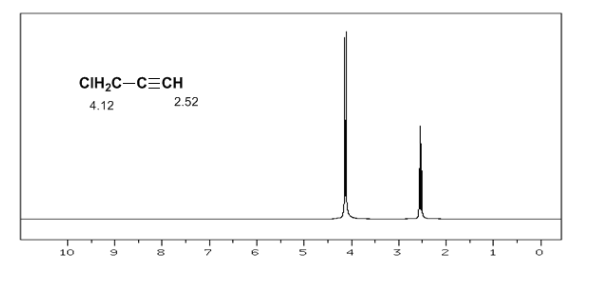
O hidrogênio acetilênico tem baixo deslocamento, pois as correntes produzem um campo magnético contrário ao aplicado.
Os deslocamentos de hidrogênio ácidos mais comuns em moléculas orgânicas são:
- ·Ácidos carboxílicos (RCOOH) δ= 10 - 12 ppm
- ·Aminas (R−NH2) δ= 0,5 - 5 ppm
- Amidas (RCONH2) δ= 5-8 ppm
- · Álcoois (ROH) δ= 0,5 - 5 ppm
- Fenóis (Ph-OH) δ= 4 - 7 ppm
Acoplamento spin-spin:
A informação estrutural da RMN deriva de dois fatores: os diferentes deslocamentos observados dependendo do ambiente químico que envolve o próton e o acoplamento entre os spins dos prótons próximos, que produz a divisão dos sinais.
Embora alguns sinais do espectro sejam picos únicos, é comum encontrar sinais compostos por vários picos muito próximos, que são nomeados com a seguinte notação: singleto (s), dupleto (d), tripleto (t), quadrupleto (c) , quíntuplo (q), sêxtuplo (sx) e sétuplo (sp), sinais complexos são designados como multipletos. O valor de δ desses sinais é atribuído ao seu centro, a menos que o multipleto seja irregular, caso em que o intervalo é indicado.
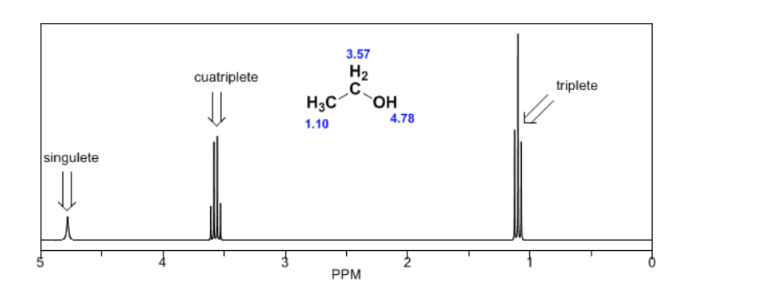
No espectro do etanol, pode-se ver que o hidrogênio da hidroxila produz um singleto, o par de hidrogênios no carbono um dá origem a um quádruplo e os três hidrogênios no carbono dois produzem um tripleto.
Explicação do acoplamento spin-spin.
Para entender a divisão de sinais devido ao acoplamento spin-spin vamos estudar o espectro do 1,1-dicloro-2,2-difeniletano ( Cl 2 CH a CH b Ph 2 ).
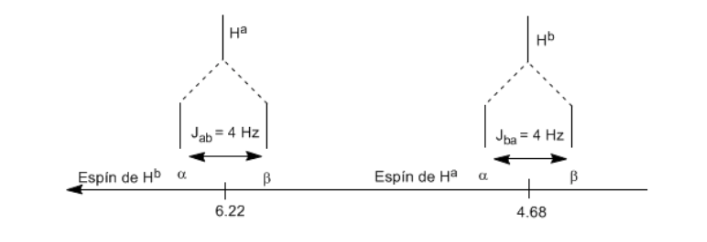
O próton Ha submetido a um campo magnético B0 produz um sinal em δa=6,22ppm. Porém, o próton da Hb gera um pequeno campo magnético que afeta o próton Ha. Aproximadamente metade das moléculas tem o próton da Hb alinhado com o campo aplicado (spin alfa) e a outra metade tem ele orientado contra o campo (spin beta). . Quando Hb tem spin α, Ha é submetido a um campo ligeiramente maior e ressoa em uma frequência mais alta (ligeiramente maior δ). Quando Hb tem spin β, Ha é submetido a um campo ligeiramente menor e ressoa em uma frequência mais baixa (ligeiramente menor δ), que divide o pico inicial em dois sinais separados por uma distância de 4 Hz, chamada de constante de acoplamento (J). Esse mesmo raciocínio pode ser feito para o próton da Hb.
Por fim, discutiremos o acoplamento de um próton com três prótons vizinhos equivalentes. Neste caso, observa-se um sinal formado por quatro picos (quadtripleto). Os picos centrais são três vezes mais intensos que os picos extremos.
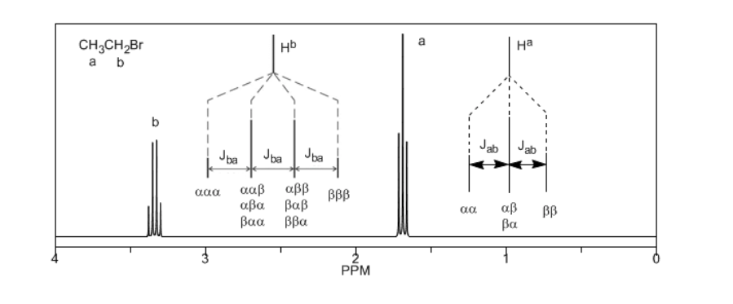
Regra N+1
Da discussão acima, pode-se deduzir que um próton produz um sinal com um número de picos uma unidade maior que o número de hidrogênios vizinhos. Na imagem a seguir podemos ver os picos produzidos por um hidrogênio Hb quando acoplado a vários hidrogênios variáveis
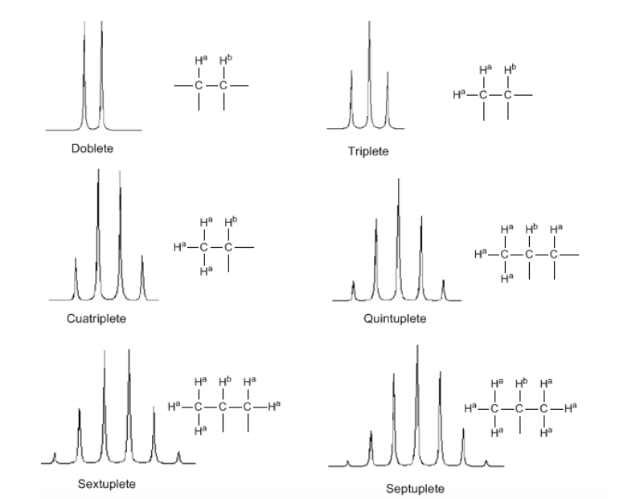
A intensidade dos picos de um sinal é dada pelo triângulo de Pascal (Tartaglia):
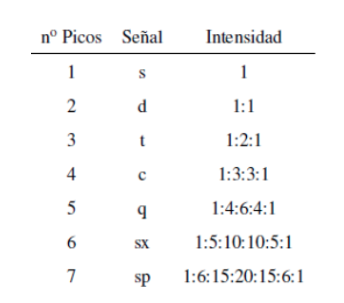
Duas considerações devem ser levadas em conta ao aplicar a regra N+1:
- Em moléculas do tipo A−CHa2−CHb2−CHa2−A, os prótons da Hb aparecem como um quíntuplo.
- Nas moléculas do tipo A−CH2−CH2−A, os quatro prótons são equivalentes e dão um singleto.
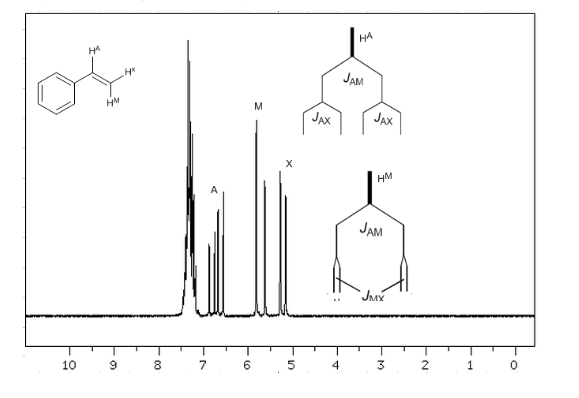
Acoplamento de três núcleos não equivalentes:
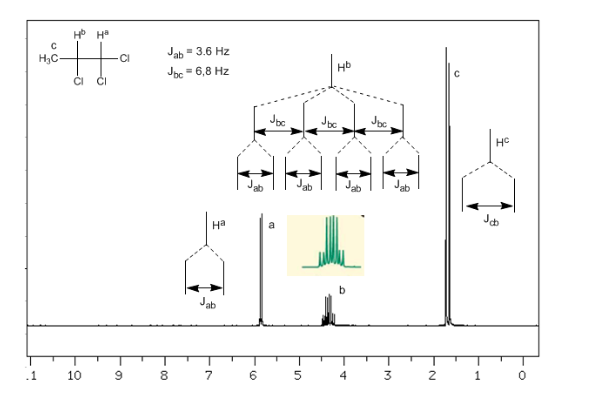
Levando em conta que a ordem das constantes de acoplamento nos alcenos é Jtrans>Jcis>Jgeminal, as árvores de acoplamento para os hidrogênios Ha e HM são as indicadas no espectro. Você seria capaz de desenhar a árvore para Hx?
13C ressonância magnética nuclear
A ressonância magnética nuclear de 13C é complementar à de 1H. A última técnica é usada para deduzir a estrutura do esqueleto de carbono observando os ambientes magnéticos dos átomos de hidrogênio, enquanto a espectroscopia 13C NMR determina o ambiente magnético dos átomos de carbono.
Os deslocamentos químicos do carbono são 15 a 20 vezes maiores do que os do hidrogênio, porque o carbono está diretamente ligado aos átomos que estão protegendo ou desprotegindo. Por exemplo, o próton de um aldeído absorve a 9,4 ppm no espectro 1H, enquanto o carbono carbonílico absorve a 180 ppm no espectro 13C.
Além disso, os sinais no espectro 13C são linhas verticais, ou seja, não há divisões spin-spin. Isso ocorre porque apenas 1% dos átomos de carbono entram em ressonância e, portanto, há uma probabilidade muito pequena de que um núcleo 13C esteja adjacente a outro núcleo 13C.
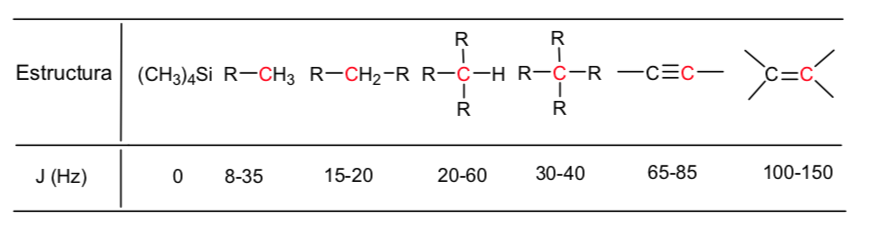
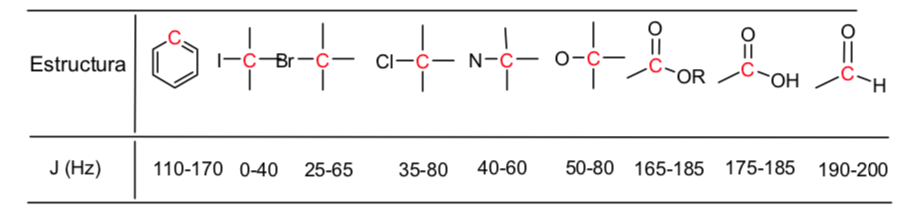
Uma tabela de valores aproximados de deslocamentos químicos em um espectro de ressonância magnética nuclear 13C é dada abaixo:
Referências recomendadas para expandir a pesquisa:
1. Aga Fano SA Espectroscopia de Emissão. (Acessado em 10 de setembro de 2007). http://hiq.aga.com.co/International/Web/LG/CO/likelgspgco.nsf/DocByAlias/anal_icp .
2. Alonso, P. et al. química Cou..Ed. McGraw-Hill. 1990.
3. Álvarez Jiménez, MD e Gómez del Río, MI Guia Didático Química Analítica II. UNED. 1999.
4. Chegadas Jimeno Siro; Burriel Barceló Fernando; Hernández Mendez Jesus; Lucena Conde Felipe. Química Analítica Qualitativa. ISBN: 8497321405. ISB. 2006.
5. Ayres, Gilbert H. Análise Química Quantitativa. Edições do Castelo, 4ª ed . ISBN: 8421902806. 1981. See More
6. Bermejo Barrera. M del Pilar. Química analítica geral, quantitativa e instrumental. Editorial Paraninfo. 7ª Edição. ISBN: 8428318093. 1990.
7. Blanco, M., Cerdá, V. e Sanz Medel, A., Analytical Atomic Spectroscopy, University Publications Autônomo de Barcelona. 1990.
8. Brode. RW, espectroscopia química, Nova York 1952.
9. Burriel, MF, Lucena, CF. Química Analítica Quantitativa. Edição Revolucionária. Havana.1978.
10. Burriel, F. Química Analítica Qualitativa. Editorial Paraninfo. ISBN: 8497321405. pp 1072. , 2003.