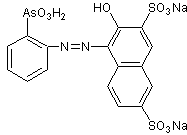
SINTESI TORINA
Le applicazioni analitiche di thorin, i parametri di lavoro, i suoi limiti e le prospettive, sono affrontati e spiegati in modo sufficientemente dettagliato in pubblicazioni di analisi chimiche specializzate come Analytical Chemistry . Un breve riassunto di essi mostra le seguenti applicazioni:
In ambiente acido : serve per la determinazione quantitativa degli elementi torio (Th), zirconio (Zr), fluoro (F), afnio (Hf) e uranio (U).
In un mezzo basico : la forma di acido disolfonico della torina, meglio nota come Thoron, viene utilizzata nella determinazione quantitativa del litio (Li).
In mezzo neutro : il thorin viene utilizzato come indicatore per la determinazione degli ioni solfato (SO 4 2- ) in soluzioni acquose.
Thorin è anche usato per determinare SO 2 nell'aria.
Problema di ricerca.
Data la richiesta di questo reagente per diverse determinazioni analitiche ed in particolare per l'analisi colorimetrica del litio in salamoia del Gran Salar de Uyuni e la scarsa offerta di esso nel mercato nazionale, nasce la necessità di sintetizzare la torina, da materiali semplici ed economici . nel nostro ambiente.
A tal fine, i percorsi di sintesi progettati vengono affrontati dal paradigma RETROSYNTHESIS , essendo applicabili i metodi di The Synthesis Sheets, Disconnection o Synthon Method e Tree Method. di Sintesi.
In relazione alla sintesi di Thorin , esiste in letteratura una descrizione breve e riassuntiva della sintesi di Thoron , secondo la direzione proposta di Kuznetsov , cioè si indica che per la preparazione del toron è necessario che l'acido o-amminofenilarsonico sia diazocopulato con il sale disodico dell'acido 2-naptol-3,6-disolfonico (sale R) in un mezzo acido.
Progetto di sintesi per Thorina .
Il design viene affrontato con il metodo delle disconnessioni o Sintón, che contempla due fasi. La prima è relativa all'analisi retrosintetica e la seconda alla sintesi nella direzione di quanto avviene in laboratorio, cioè dai materiali di partenza fino ad arrivare alla Molecola Target (MOb).
A) Elementi strutturale e reattività da considerare, per l'analisi retrosintetica
Thorin è tipicamente un composto azoico, quindi un colorante. La preparazione di questi composti comprende generalmente due reazioni fondamentali, che sono: la diazoazione e il diazoaccoppiamento (o semplicemente accoppiamento).
D'altra parte, tutte le molecole precursori dell'accoppiamento utilizzate per la formazione di coloranti azoici hanno un carattere comune, cioè: un atomo di idrogeno attivo legato ad un atomo di carbonio.
Le seguenti sono ampiamente utilizzate come molecole precursori (substrati) per l'accoppiamento: Composti che hanno ossidrili fenolici, come fenoli e naftoli, Ammine aromatiche, Molecole con gruppi chetonici alifatici enolizzabili e Molecole eterocicliche come pirrolo, indolo, ecc.
In relazione alla reazione di copulazione, devono essere presi in considerazione alcuni principi euristici, vale a dire:
· I fenoli si accoppiano più facilmente delle ammine e i membri della serie dei naftalene più facilmente del benzene.
· I sostituenti con effetto induttivo negativo (-I), come i gruppi alogeni, nitro, sulfamidici, carbossilici e carbonilici ritardano l'accoppiamento.
· Un gruppo alchilico o alcossilico in posizione orto o meta rispetto a un gruppo amminico favorisce l'accoppiamento. E se si trovano nelle posizioni 2 e 5 rispetto al gruppo amminico, sono particolarmente buoni accoppiatori.
· Nella serie del benzene, l'accoppiamento avviene normalmente in posizione para rispetto al gruppo ossidrile (-OH) o amminico (-NH 2 ). Se la posizione per è occupata, il collegamento avviene nella posizione orto.
· Nella serie del naftalene, quando il gruppo ammino ossidrile è in posizione 2 ( b ), il reagente è accoppiato in posizione 1 ( a ). Se il gruppo ossidrile o amminico si trova nella posizione alfa, il legame si verifica solitamente nella posizione 4; ma se la posizione 3 o 6 è occupata da un gruppo solfonico, l'unione avviene in posizione beta.
· Quando ci sono due possibili posizioni di accoppiamento, la posizione del legame è spesso decisa dal pH del mezzo: l'accoppiamento avviene in orto con il gruppo amminico quando è effettuato in un mezzo acido e in orto con il gruppo ossidrile quando è effettuato in un mezzo di base.
Sulla base degli elementi euristici menzionati in precedenza, ci sono vari progetti di sintesi per Thorin, che rispondono all'analisi retrosintetica . , proposto . Che in sostanza è una sintesi convergente, espressa dal accoppiamento diazo del sale disodico dell'acido 2-naftol-3,6-disolfonico, comunemente noto come "sale R", con cloruro ortodiazofenilarzonico in ambiente acido
Si può vedere nell'analisi retrosintetica che un intermedio chiave o strategico è l'orto -nitroanilina, un aspetto che porta a materiali di partenza semplici come benzene e naftalene rispettivamente.
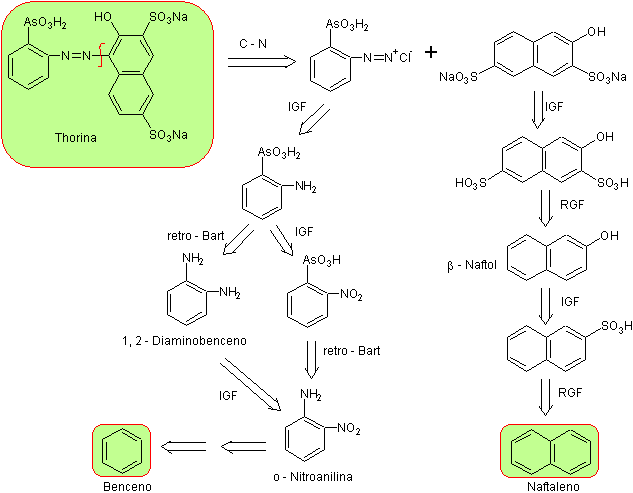
Fonte: fai da te
ortonitroanilina , Può essere sintetizzato con diverse procedure, con diversi livelli di complessità e resa. Delle undici alternative studiate sperimentalmente, solo otto sono indicate nella rosetta di retrosintesi.
Da esso, le alternative di disconnessione 3 e 4 sono state selezionate per questa pubblicazione. , che a loro volta originano due percorsi di sintesi convergenti.
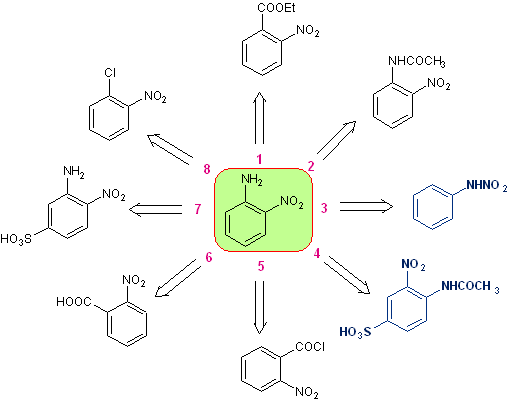
Rosetta di retrosintesi per orto-nitroanilina
B) Sintesi del "sale R".
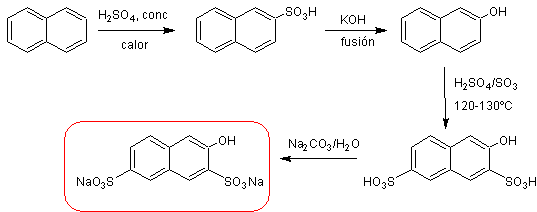
C) Sintesi di Thorin.
Percorso di sintesi I : la strategia tiene conto della formazione di orto -nitroanilina da Riarrangiamento nitroamminico della nitranilina, in ambiente acido.
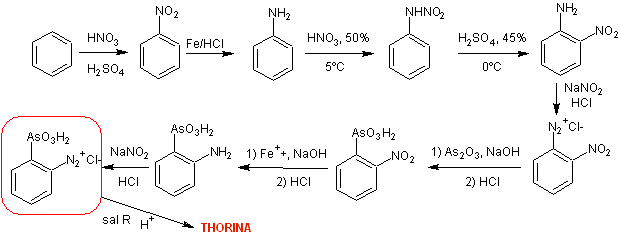
Percorso di sintesi II. La strategia prevede la formazione di orto -nitroanilina, attraverso processi di protezione e deprotezione della posizione para dell'anilina.
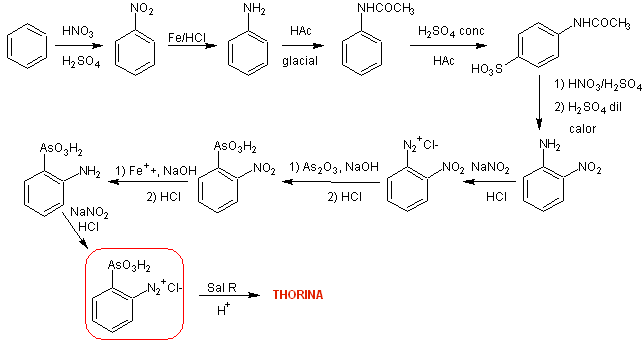
Risultati
Gli esperimenti sviluppati per ciascuna fase nei diversi Percorsi di Sintesi hanno risposto a un disegno sperimentale fattoriale 2 2 che ha permesso di indagare l'effetto principale dei fattori e l'interazione tra loro. , per ottimizzare le condizioni di lavoro.
ü Risultati sperimentali della preparazione del “sale R”.
naftalene ![]() β-naftalensolfonato di sodio
β-naftalensolfonato di sodio ![]() β-naftolo
β-naftolo ![]() "sale R"
"sale R"
r 1 = 87,89% r2 = 86,55% r3 =75,23%
La resa di solfonazione del β -naftolo è relativamente bassa, perché alla stessa temperatura di solfonazione, altri prodotti come il sale di Schaeffer (2-naftol-6-solfonato di sodio) e piccole quantità del sale sodico di 2-naftol-6,8- acido disolfonico (acido G), il cui sale sodico è più solubile del "sale R", aspetto che viene utilizzato nel processo di ricristallizzazione del "sale R".
Rendimento complessivo : sale R = (r 1 * r 2 * r 3 )*100
= (0,8789*0,8655*0,7523)*100 = (0,5723)*100 = 57,23%
ü Risultati sperimentali per Synthesis Route I.
Il processo che parte dal benzene fino ad arrivare al cloruro orto -diazofenilarzonico (Cl-o-DFA), si compone di otto stadi e raggiunge una resa di R Cl-o-DFA = 23,39%.
Invece la reazione in ambiente acido, del cloruro orto -diazofenilarzonico con il "sale R", preparato secondo gli schemi precedentemente indicati, per ottenere THORINA, presenta una resa dell'85,46% .
Sulla base di questi risultati sperimentali, la resa totale (Q TSI ) di Synthesis I, con un limite di confidenza del 95% è:
QTSI = [(57,23% + 23,39%)/2]*85,46 = 34,45%
Il costo intrinseco di produzione del torino, nel percorso Synthesis I, è di 0,81 $us/g
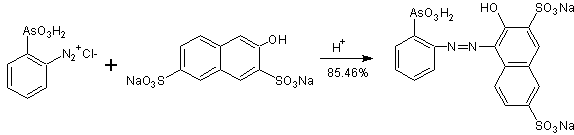
ü Risultati sperimentali per Synthesis Route II.
In questa nuova alternativa di sintesi, il benzene viene trasformato in cloruro orto -diazofenilarzonico in nove stadi, con una resa RCl-o-DFA = 28,04%.
La reazione di questo sale, cloruro orto -diazofenilarzonico, con il sale R" in ambiente acido, come sopra indicato, raggiunge una resa dell'85,46%, per cui la resa totale della Via di Sintesi II (Q TSII ), è del 36,44%.
Il costo intrinseco della produzione di thorin, secondo questo percorso di sintesi, è di 1,17 $us/g
conclusioni
I diversi percorsi di sintesi proposti e sperimentati hanno il pregio di dimostrare che la sintesi organica, cuore della chimica organica, è una disciplina eminentemente predittiva, ed è uno strumento pedagogico di grande valore.
L'analisi retrosintetica, espressa dalla metodologia della disconnessione nel piano progettuale e l'utilizzo di disegni sperimentali fattoriali utilizzati nella pratica, sono una potente combinazione per affrontare lavori di sintesi organica di notevole profondità.
La riproducibilità dell'analisi del litio in soluzione acquosa in mezzo basico, la stabilità del complesso litio-torino, la percentuale di Na e As presenti nella molecola, nonché gli spettri IR e NMR del prodotto ottenuto, dimostrano l'elevata grado di purezza del thorin sintetizzato.
BIBLIOGRAFIA
01. ALDRICO. Catalogo Manuale di chimica fine . Ed. Aldrich Chemical Company Inc. 1994 – 1995.
02. CAICEO AF Progettazione Sperimentale . S. ed. sf
03. CHARLOT G. Determinazione colorimetrica degli elementi (principi e metodi) Ed. Elsever Publishing Company, 1964
04. DOMÍNGUEZ XA Chimica Organica Sperimentale . Ed.Limusa SA 1982
05. GOULD ES Meccanismo e strutture in chimica organica . Ed. Kapeluz. 1967
06. KIRK E VARI. Enciclopedia della tecnologia chimica . Ed. ispano-americana, 19959
07. MILLER JC Statistiche per la chimica analitica . Ed. Addison - Wesley Iberoamericana, SA Seconda Edizione 1993.
08. THOMASON PF Anal Chem 28 (1956)
09. WARREN S. Organic Synthesis Design (Introduzione al metodo Synthon) . Ed. Alhambra, 1983.
Wilbert Rivera Munoz. Questo indirizzo email è protetto dagli spambots. È necessario abilitare JavaScript per vederlo.