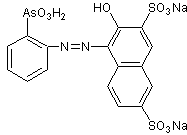
ТОРИН СИНТЕЗ
Аналитическое применение торина, рабочие параметры, его ограничения и перспективы рассматриваются и объясняются достаточно подробно в специализированных публикациях по химическому анализу, таких как Analytical Chemistry . Краткий обзор их показывает следующие приложения:
В кислой среде : используется для количественного определения элементов тория (Th), циркония (Zr), фтора (F), гафния (Hf) и урана (U).
В щелочной среде : Форма дисульфоновой кислоты тора, более известная как Торон, используется для количественного определения лития (Li).
В нейтральной среде : торин используется как индикатор для определения сульфат-ионов (SO 4 2- ) в водных растворах.
Торин также используется для определения SO 2 в воздухе.
Исследовательская проблема.
Учитывая спрос на этот реагент для различных аналитических определений и, в частности, для колориметрического анализа лития в рассолах из Гран-Салар-де-Уюни и малое предложение его на национальном рынке, возникает необходимость синтезировать торин из простых и доступных материалов . в нашей среде.
С этой целью к разработанным маршрутам синтеза подходят из парадигмы РЕТРОСИНТЕЗ , к которым применимы методы Листов Синтеза, Метод Разъединения или Синтона и Метод Дерева. синтеза.
Что касается синтеза торина , то в литературе имеется краткое и обобщенное описание синтеза торона. , согласно предложенному направлению Кузнецовым , т. е. указано, что для получения торона необходимо диазосопопулирование о-аминофениларсоновой кислоты с динатриевой солью 2-наптол-3,6-дисульфокислоты (соль R) в кислая среда.
Синтез дизайна для Thorina .
К дизайну подходит метод отключения или Sintón, который предусматривает два этапа. Первый связан с ретросинтетическим анализом, а второй — с синтезом в направлении того, что происходит в лаборатории, то есть от исходных материалов до достижения молекулы-мишени (МОб).
к) Предметы структурную и реакционную способность, которые необходимо учитывать для ретросинтетического анализа
Торин обычно представляет собой азосоединение, поэтому является красителем. Получение этих соединений обычно включает две основные реакции: диазоирование и диазосочетание (или просто связывание).
С другой стороны, все молекулы-предшественники сочетания, используемые для образования азокрасителей, имеют общий характер, а именно: активный атом водорода, связанный с атомом углерода.
В качестве молекул-предшественников (субстратов) для связывания широко используются следующие соединения: соединения с фенольными гидроксилами, такие как фенолы и нафтолы, ароматические амины, молекулы с енолизуемыми алифатическими кетоновыми группами и гетероциклические молекулы, такие как пиррол, индол и т. д.
В отношении реакции копуляции необходимо учитывать некоторые эвристические принципы, а именно:
· Фенолы связываются легче, чем амины, а члены нафталинового ряда легче, чем бензол.
· Заместители с отрицательным индуктивным эффектом (-I), такие как галогены, нитро, сульфамидные, карбоксильные и карбонильные группы, замедляют связывание.
· Алкильная или алкоксигруппа в орто- или метаположении по отношению к аминогруппе способствует связыванию. А если они находятся в положениях 2 и 5 по отношению к аминогруппе, они являются особенно хорошими связующими.
· В бензольном ряду связывание обычно происходит в пара- положении по отношению к гидроксильной (-ОН) или аминогруппе (-NH 2 ). Если позиция for занята, связь происходит в орто-позиции.
· В ряду нафталина, когда аминогидроксильная группа находится в положении 2 ( б ), реагент связан в положении 1 ( а ). Если гидроксильная или аминогруппа находится в альфа-положении, связь обычно возникает в 4-м положении; но если положение 3 или 6 занято сульфогруппой, то соединение происходит в бета-положении.
· Когда есть два возможных положения связывания, положение связи часто определяется рН среды: связывание происходит в орто-положении к аминогруппе, когда оно осуществляется в кислой среде, и в орто- положении к гидроксильной группе, когда оно осуществляется в кислой среде. осуществляется в основной среде.
На основе ранее упомянутых эвристических элементов существуют различные схемы синтеза торина, которые реагируют на ретросинтетический анализ . , предложил . Что по сути является конвергентным синтезом, выраженным диазосочетание динатриевой соли 2-нафтол-3,6-дисульфоновой кислоты, широко известной как «R-соль», с ортодиазофениларзонхлоридом в кислой среде
В ретросинтетическом анализе можно увидеть, что ключевым или стратегическим промежуточным продуктом является орто -нитроанилин, аспект, который приводит к простые исходные материалы, такие как бензол и нафталин соответственно.
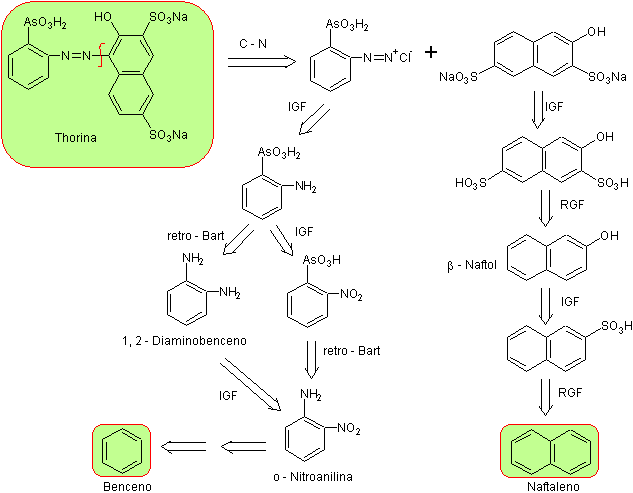
Источник: самодельный
Ортонитроанилин , Его можно синтезировать разными способами, с разным уровнем сложности и выходом. Из одиннадцати экспериментально исследованных альтернатив в розетке ретросинтеза указаны только восемь.
Из него для данной публикации были выбраны варианты отключения 3 и 4. , которые, в свою очередь, порождают два конвергентных пути синтеза.
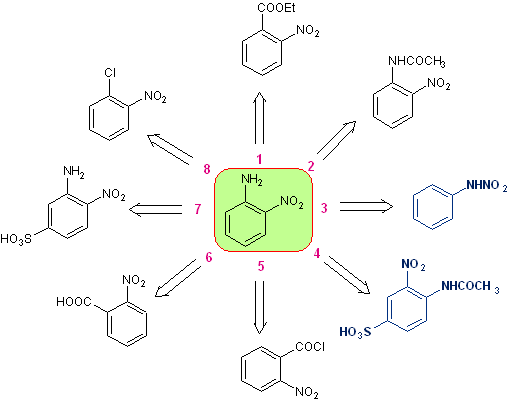
Розетка ретросинтеза орто-нитроанилина
б) Синтез «соли Р».
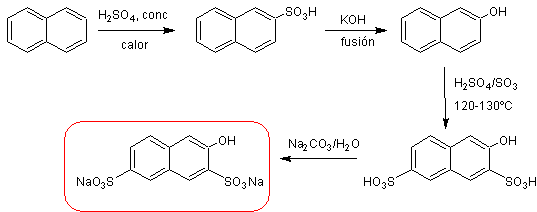
в) Синтез торина.
Путь синтеза I : стратегия учитывает образование орто -нитроанилина из Нитроаминовая перегруппировка нитранилина в кислой среде.
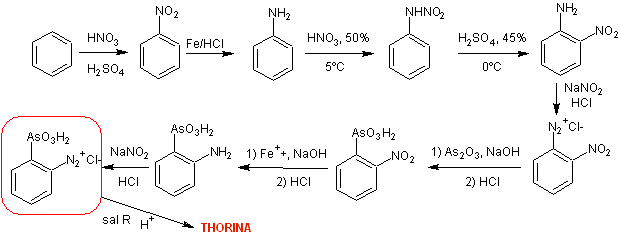
Синтез Путь II. Стратегия включает образование орто -нитроанилина посредством процессов защиты и снятия защиты пара- положения анилина.
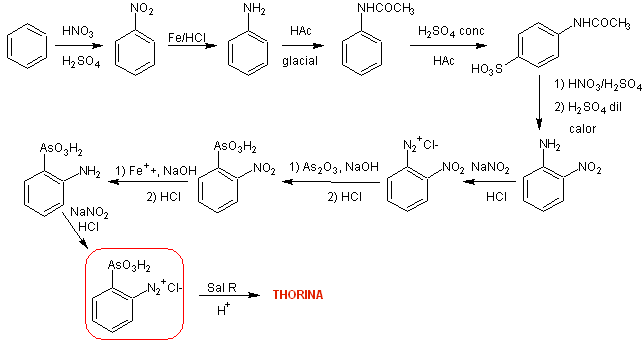
Полученные результаты
Эксперименты, разработанные для каждой стадии различных Путей Синтеза, соответствовали плану 2 2 факторного эксперимента, который позволил нам исследовать основной эффект факторов и взаимодействие между ними. , для оптимизации условий труда.
ü Экспериментальные результаты приготовления «соли R».
нафталин ![]() β-нафталинсульфонат натрия
β-нафталинсульфонат натрия ![]() β-нафтол
β-нафтол ![]() «соль Р»
«соль Р»
р 1 = 87,89% г2 = 86,55% г3 =75,23%
Выход сульфирования β -нафтола относительно низок, поскольку при той же температуре сульфирования другие продукты, такие как соль Шеффера (2-нафтол-6-сульфонат натрия) и небольшие количества натриевой соли 2-нафтола-6,8- дисульфоновая кислота (кислота G), натриевая соль которой более растворима, чем «соль R», аспект, который используется в процессе перекристаллизации «соли R».
Общий доход : Р соль Р = (r 1 *r 2 *r 3 )*100
= (0,8789*0,8655*0,7523)*100 = (0,5723)*100 = 57,23%
ü Экспериментальные результаты для пути синтеза I.
Процесс, который начинается с бензола до получения орто -диазофениларзонхлорида. (Cl-о-ДФА), состоит из восьми стадий и достигает выхода R Cl-о-ДФА = 23,39%.
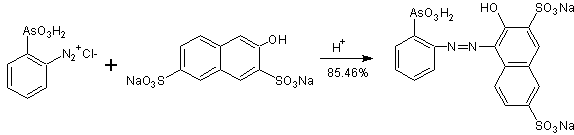
С другой стороны, реакция в кислой среде орто -диазофениларзонхлорида с «солью R», приготовленной по ранее указанным схемам, с получением ТОРИНА дает выход 85,46% .
На основании этих экспериментальных результатов общий выход (Q TSI ) Синтеза I с доверительной вероятностью 95% составляет:
QTSI = [(57,23% + 23,39%)/2]*85,46 = 34,45%
Собственная себестоимость производства тория на пути Синтеза I составляет 0,81 долл.США/г.
ü Экспериментальные результаты для Synthesis Route II.
В этом новом варианте синтеза бензол превращается в орто -диазофениларзонхлорид в девять стадий с выходом RCl-o-DFA = 28,04%.
Реакция этой соли, орто -диазофениларзонхлорида, с солью R" в кислой среде, как указано выше, достигает выхода 85,46%, для которого общий выход пути синтеза II ( QTSII ) составляет 36,44%.
Собственная стоимость производства торина по этому пути синтеза составляет 1,17 долл.США/г.
выводы
Различные пути синтеза, предложенные и проверенные, демонстрируют, что органический синтез, сердце органической химии, является в высшей степени предсказательной дисциплиной и является очень ценным педагогическим инструментом.
Ретросинтетический анализ, выраженный методологией отключения в плоскости проектирования и использованием факторных экспериментальных планов, используемых на практике, представляет собой мощную комбинацию, позволяющую столкнуться с работами по органическому синтезу значительных уровней глубины.
Воспроизводимость анализа лития в водных растворах в щелочной среде, стабильность литий-торинового комплекса, процентное содержание Na и As в молекуле, а также ИК- и ЯМР-спектры полученного продукта свидетельствуют о высокой степень чистоты синтезированного торина.
БИБЛИОГРАФИЯ
01. ОЛДРИХ. Каталог Справочник тонкой химии . Эд Олдрич Кемикал Компани Инк., 1994 – 1995 гг.
02. CAICEO AF Экспериментальный дизайн . С. изд. нф
03. ШАРЛО Г. Колориметрическое определение элементов (принципы и методы) Эд Elsever Publishing Company, 1964
04. ДОМИНГЕС XA Экспериментальная органическая химия . Эд Лимуса С.А., 1982 г.
05. ГУЛД Э.С. Механизмы и структуры в органической химии . Эд Капелуз. 1967 г.
06. КИРК И РАЗНЫЕ. Энциклопедия химической технологии . Испано-американское издание, 19959 г.
07. МИЛЛЕР Дж. К. Статистика аналитической химии . Эддисон - Уэсли Ибероамерикана, SA, второе издание, 1993 г.
08. THOMASON PF Anal Chem 28 (1956)
09. УОРРЕН С. Дизайн органического синтеза (Введение в метод Synthon) . Эд Альгамбра, 1983.
Уилберт Ривера Муньос. Адрес электронной почты защищен от спам-ботов. Для просмотра адреса в вашем браузере должен быть включен Javascript.