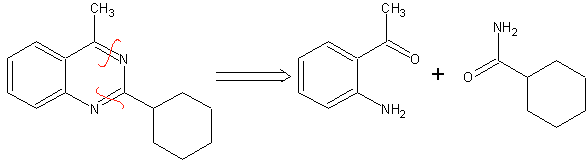
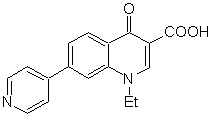
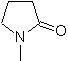
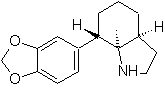
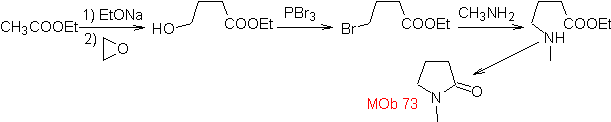SINTESI DI ETEROCICLI MEDIANTE CICLAZIONE INTRAMOLECOLARE
Anche la costruzione di sistemi eterociclici utilizza queste stesse reazioni, con la particolarità che il sistema eterociclico deve essere presente o contenere almeno un atomo diverso dal carbonio. I più comuni sono azoto, ossigeno, zolfo e fosforo.
Il sistema ciclico della molecola da sintetizzare può derivare dalla modifica di un sistema ciclico presente in uno dei reagenti coinvolti nella sintesi o essere il risultato della ciclizzazione di antecedenti non ciclici e che è stato costruito nello sviluppo della sintesi mediante ciclizzazione intramolecolare o mediante metodi basati su ciclizzazioni intermolecolari (cicloaddizioni).
1. Ciclizzazione intramolecolare
Le regole generali per la disconnessione degli eterocicli originati da una ciclizzazione intramolecolare, sono state adeguatamente sistematizzate da JI Borrell , gli stessi assunti in questa sezione (Het = N, O, S)
1.
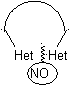
Nella sintesi di un composto monociclico, la chiusura dell'anello comporta generalmente la formazione di un legame carbonio-eteroatomo.
Modello: |
|
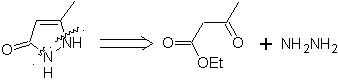
Esempio: |
|
|
|
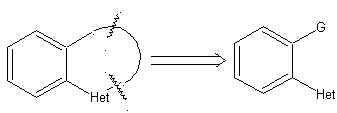
Esempio : |
|
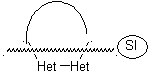
Modello: |
|
Esempio: |
|
1.1. Modelli di ciclizzazione intramolecolare
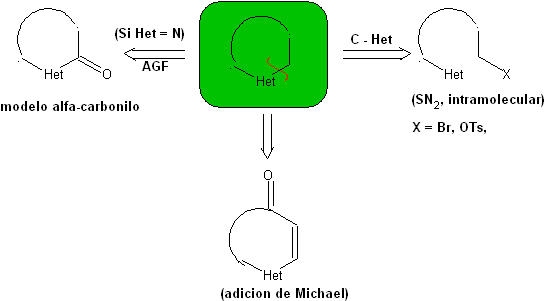
Si possono citare tre modelli di ciclizzazione intramolecolare e le corrispondenti disconnessioni:
Modello saturo:
| modello α-insaturo
| Modello α-carbonile
|
1.1.1.
modello saturo
Proporre un progetto di sintesi, a partire da materiali semplici ed economici, per le seguenti molecole:
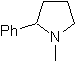
MOb 65
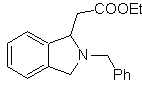
| … | MOb 66
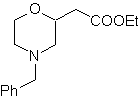
| … | folla 67
|
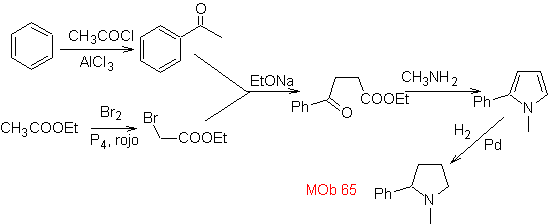
Sintesi. Si inizia con l'acilazione di Friedel-Crafts del benzene da un lato e dall'altro con la bromurazione dell'acetato di etile, secondo HVZ.Le fasi successive richiedono il lavoro in un mezzo basico e alla fine si procede all'idrogenazione dei centri insaturi raggiungere
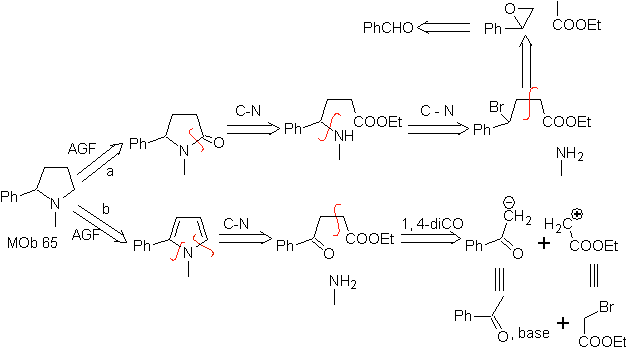
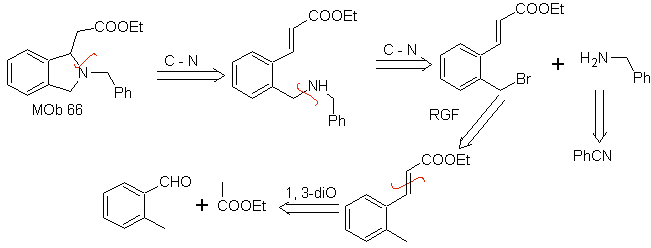
Assalire. 66. Analisi retrosintetica . L'attacco dell'N nucleofilo al carbonio β, in relazione al gruppo estere, (MOb 66) fa pensare che sia stato formato da un'addizione di Michael coniugato intramolecolare di un'ammina su un estere α, β insaturo. La disconnessione C-N dà luogo ad altre disconnessioni comuni, fino a giungere a materiali di partenza semplici.
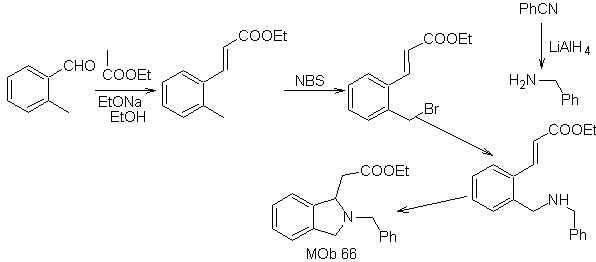
sintesi . L'o-metil benzaldeide può essere preparata, se necessario, mediante reazione di Gattermann-Koch su acido para-metilsolfonico. Il resto delle reazioni, per la sintesi di
MOb 67. Analisi retrosintetica. Come nell'esempio precedente, il legame CO in posizione β al gruppo estere, in
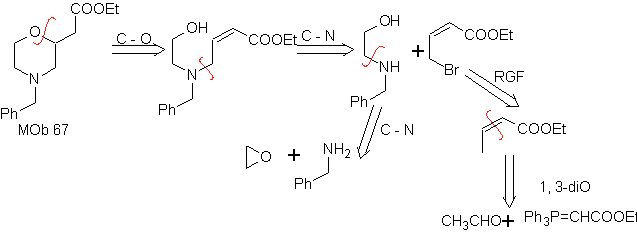
Sintesi. La sintesi di
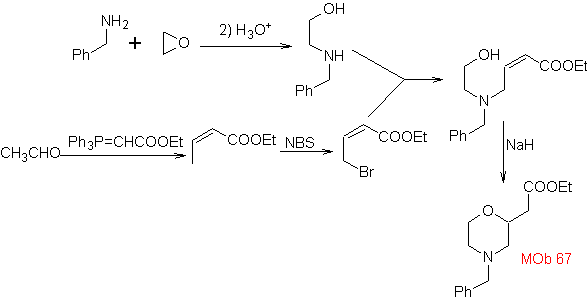
1.1.2.
modello α-insaturo
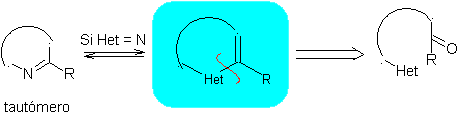
Proponi un progetto di sintesi da materiali semplici ed economici, per le seguenti molecole:
MOb: 68
| MOb: 69
| MOb: 70
| MOb: 71
|
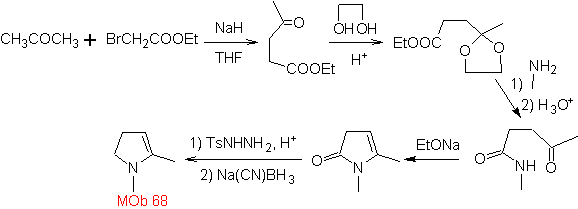
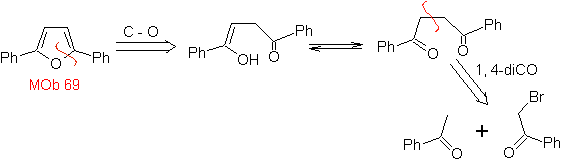
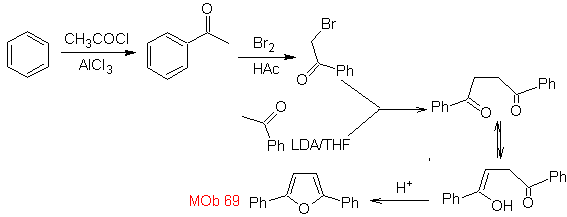
MOb 68. Analisi retrosintetica . Il processo di disconnessione
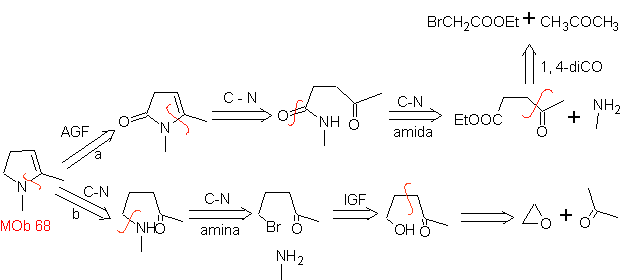
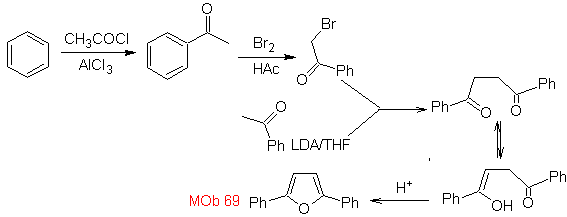
Sintesi. Le vie della disconnessione, di
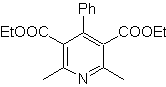
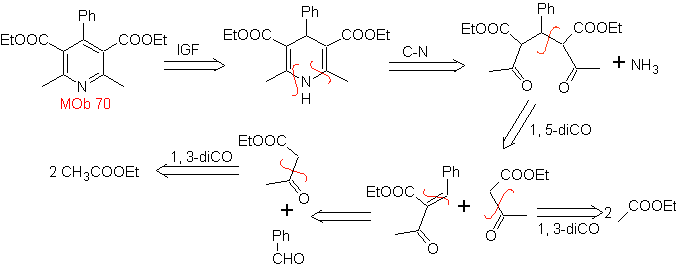
Assalire. 70 . Analisi retrosintetica . Questo MOb è un derivato della piridina, la struttura che presenta è caratteristica dei prodotti formati nella sintesi della piridina di Hansch, cioè il ciclo della piridina deve essere formato da un'aldeide e due moli di composto 1,3-diCO e ossidare l'intermedio diidrochinone formato .
MOb 71 . Analisi retrosintetica.
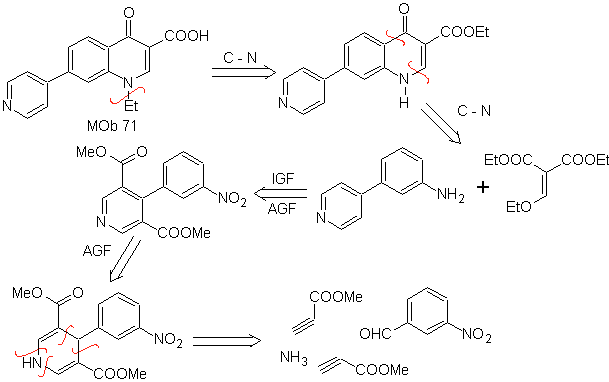
La disconnessione simultanea, sul chetone e sull'ammina, mostra che l'anilina e il composto carbonilico si sono condensati. Poiché l'introduzione dell'anello benzenico in una piridina è improbabile, viene adottata la strategia di costruire l'anello piridinico da appropriati derivati acetilidici.
sintesi . Gli esteri nitrilici, insieme alla m-nitrobenzaldeide, consentono la ciclizzazione intermolecolare per formare un derivato idropiridinico che viene ossidato a piridina con conc HNO 3 .
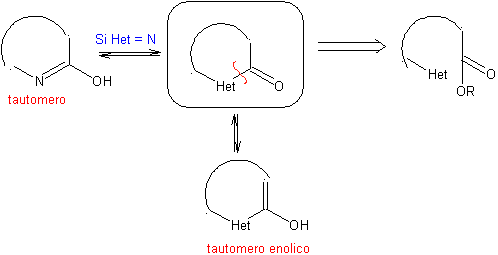
Poi lui gruppo nitro, permette di costruire l'anello piridinico chinolina, mediante reazioni di condensazione con un opportuno composto diCO. etilazione

Proporre un piano di sintesi, a partire da materiali semplici, per le seguenti molecole:
MOb: 72
| MOb: 73
| MOb: 74
|
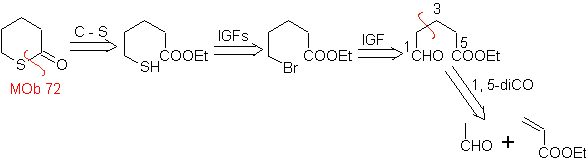
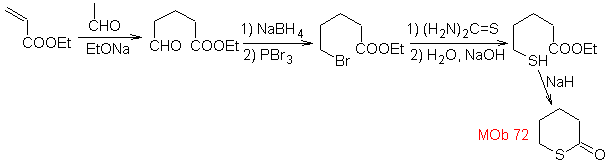
MOb 72. Analisi retrosintetica . Questo MOb è un tetraidropiranone, è disconnesso dal legame S-CO. I seguenti IGF consentono la formazione di un precursore 1,5-diCO che, una volta disconnesso, fornisce i materiali di partenza.
MOb 73. Analisi retrosintetica . La disconnessione del legame lattamico ammidico genera la prima molecola precursore, che è un γ. estere amminico, che si forma tra un'ammina primaria e il γ-bromoestere e di conseguenza γ-idrossiestere, che viene fatto reagire tra acetato di etile enolato e un epossido come materiali di partenza semplici ed economici.
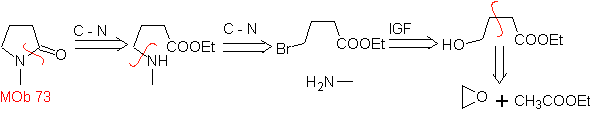
Sintesi : L'epossido e l'acetato etile sono i reagenti che reagiscono per formare il γ -idroestere. L'OH è sostituito dal bromo con PBr 3 e questo reagisce con la metilammina. formare la molecola precursore che si chiude in un anello lattamico, formare