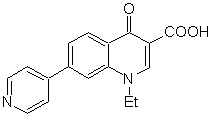
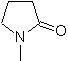
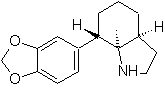
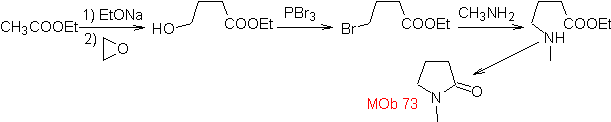SYNTHESE D'HETEROCYCLES PAR CYCLATION INTRAMOLECULAIRE
La construction de systèmes hétérocycliques utilise également ces mêmes réactions, avec la particularité que le système hétérocyclique doit être présent ou contenir au moins un atome autre que le carbone. Les plus courants sont l'azote, l'oxygène, le soufre et le phosphore.
Le système cyclique de la molécule à synthétiser peut provenir de la modification d'un système cyclique présent dans l'un des réactifs impliqués dans la synthèse ou être le résultat d'une cyclisation d'antécédents non cycliques et qui a été construit dans le développement de la synthèse par cyclisation intramoléculaire ou par des méthodes basées sur des cyclisations intermoléculaires (cycloadditions).
1. Cyclisation intramoléculaire
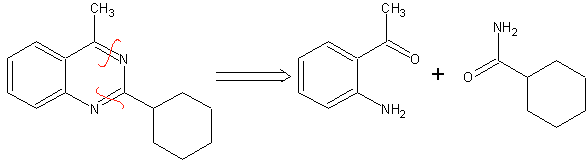
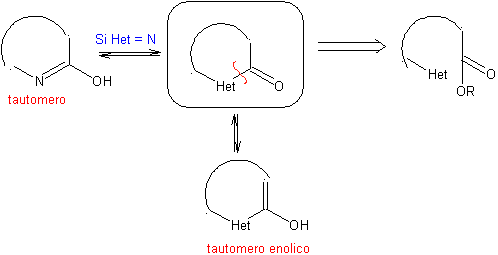
Les règles générales de déconnexion des hétérocycles issus d'une cyclisation intramoléculaire, ont été adéquatement systématisées par JI Borrell , les mêmes que ceux supposés dans cette section (Het = N, O, S)
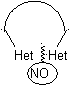
1. Dans la synthèse d'un composé monocyclique, la cyclisation implique généralement la formation d'une liaison carbone-hétéroatome.
|
Modèle:
|
|
|
Exemple: |
|
|
|
|
|
|
Exemple :
|
|
|
Modèle:
|
|
|
Exemple:
|
|
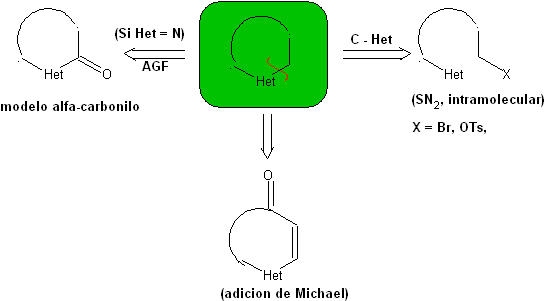
1.1. Modèles de cyclisation intramoléculaire
Trois modèles de cyclisation intramoléculaire et les déconnexions correspondantes peuvent être mentionnés :
|
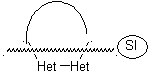
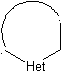
Modèle saturé :
|
|
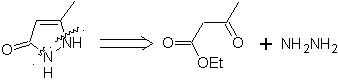
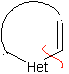
modèle α-insaturé
|
|
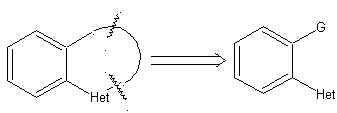
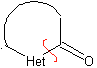
modèle α-carbonyle
|
1.1.1. modèle saturé
Proposer un design de synthèse, à partir de matériaux simples et abordables, pour les molécules suivantes :
|
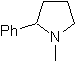
Mob 65
|
… |
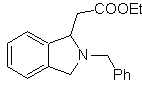
Mob 66
|
… |
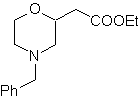
foule 67
|
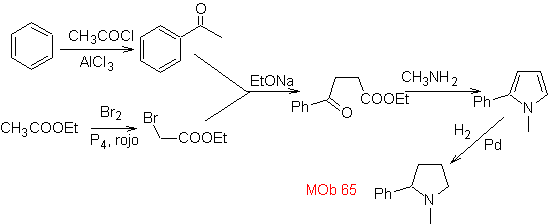
La synthèse. Elle commence par l'acylation de Friedel-Crafts du benzène d'une part et d'autre part par la bromuration de l'acétate d'éthyle, selon HVZ.Les étapes suivantes nécessitent un travail en milieu basique et à la fin on procède à l'hydrogénation des centres insaturés atteindre
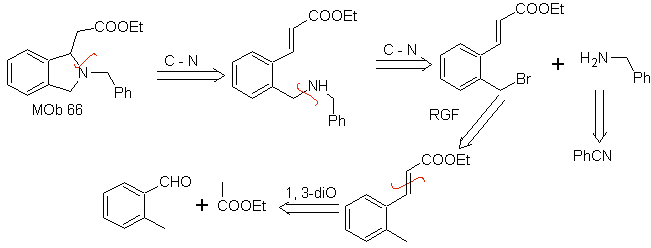
Foule. 66. Analyse rétrosynthétique . L'attaque du N nucléophile sur le carbone β, par rapport au groupement ester, (MOb 66) oriente à penser qu'il a été formé par une addition intramoléculaire conjuguée de Michael d'une amine sur un ester α, β insaturé. La déconnexion C-N donne lieu à d'autres déconnexions courantes, jusqu'à atteindre des matières premières simples.
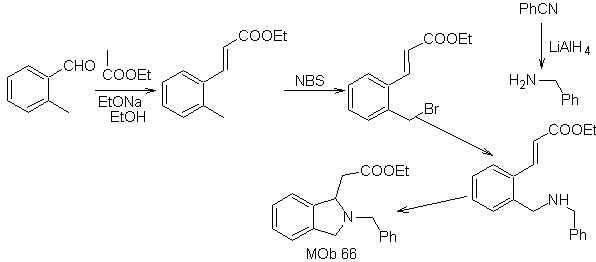
synthèse . L'o-méthyl benzaldéhyde peut être préparé, si nécessaire, par la réaction de Gattermann-Koch sur l'acide para-méthyl sulfonique. Le reste des réactions, pour la synthèse de
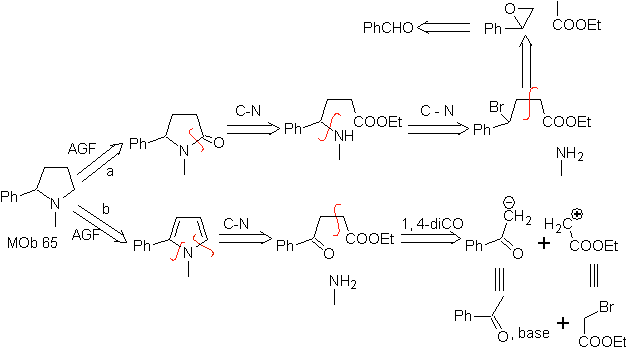
MOb 67. Analyse rétrosynthétique. Comme dans l'exemple précédent, la liaison CO en position β par rapport au groupe ester, dans
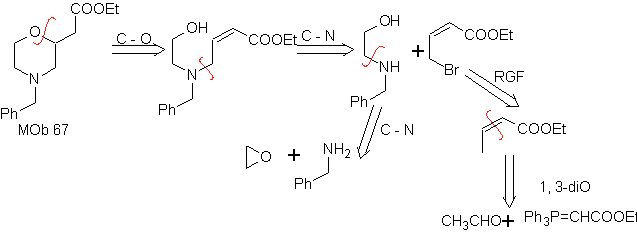
La synthèse. La synthèse de
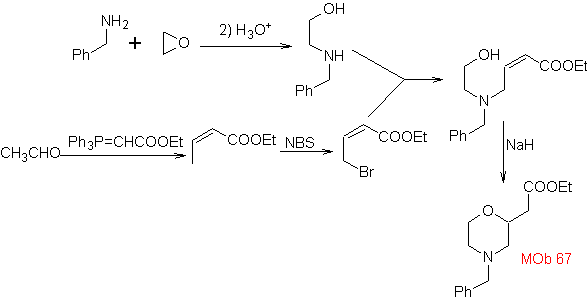
1.1.2. modèle α-insaturé
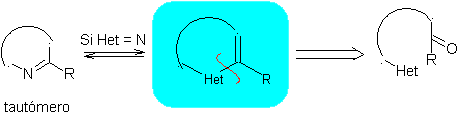
Proposer un design de synthèse à partir de matériaux simples et abordables, pour les molécules suivantes :
|
Mob : 68
|
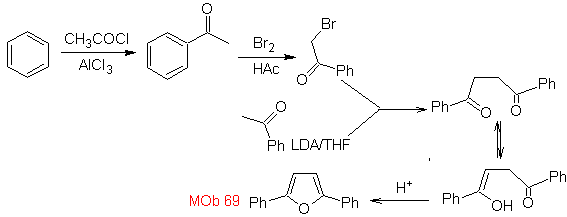
Mob : 69
|
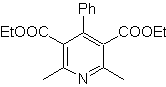
Mob : 70
|
Mob : 71
|
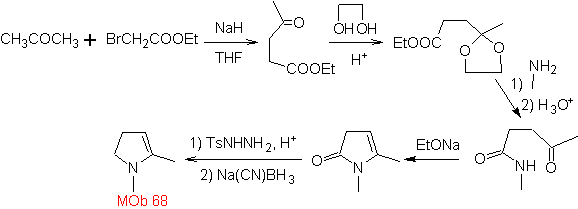
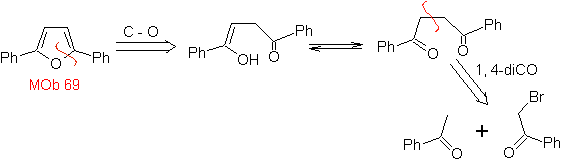
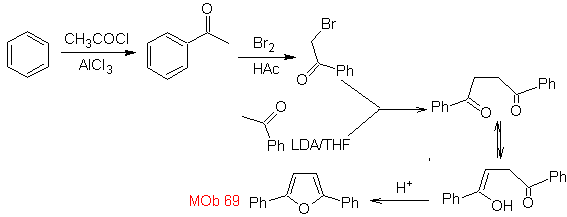
MOb 68. Analyse rétrosynthétique . Le processus de déconnexion
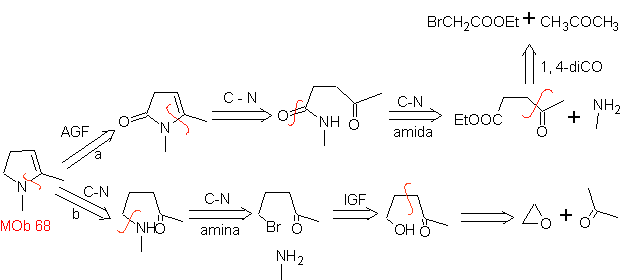
La synthèse. Les voies de déconnexion, de
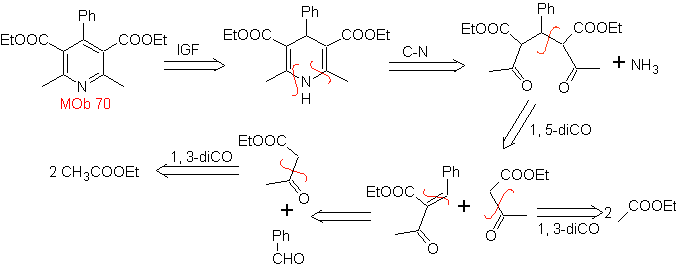
Foule. 70 . Analyse rétrosynthétique . Ce MOb est un dérivé de la pyridine, la structure qu'il présente est caractéristique des produits formés dans la synthèse de la pyridine de Hansch, c'est-à-dire que le cycle de la pyridine doit être formé à partir d'un aldéhyde et de deux moles de composé 1,3-diCO et oxyder la dihydroquinone intermédiaire formé .
Mob 71 . Analyse rétrosynthétique.
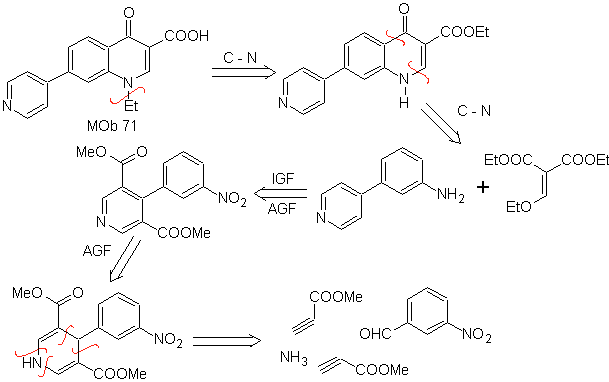
La déconnexion simultanée, sur la cétone et l'amine, montre que l'aniline et le composé carbonylé se sont condensés. Étant donné que l'introduction du cycle benzénique dans une pyridine est peu probable, la stratégie de construction du cycle pyridine à partir de dérivés d'acétylure appropriés est adoptée.
synthèse . Les esters nitriles, associés au m-nitrobenzaldéhyde, permettent une cyclisation intermoléculaire pour former un dérivé d'hydropyridine qui est oxydé en pyridine avec HNO3 conc.
Puis il groupe nitro, permet de construire le cycle quinoléine pyridine, par des réactions de condensation avec un composé diCO approprié. éthylation

Proposer un plan de synthèse, à partir de matériaux simples, pour les molécules suivantes :
|
Mob : 72
|
|
Mob : 73
|
|
Mob : 74
|
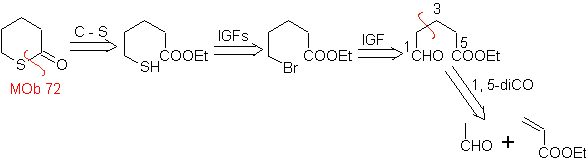
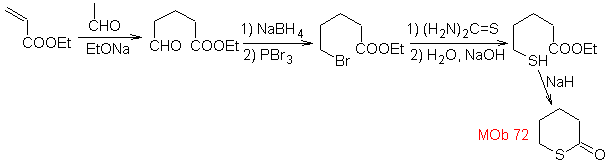
MOb 72. Analyse rétrosynthétique . Ce MOb est une tétrahydropyranone, elle est déconnectée par la liaison S-CO. Les IGF suivants permettent la formation d'un précurseur 1,5-diCO, qui, lorsqu'il est déconnecté, fournit les matières premières.
MOb 73. Analyse rétrosynthétique . La déconnexion de la liaison lactame amido génère la première molécule précurseur, qui est un γ. ester aminé, qui se forme entre une amine primaire et le Le γ-bromoester et par conséquent le γ-hydroxyester, qui est mis à réagir entre l'énolate d'acétate d'éthyle et un époxyde comme matières premières simples et abordables.
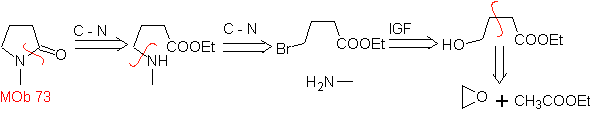
Synthèse : L'époxyde et l'acétate éthyle sont les réactifs qui réagissent pour former le γ -hydroester. L'OH est remplacé par du brome avec PBr 3 et celui-ci réagit avec la méthylamine. pour former la molécule précurseur qui se ferme dans un cycle lactame, pour former