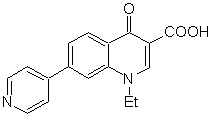
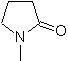
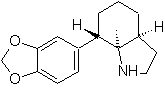
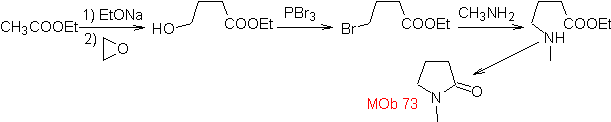СИНТЕЗ ГЕТЕРОЦИКЛОВ МЕТОДОМ ВНУТРИМОЛЕКУЛЯРНОГО ЦИКЛИРОВАНИЯ
Построение гетероциклических систем также использует те же самые реакции, с тем отличием, что гетероциклическая система должна присутствовать или содержать по крайней мере один атом, отличный от углерода. Наиболее распространены азот, кислород, сера и фосфор.
Циклическая система синтезируемой молекулы может происходить в результате модификации циклической системы, присутствующей в одном из реагентов, участвующих в синтезе, или быть результатом циклизации нециклических предшественников, которая была построена в ходе развития синтеза. внутримолекулярной циклизацией или методами, основанными на межмолекулярной циклизации (циклоприсоединения).
1. Внутримолекулярная циклизация
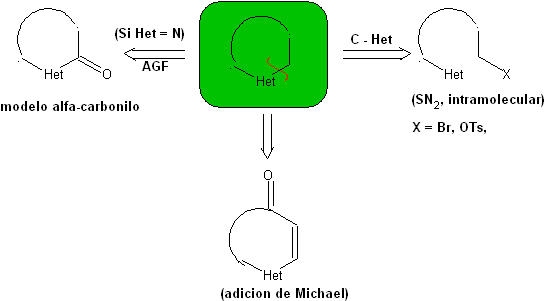
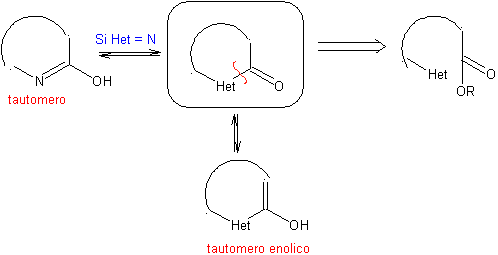
Общие закономерности разъединения гетероциклов, возникающих в результате внутримолекулярной циклизации, были адекватно систематизированы Дж. И. Боррелем. , те же, что и в этом разделе (Het = N, O, S)
1.
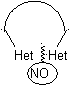
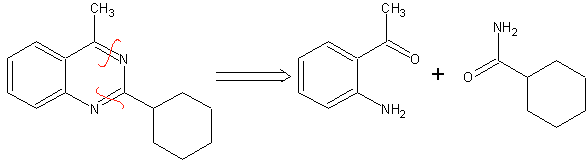
В синтезе моноциклического соединения замыкание кольца обычно включает образование связи углерод-гетероатом.
Модель: |
|
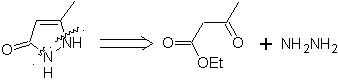
Пример: |
|
|
|
Пример : |
|
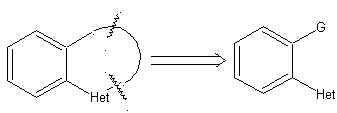
Модель: |
|
Пример: |
|
1.1. Модели внутримолекулярной циклизации
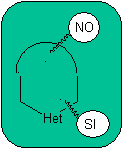
Можно назвать три модели внутримолекулярной циклизации и соответствующих разрывов:
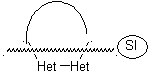
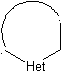
Насыщенная модель:
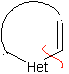
| α-ненасыщенная модель
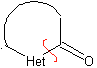
| α-карбонильная модель
|
1.1.1.
насыщенная модель
Предложите схему синтеза из простых и доступных материалов следующих молекул:
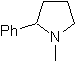
МОБ 65
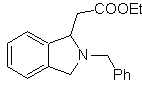
| … | МОБ 66
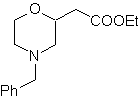
| … | моб 67
|
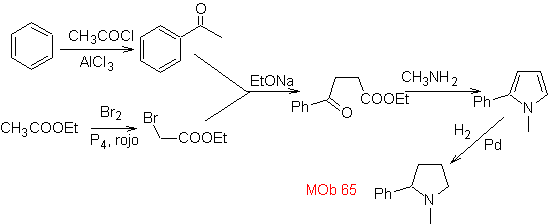
Синтез. Начинается с ацилирования бензола по Фриделю-Крафтсу с одной стороны и с бромирования этилацетата с другой по ХВЗ Следующие стадии требуют работы в основной среде и в конце переходим к гидрированию ненасыщенных центров достигать
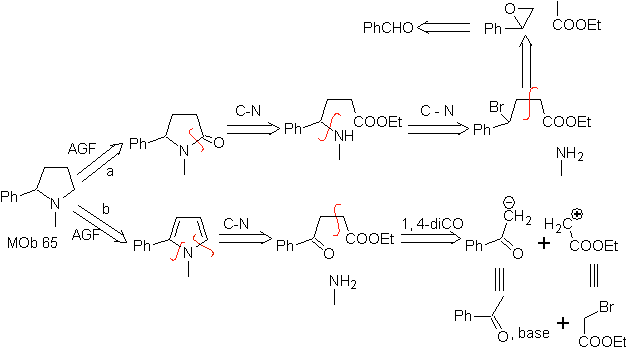
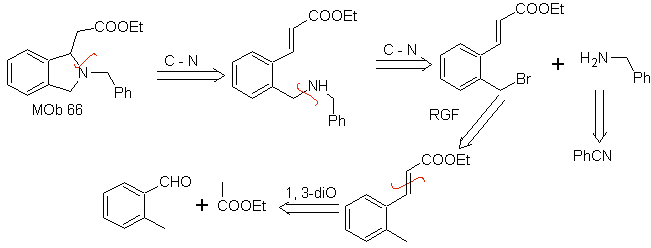
Моб. 66. Ретросинтетический анализ . Атака нуклеофильного N на β-углерод по отношению к сложноэфирной группе (MOb 66) заставляет думать, что он был образован внутримолекулярным сопряженным присоединением амина по Михаэлю к α, β-ненасыщенному сложному эфиру. Разъединение CN приводит к другим обычным разъединениям, пока не будут достигнуты простые исходные материалы.
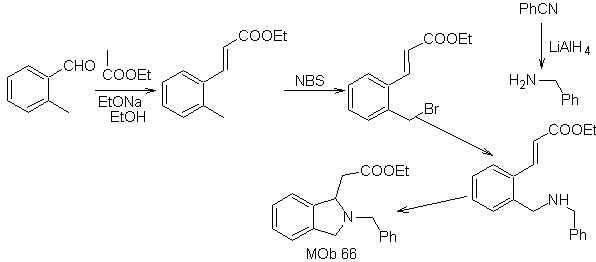
синтез . О-метилбензальдегид при необходимости можно получить по реакции Гаттермана-Коха с пара-метилсульфоновой кислотой. Остальные реакции, для синтеза
MOb 67. Ретросинтетический анализ. Как и в предыдущем примере, связь CO в положении β к сложноэфирной группе, в
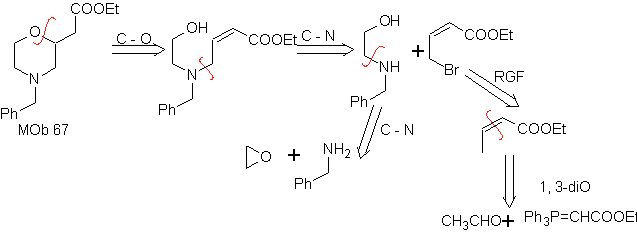
Синтез. Синтез
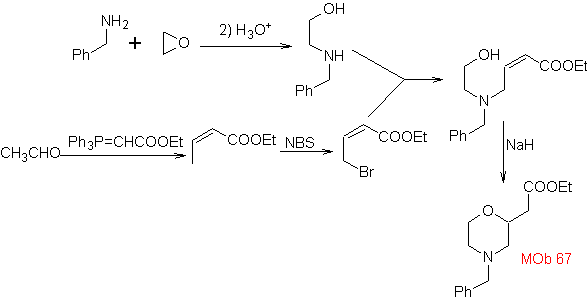
1.1.2.
α-ненасыщенная модель
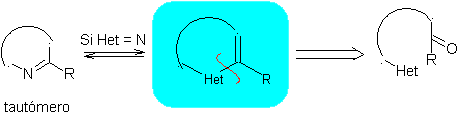
Предложите схему синтеза из простых и доступных материалов следующих молекул:
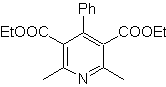
Моб: 68
| Моб: 69
| МОБ: 70
| Моб: 71
|
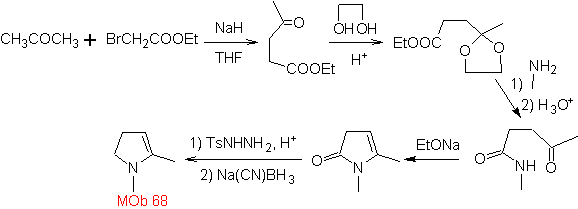
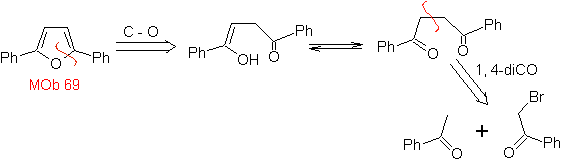
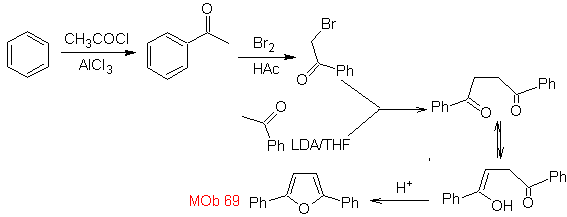
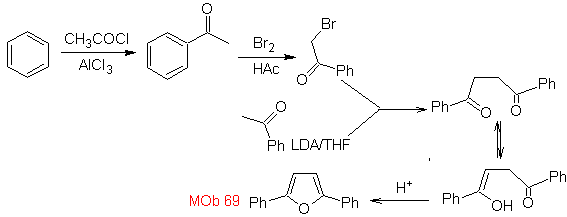
MOb 68. Ретросинтетический анализ . Процесс отключения
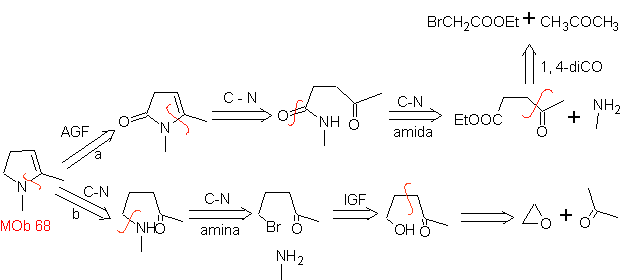
Синтез. Способы отключения,
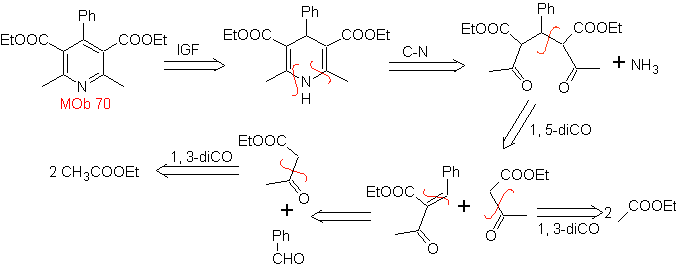
Моб. 70 . Ретросинтетический анализ . Этот MOb является производным пиридина, его структура характерна для продуктов, образующихся в синтезе пиридина Ханша, то есть пиридиновый цикл должен образовываться из альдегида и двух молей соединения 1,3-диСО и окислять промежуточный дигидрохинон. сформированный .
МОБ 71 . Ретросинтетический анализ.
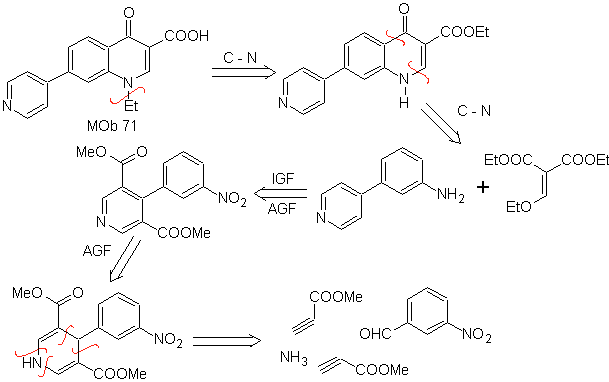
Одновременное отсоединение кетона и амина показывает, что анилин и карбонильное соединение конденсировались. Поскольку введение бензольного кольца в пиридин маловероятно, выбирается стратегия построения пиридинового кольца из соответствующих производных ацетилидов.
синтез . Нитрильные эфиры вместе с м-нитробензальдегидом обеспечивают межмолекулярную циклизацию с образованием производного гидропиридина, которое окисляется до пиридина концентрированной HNO 3 .
Затем он нитрогруппа позволяет построить пиридиновое кольцо хинолина путем реакций конденсации с подходящим соединением диСО. этилирование

Предложите план синтеза из простых материалов следующих молекул:
Моб: 72
| Моб: 73
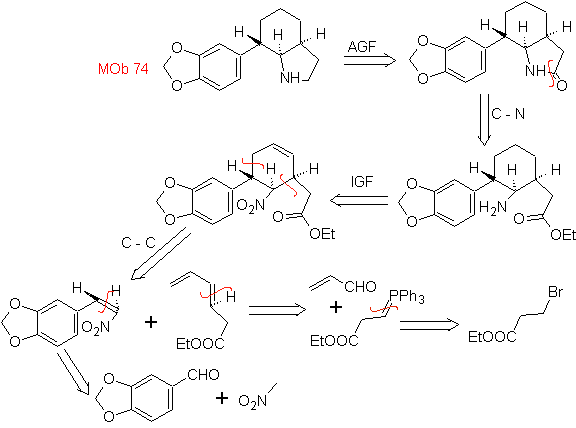
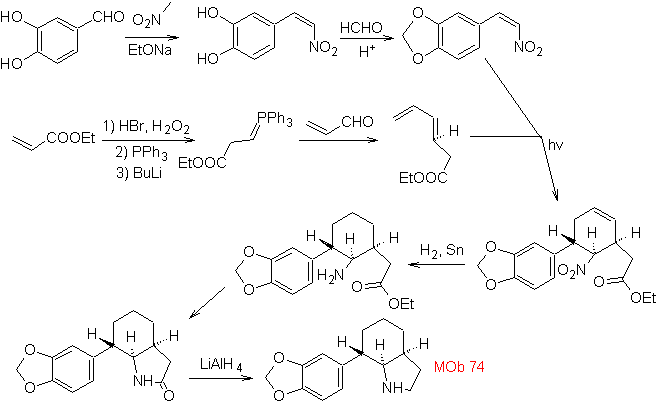
| Моб: 74
|
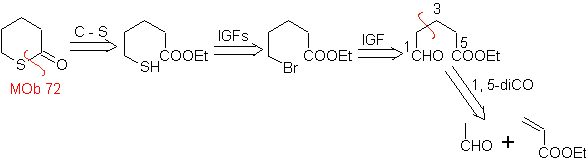
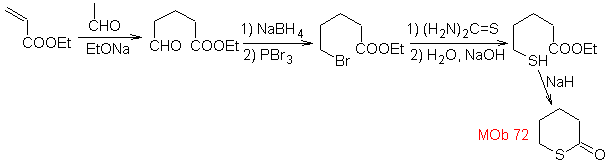
MOb 72. Ретросинтетический анализ . Этот MOb представляет собой тетрагидропиранон, он разъединен связью S-CO. Следующие IGF позволяют образовывать предшественник 1,5-diCO, который при отсоединении дает исходные материалы.
MOb 73. Ретросинтетический анализ . Разрыв амидной связи лактама приводит к образованию первой молекулы-предшественника, которая представляет собой γ. аминоэфир, который образуется между первичным амином и γ-бромэфир и, следовательно, γ-гидроксиэфир, которые реагируют между энолатом этилацетата и эпоксидом в качестве простых и доступных исходных материалов.
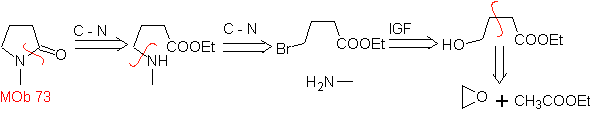
Синтез : Эпоксид и ацетат этил - это реагенты, которые реагируют с образованием γ -гидроэфира. OH заменяется бромом на PBr 3 и это реагирует с метиламином. с образованием молекулы-предшественника, замыкающейся в лактамное кольцо, с образованием