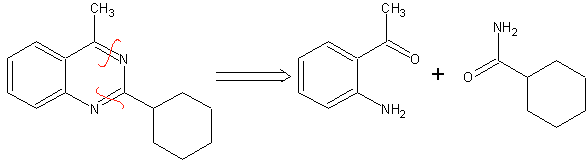
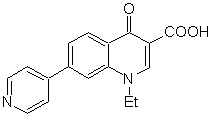
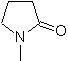
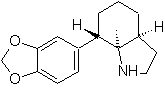
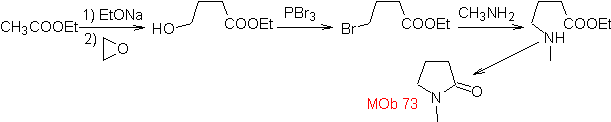SINTESIS HETEROSIKAL DENGAN SIKLASI INTRAMOLEKULER
Konstruksi sistem heterosiklik juga menggunakan reaksi yang sama ini, dengan kekhususan bahwa sistem heterosiklik harus ada atau mengandung setidaknya satu atom selain karbon. Yang paling umum adalah nitrogen, oksigen, belerang dan fosfor.
Sistem siklik molekul yang akan disintesis dapat berasal dari modifikasi sistem siklik yang terdapat pada salah satu reagen yang terlibat dalam sintesis atau merupakan hasil siklisasi anteseden nonsiklik dan yang telah dibangun dalam pengembangan sintesis. dengan siklisasi intramolekul atau dengan metode berdasarkan siklisasi antarmolekul (sikloadisi).
1. Siklisasi intramolekul
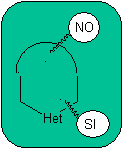
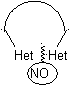
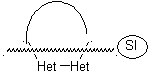
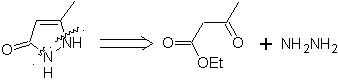
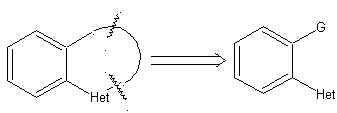
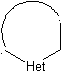
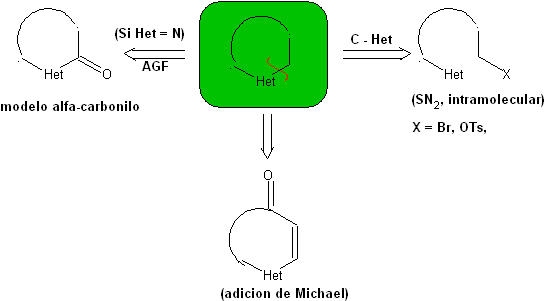
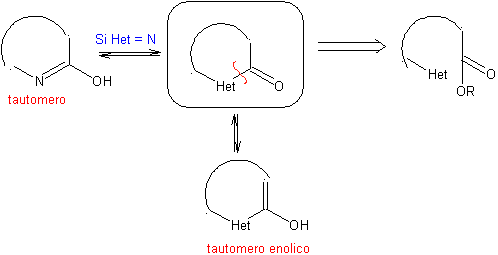
Aturan umum untuk pemutusan heterosiklik yang berasal dari siklisasi intramolekul, disistematisasi secara memadai oleh JI Borrell , sama seperti yang diasumsikan pada bagian ini (Het = N, O, S)
1.
Dalam sintesis senyawa monosiklik, penutupan cincin umumnya melibatkan pembentukan ikatan karbon-heteroatom.
Model: |
|
Contoh: |
|
|
|
Contoh : |
|
Model: |
|
Contoh: |
|
1.1. Model untuk siklisasi intramolekul
Tiga model untuk siklisasi intramolekul dan pemutusan yang sesuai dapat disebutkan:
Model jenuh:
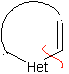
| model α-tak jenuh
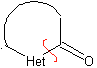
| model α-karbonil
|
1.1.1.
model jenuh
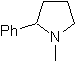
Usulkan desain sintesis, dari bahan yang sederhana dan terjangkau, untuk molekul-molekul berikut:
MO 65
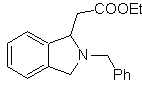
| … | MOb 66
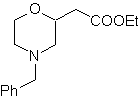
| … | massa 67
|
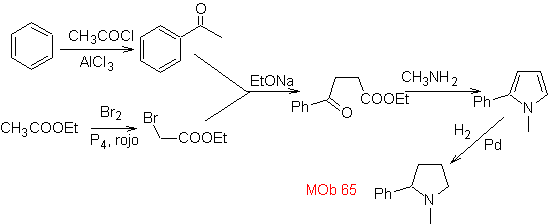
Perpaduan. Ini dimulai dengan asilasi Friedel-Crafts benzena di satu sisi dan di sisi lain dengan brominasi etil asetat, menurut HVZ. Tahapan berikut membutuhkan kerja dalam media dasar dan pada akhirnya kita melanjutkan ke hidrogenasi pusat tak jenuh untuk mencapai
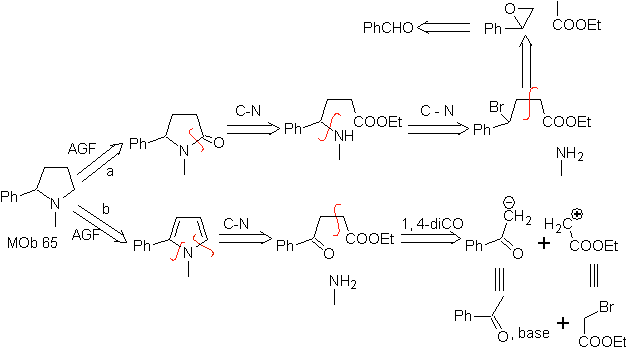
Massa. 66. Analisis Retrosintetik . Serangan nukleofilik N pada karbon β, dalam kaitannya dengan gugus ester, (MOb 66) mengarah pada anggapan bahwa ia dibentuk oleh penambahan amina Michael terkonjugasi intramolekul pada ester tak jenuh α, β. Pemutusan C-N memunculkan pemutusan umum lainnya, hingga mencapai bahan awal yang sederhana.
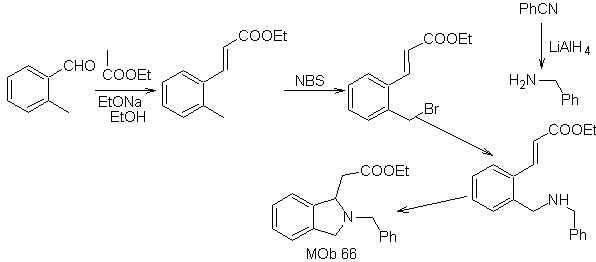
sintesis . O-metil benzaldehida dapat dibuat, jika perlu, dengan reaksi Gattermann-Koch pada asam para-metil sulfonat. Sisa reaksi, untuk sintesis
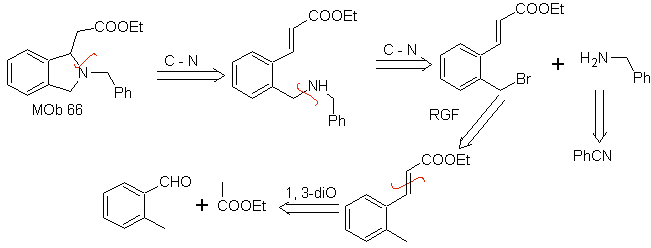
MOb 67. Analisis retrosintetik. Seperti pada contoh sebelumnya, ikatan CO pada posisi β ke gugus ester, in
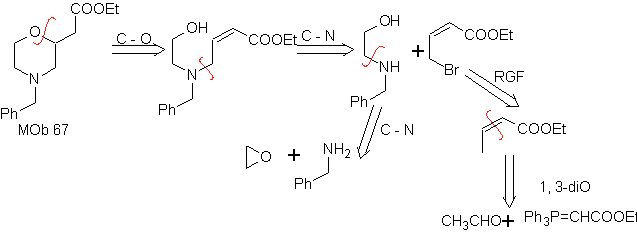
Perpaduan. Sintesis dari
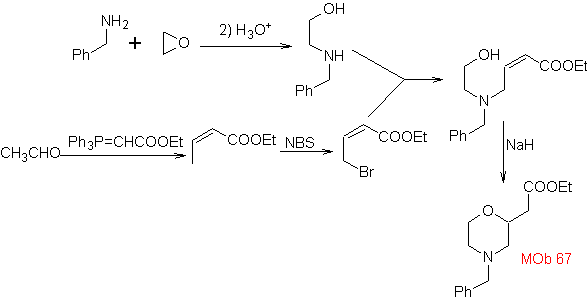
1.1.2.
model α-tak jenuh
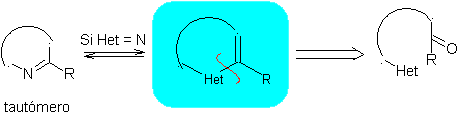
Usulkan desain sintesis dari bahan yang sederhana dan terjangkau, untuk molekul berikut:
MOb: 68
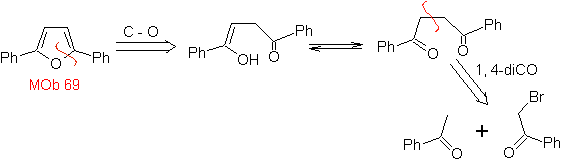
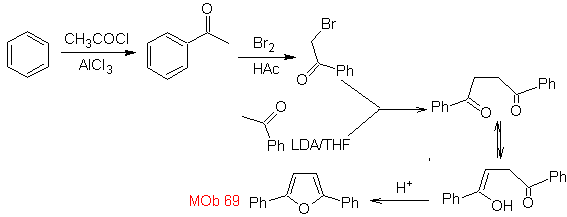
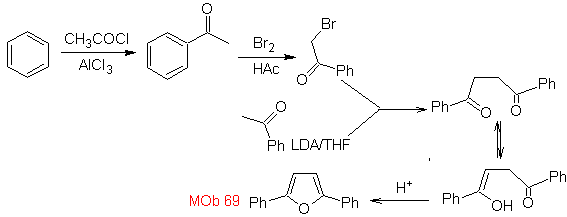
| MOb: 69
| MOb: 70
| MOb: 71
|
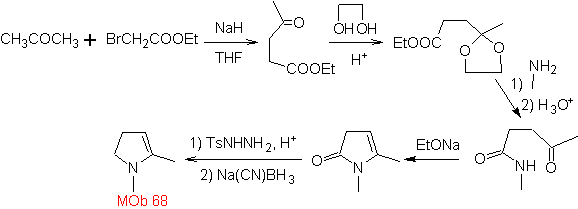
MOb 68. Analisis retrosintetik . Proses pemutusan
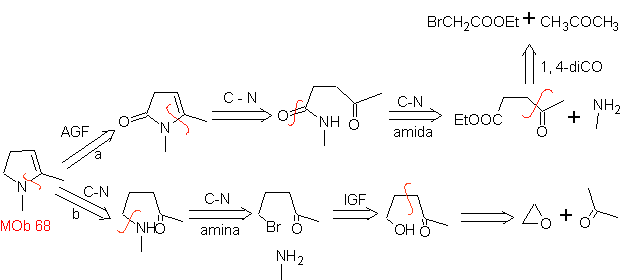
Perpaduan. Cara pemutusan, dari
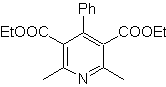
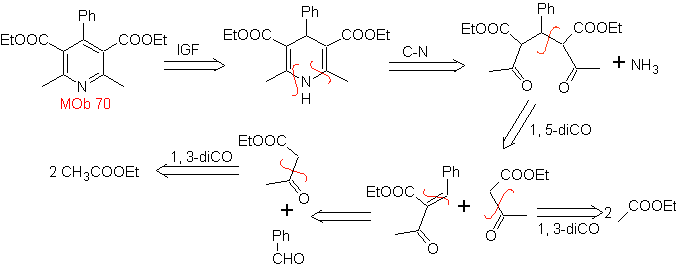
Massa. 70 . Analisis retrosintetik . MOb ini adalah turunan piridin, struktur yang disajikannya adalah karakteristik dari produk yang terbentuk dalam sintesis piridin Hansch, yaitu, siklus piridin harus dibentuk dari aldehida dan dua mol senyawa 1,3-diCO dan mengoksidasi perantara dihidrokuinon terbentuk .
MOb 71 . Analisis retrosintetik.
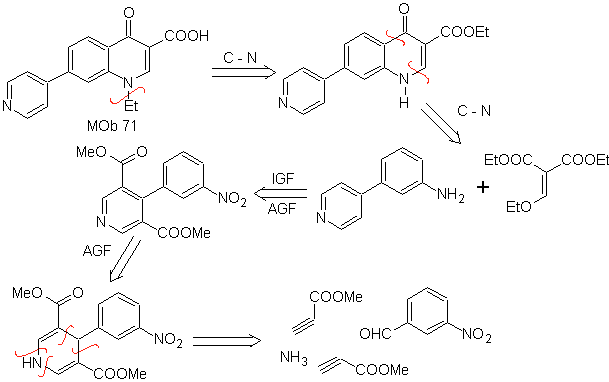
Pemutusan serentak, pada keton dan amina, menunjukkan anilin dan senyawa karbonil telah terkondensasi. Karena pengenalan cincin benzena ke dalam piridin tidak mungkin, strategi membangun cincin piridin dari turunan asetilida yang sesuai diambil.
sintesis . Ester nitril, bersama dengan m-nitrobenzaldehida, memungkinkan siklisasi antarmolekul untuk membentuk turunan hidropiridin yang dioksidasi menjadi piridin dengan konsentrasi HNO 3 .
Kemudian dia gugus nitro, memungkinkan untuk membangun cincin kinolin piridin, melalui reaksi kondensasi dengan senyawa diCO yang sesuai. etilasi

Usulkan rencana sintesis, dari bahan sederhana, untuk molekul berikut:
MOb: 72
| MOb: 73
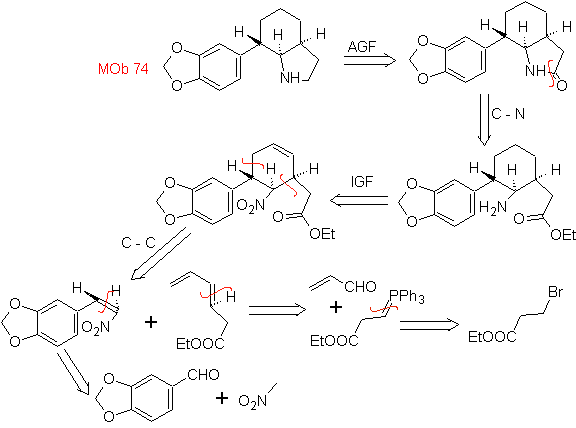
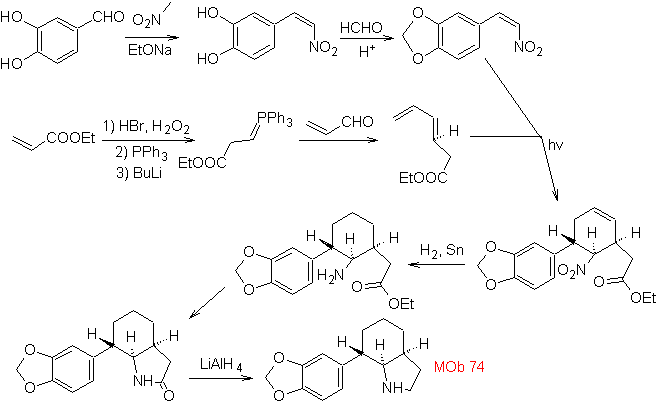
| MOb: 74
|
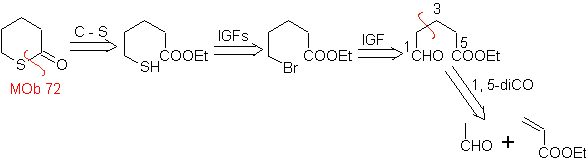
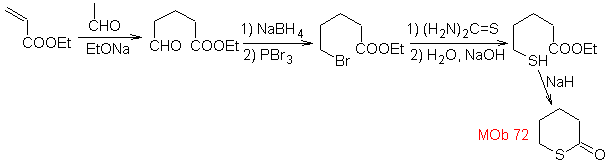
MOb 72. Analisis retrosintetik . Ini MOb adalah tetrahydropyranone, itu terputus oleh ikatan S-CO. IGF berikut memungkinkan pembentukan prekursor 1,5-diCO, yang, ketika dilepas, menyediakan bahan awal.
MOb 73. Analisis retrosintetik . Pemutusan ikatan laktam amido menghasilkan molekul prekursor pertama, yaitu γ. amino ester, yang terbentuk antara amina primer dan γ-bromoester dan akibatnya γ-hidroksiester, yang direaksikan antara etil asetat enolat dan epoksida sebagai bahan awal yang sederhana dan terjangkau.
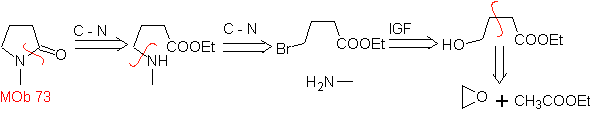
Sintesis : Epoksida dan asetat etil adalah reaktan yang bereaksi membentuk γ -hidroester. OH digantikan oleh brom dengan PBr 3 dan ini bereaksi dengan metilamin. untuk membentuk molekul prekursor yang menutup cincin laktam, untuk membentuk