Les halogénures d'alcanoyle sont obtenus en faisant réagir des acides carboxyliques avec du PBr 3 . SOCl 2 peut également être utilisé.
Ainsi, l'acide éthanoïque est transformé en bromure d'éthanoyle par réaction avec le tribromure de phosphore. L'acide éthanoïque réagit avec le chlorure de thionyle pour former le composé
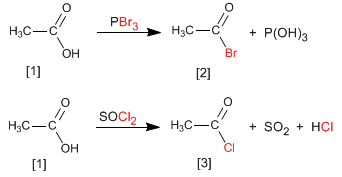
Le mécanisme réactionnel consiste en l'attaque nucléophile de l'acide carboxylique sur le phosphore ou le soufre du réactif, produisant un mécanisme d'addition-élimination qui conduit à l'halogénure d'alcanoyle.
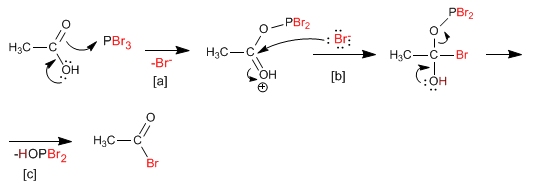
[a] Attaque acide du tribromure de phosphore.
[b] Étape d'addition nucléophile.
[c] Étape d'élimination
Ce mécanisme est répété trois fois, remplaçant tous les bromes du tribromure de phosphore par des groupes hydroxy.
Le chlorure de thionyle a un mécanisme analogue à celui du tribromure de phosphore, convertissant les acides carboxyliques en chlorures d'alcanoyle. Les sous-produits formés dans cette réaction sont le dioxyde de soufre et le chlorure d'hydrogène.
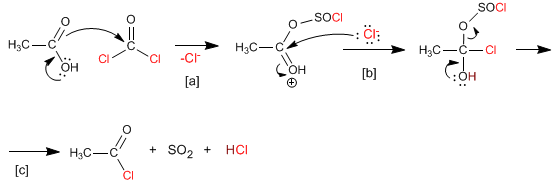
[a] Attaque acide du chlorure de thionyle.
[b] Addition nucléophile
[c] Élimination
