TEORI SISTEM ALLYLIC
- Detail
- Germán Fernández
- TEORI SISTEM ALLYLIC
- Dilihat: 22895
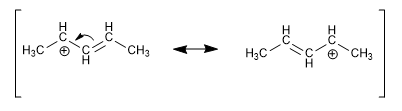
Muatan positif, negatif atau radikal dalam posisi yang dekat dengan ikatan rangkap terdelokalisasi oleh resonansi, menjadi sangat stabil.
- Detail
- Germán Fernández
- TEORI SISTEM ALLYLIC
- Dilihat: 43296
Gugus CH 2 = CHCH 2 - disebut alil. Beberapa senyawa yang berasal dari gugus alil adalah:
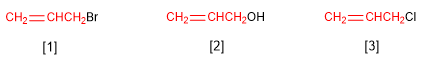
- Detail
- Germán Fernández
- TEORI SISTEM ALLYLIC
- Dilihat: 24873
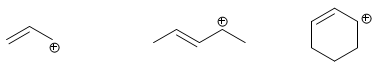
Karbokation yang terbentuk pada karbon yang terletak pada posisi alilik disebut kation alilik.
- Detail
- Germán Fernández
- TEORI SISTEM ALLYLIC
- Dilihat: 16373
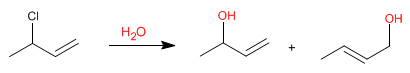
Sistem alilik dapat bertindak sebagai substrat dalam reaksi substitusi nukleofilik. Jadi, reaksi 3-kloro-1-butena dengan air menghasilkan dua alkohol alilik.
- Detail
- Germán Fernández
- TEORI SISTEM ALLYLIC
- Dilihat: 3401
Pembentukan karbokation alilik, yang distabilkan oleh resonansi, memungkinkan reaksi berkembang dalam dua cara yang mengarah pada produk kinetik dan termodinamika.
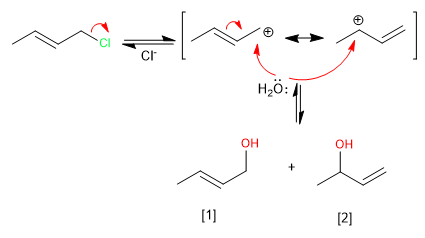
Selengkapnya: Kontrol kinetik dan termodinamika dalam sistem alilik
- Detail
- Germán Fernández
- TEORI SISTEM ALLYLIC
- Dilihat: 2762
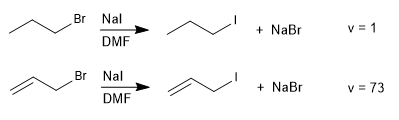
Reaksi S N 2 dengan gugus pergi pada posisi alilik berlangsung lebih cepat daripada reaksi haloalkana jenuh.
- Detail
- Germán Fernández
- TEORI SISTEM ALLYLIC
- Dilihat: 2769
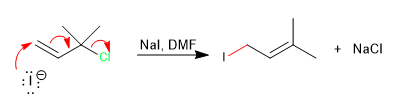
Dengan substrat alilik tersier dan dalam kondisi S N 2 (nukleofil yang baik dan pelarut aprotik), reaksi terpadu dihasilkan oleh nukleofil yang menyerang karbon ikatan rangkap dengan hilangnya gugus lepas.
- Detail
- Germán Fernández
- TEORI SISTEM ALLYLIC
- Dilihat: 2726
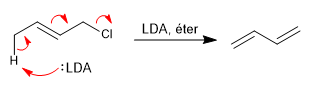
Basa yang kuat dan terhalang sebagian besar memberikan E2 dengan sistem alilik, mendeprotonasi karbon yang terletak di posisi 4 sehubungan dengan gugus pergi.
- Detail
- Germán Fernández
- TEORI SISTEM ALLYLIC
- Dilihat: 3596
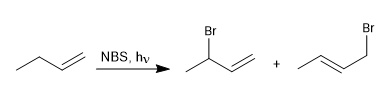
Halogen dapat ditambahkan ke alkena menghasilkan dihaloalkana vicinal, tetapi ketika reaksi ini dilakukan pada konsentrasi halogen rendah, mekanisme radikal lebih disukai. Reagen yang banyak digunakan dalam brominasi alilik adalah NBS (N-bromosuccinimide).
- Detail
- Germán Fernández
- TEORI SISTEM ALLYLIC
- Dilihat: 3014
Diena terkonjugasi menambahkan asam dari halogen membentuk produk kinetik dan termodinamika, yang rasionya dapat dikontrol dengan kondisi reaksi (suhu dan waktu).
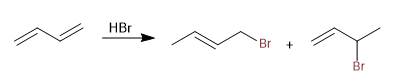
Selengkapnya: Penambahan asam halogen (HX) ke diena terkonjugasi
- Detail
- Germán Fernández
- TEORI SISTEM ALLYLIC
- Dilihat: 3109
Berbeda dengan penambahan bromin ke alkena, diena terkonjugasi tidak membentuk ion halonium karena stabilitas tinggi dari karbokation yang terbentuk.
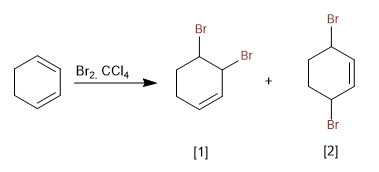
[1 ] Produk penjumlahan 1,2
[2 ] Produk penjumlahan 1.4