La condensazione aciloinica trasforma gli esteri in alfa-idrossichetoni. Questa reazione viene condotta con sodio metallico in un solvente inerte. 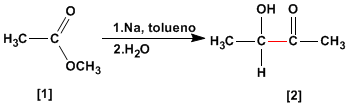
Meccanismo
Nel meccanismo della reazione, il sodio metallico reagisce con l'estere per formare un anione radicale, che dimerizza per formare il dianione. 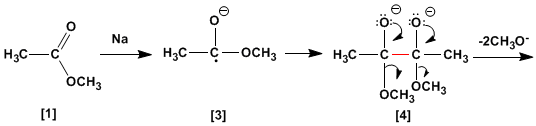
Il dichetone è formato dalla perdita di due equivalenti di metossido. La reazione con due equivalenti di sodio metallico converte il dichetone nell'enodiolato, che genera un enodiolo sulla lavorazione acquosa. 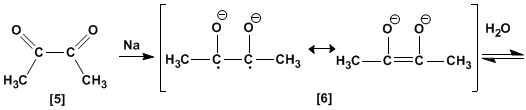
L'ultima fase è l'interconversione tra enolo e chetone, nota come tautomeria cheto-enolica. 
La condensazione dell'aciloina è anche un metodo importante per la preparazione di cicli medi e grandi. 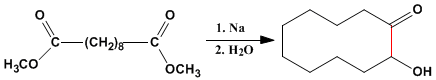
Riferimenti
1. N. Allinger, org. Sintetizzatore. VI:840(1963)
2. J.-P. Sauvage, Acc. Chem. Res. 1990, 23, 319-327.
3. SM McElvain, org. reagire. 1948, 4, 256-268.
4. M.Makosza e k. Grela, Synlett. 1997:267.







