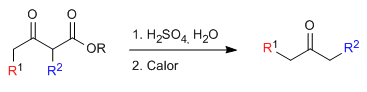
A síntese acetilacética permite a preparação de cetonas por C-alquilação do acetilacetato de etila (3-oxobutanoato de etila). acidez significativa (pKa=11) devido à estabilização da base conjugada nas duas carbonilas vizinhas.
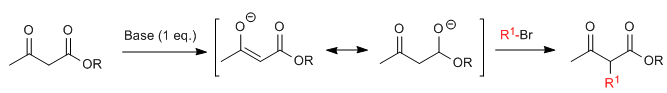
Onde R 1 é um grupo alquil, alil ou benzil primário ou secundário.
O substrato monoalquilado é passível de uma segunda alquilação pela adição de um segundo equivalente de base seguido pelo eletrófilo.
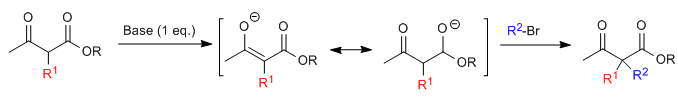
O cetoéster monoalquilado ou dialquilado é então submetido a uma etapa de hidrólise ácida que o transforma em um cetoácido sensível à descarboxilação por aquecimento.
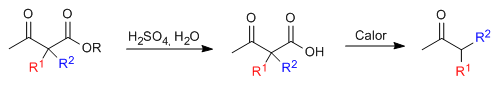
A hidrólise básica é desaconselhável devido à possível competição com retro-Claisen.
Na presença de dois equivalentes de base, os dianions são gerados com capacidade de alugar nas posições C2 e C4.
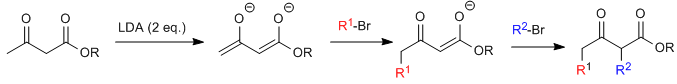
A hidrólise seguida de aquecimento produz cetonas dialquiladas.