TEORI ALDEHIDA DAN KETON
- Detail
- Germán Fernández
- TEORI ALDEHIDA DAN KETON
- Dilihat: 213276
Aldehida diberi nama dengan mengganti akhiran -o dari alkana yang sesuai dengan -al . Tidak perlu menentukan posisi gugus aldehida, karena menempati ujung rantai (locant 1).
Ketika string berisi dua fungsi aldehida, akhiran -dial digunakan.
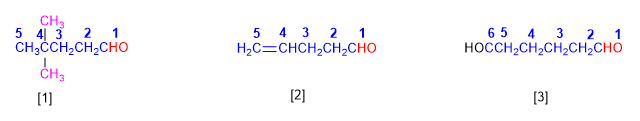
[1] 4,4-Dimetilpentanal
[2] Pent-4-enal
[3] Heksanodial
- Detail
- Germán Fernández
- TEORI ALDEHIDA DAN KETON
- Dilihat: 141233
Aldehida dan keton dapat dibuat dengan oksidasi alkohol, ozonolisis alkena, hidrasi alkuna, dan asilasi Friedel-Crafts sebagai metode utama.
a) Ozonolisis alkena: Alkena terurai dengan ozon untuk membentuk aldehida dan/atau keton. Jika alkena memiliki hidrogen vinil, ia menghasilkan aldehida. Jika memiliki dua rantai karbon, ia membentuk keton. 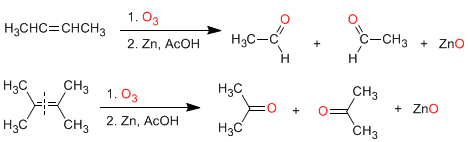
- Detail
- Germán Fernández
- TEORI ALDEHIDA DAN KETON
- Dilihat: 69397
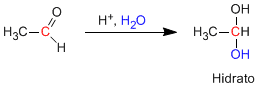
Aldehida dan keton bereaksi dalam media asam berair untuk membentuk hidrat. Mekanismenya terdiri dari tiga tahap. Yang pertama dan tercepat adalah protonasi oksigen karbonil. Protonasi ini menghasilkan peningkatan polaritas pada karbon dan mendukung serangan nukleofil. Pada tahap kedua, air menyerang karbon karbonil, ini adalah tahap mekanisme yang lambat. Pada tahap ketiga, deprotonasi oksigen terjadi, membentuk hidrat akhir.
- Detail
- Germán Fernández
- TEORI ALDEHIDA DAN KETON
- Dilihat: 91429
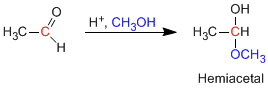
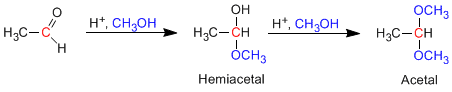
Hemiasetal dibentuk dengan mereaksikan satu ekuivalen alkohol dengan gugus karbonil aldehida atau keton. Reaksi ini dikatalisis asam dan setara dengan pembentukan hidrat.
- Detail
- Germán Fernández
- TEORI ALDEHIDA DAN KETON
- Dilihat: 86339
- Detail
- Germán Fernández
- TEORI ALDEHIDA DAN KETON
- Dilihat: 61829
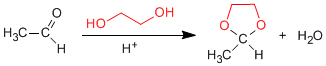
1,2- dan 1,3-diol bereaksi dengan aldehida dan keton membentuk asetal siklik. Kesetimbangan digeser menuju produk akhir dengan menghilangkan air yang dibentuk oleh azeotroping dengan benzena atau toluena.
- Detail
- Germán Fernández
- TEORI ALDEHIDA DAN KETON
- Dilihat: 52324
 Asetal dapat digunakan, karena kestabilannya, sebagai gugus pelindung karbonil. Asetal adalah eter, sangat stabil dalam media dasar, meskipun pecah dengan adanya media asam. Dalam banyak proses sintesis, gugus karbonil tidak sesuai dengan reagen yang digunakan. Dalam kasus ini harus dilindungi untuk mencegahnya bereaksi. Ketidakstabilan asetal dalam media asam dapat digunakan untuk menghilangkan perlindungan karbonil.
Asetal dapat digunakan, karena kestabilannya, sebagai gugus pelindung karbonil. Asetal adalah eter, sangat stabil dalam media dasar, meskipun pecah dengan adanya media asam. Dalam banyak proses sintesis, gugus karbonil tidak sesuai dengan reagen yang digunakan. Dalam kasus ini harus dilindungi untuk mencegahnya bereaksi. Ketidakstabilan asetal dalam media asam dapat digunakan untuk menghilangkan perlindungan karbonil.
Mari kita lihat beberapa contoh:
- Detail
- Germán Fernández
- TEORI ALDEHIDA DAN KETON
- Dilihat: 80271
Reaksi aldehida atau keton dengan amina primer menghasilkan imina . Reaksi disukai dalam media yang sedikit asam (pH = 4,5). 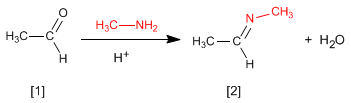
- Detail
- Germán Fernández
- TEORI ALDEHIDA DAN KETON
- Dilihat: 59504
Oksim [3] diperoleh dengan reaksi aldehida atau keton [1] dan hidroksilamin [2] dalam media asam lemah. Mekanismenya analog dengan pembentukan imina. 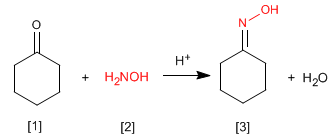
- Detail
- Germán Fernández
- TEORI ALDEHIDA DAN KETON
- Dilihat: 54859
Hidrazon [3] diperoleh dengan mereaksikan aldehida atau keton [1] dengan hidrazin [2] . Seperti halnya imina dan oksim, ini membutuhkan pH=4.
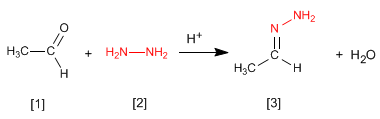
- Detail
- Germán Fernández
- TEORI ALDEHIDA DAN KETON
- Dilihat: 31243
Hidrazin [2] bereaksi dengan dua molekul aldehida [1] membentuk azin [3]. 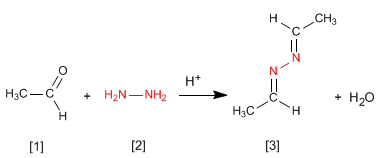
- Detail
- Germán Fernández
- TEORI ALDEHIDA DAN KETON
- Dilihat: 34871
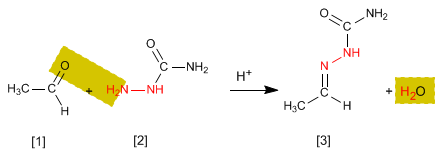
Semikarbazon [3] diperoleh dengan mereaksikan aldehida atau keton [1] dengan semikarbazida [2] . Mari kita lihat contohnya:
- Detail
- Germán Fernández
- TEORI ALDEHIDA DAN KETON
- Dilihat: 90003
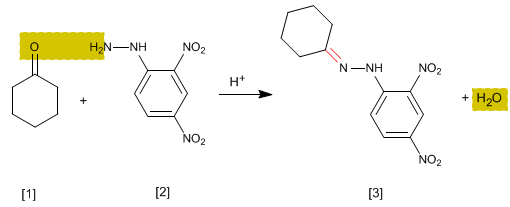
Ini adalah tes analitik khusus untuk aldehida dan keton. Karbonil [1] bereaksi dengan 2,4-Dinitrofenilhidrazin [2] membentuk fenilhidrazon [3] yang mengendap berwarna kuning. Munculnya endapan merupakan indikator adanya karbonil dalam medium.
- Detail
- Germán Fernández
- TEORI ALDEHIDA DAN KETON
- Dilihat: 36433
sintesis enamina
Seperti yang kita lihat di bagian sebelumnya, kondensasi amina primer dengan aldehida dan keton menghasilkan imina. Pada bagian ini kita akan mempelajari kondensasi karbonil dengan amina sekunder yang menghasilkan enamina.
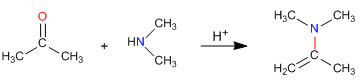
Mekanisme pembentukan enamel
Setelah serangan awal amina sekunder pada karbonil, air dihilangkan, membentuk ikatan rangkap antara karbon karbonil dan alfa dari karbonil awal.
Langkah 1. Protonasi karbonil
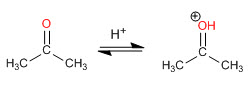
Langkah 2. Serangan nukleofilik amina sekunder
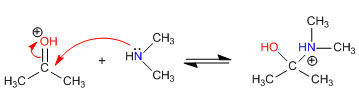
Tahap 3. Keseimbangan asam-basa
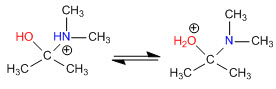
Tahap 4. Kehilangan air
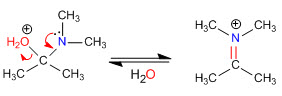
Tahap 5. Eliminasi
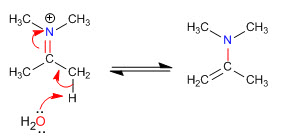
Halangan sterik membuat enamina yang paling tidak tersubstitusi menjadi paling stabil
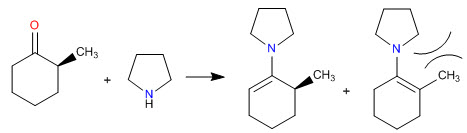
- Detail
- Germán Fernández
- TEORI ALDEHIDA DAN KETON
- Dilihat: 59070
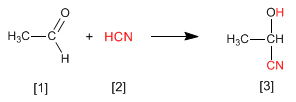
Sianohidrin [3] dibentuk oleh reaksi aldehida atau keton [1] dengan asam hidrosianat [2] dan merupakan senyawa yang mengandung gugus siana dan hidroksi pada karbon yang sama.
- Detail
- Germán Fernández
- TEORI ALDEHIDA DAN KETON
- Dilihat: 65893
Reaksi Wittig menggunakan fosfor ilida [2] untuk mengubah aldehida dan keton [1] menjadi alkena [3] . Trifenilfosfin oksida diperoleh sebagai produk samping [4]. 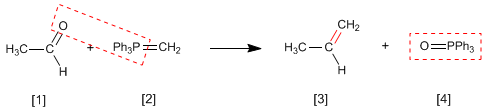
- Detail
- Germán Fernández
- TEORI ALDEHIDA DAN KETON
- Dilihat: 59055
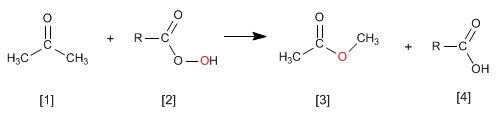
Reaksi keton [1] dengan peracid [2] menghasilkan ester [3] . Oksigen dari peracid disisipkan di antara karbon karbonil dan karbon alfa dari keton. Reaksi ini dijelaskan oleh Adolf von Baeyer dan Victor Villiger pada tahun 1899.