Alkohol adalah spesies amfoter (amfiprotik), mereka dapat bertindak sebagai asam atau basa. Dalam larutan berair, kesetimbangan terbentuk antara alkohol, air dan basa konjugatnya.
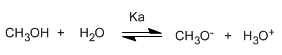
Menulis konstanta kesetimbangan (Ka)
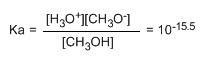
Nilai konstanta yang kecil memberi tahu kita bahwa kesetimbangan sepenuhnya bergeser ke kiri. Logaritma konstanta kesetimbangan yang diubah memberi kita pKa metanol, parameter yang menunjukkan tingkat keasaman senyawa organik.
pKa = - log ka = 15,5
Peningkatan pKa menyiratkan penurunan keasaman. Jadi, metanol dengan pka 15,5 sedikit lebih asam daripada etanol dengan pka 15,9.
pKa alkohol dipengaruhi oleh beberapa faktor seperti ukuran rantai karbon dan gugus elektronegatif.
Dengan meningkatnya panjang rantai karbon, alkohol menjadi kurang asam.
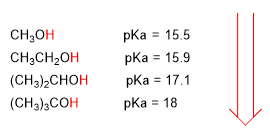
keasaman lebih rendah
Gugus elektronegatif (halogen) meningkatkan keasaman alkohol (menurunkan pKa)
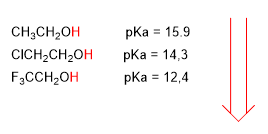
keasaman lebih tinggi