Amina memiliki hidrogen asam pada gugus amino. Hidrogen ini dapat dikurangi menggunakan basa kuat (organologam, hidrida logam) membentuk amida (basa amina).
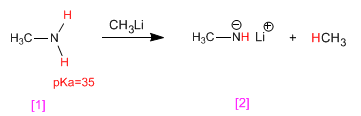
Metilamin [1] bereaksi dengan metillitium, berubah menjadi basa konjugatnya, litium metilamida [2] . Untuk bagiannya, methyllithium diubah menjadi asam konjugatnya, metana.
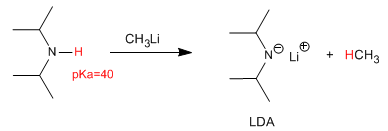
Deprotonasi diisopropilamin menghasilkan salah satu basa yang paling banyak digunakan dalam kimia organik, litium diisopropilamida (LDA).
Namun, perilaku amina yang paling penting adalah basa. Amina adalah zat organik netral yang paling dasar.
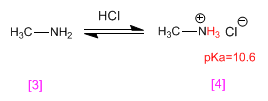
Metilamin [3] terprotonasi menjadi metilamonium klorida (garam amonium) [4] . Garam amonium adalah asam konjugasi amina dan memiliki pKa mulai dari 9 hingga 11.
Kebasaan amina tergantung pada efek induktif dan sterik. Jadi, pKa meningkat dengan panjang rantai karbon (efek induktif).
CH3NH2 pKa = 10,6
CH 3 CH 2 NH 2 pKa = 10,8
(CH 3 ) 3 CNH 2 pKa=10,4
Rantai karbon memberi muatan pada gugus amino, dengan efek induktif, meningkatkan kebasaannya. Basa kuat memiliki asam konjugat yang lemah, sehingga pKa naik. Tetapi jika rantai sangat banyak, efek sterik mulai mendominasi, menyebabkan penurunan pKa.