Die S N 2 (bimolekulare nukleophile Substitution) ist eine konzertierte Reaktion, dh sie erfolgt in einem einzigen Schritt.
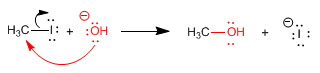
Der Mechanismus besteht darin, dass das Nucleophil den Kohlenstoff angreift, der die Abgangsgruppe enthält. Dieser Kohlenstoff weist aufgrund der Elektronegativität des Halogens eine wichtige positive Polarität auf. Gleichzeitig mit dem Angriff des Nucleophils wird die Kohlenstoff-Halogen-Bindung aufgebrochen, wodurch das Endprodukt erhalten wird.
Der Übergangszustand von S N 2 hat die folgende Form:
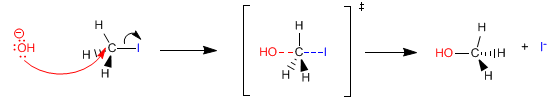
Die Geschwindigkeit einer Elementarreaktion ist proportional zum Produkt der Konzentrationen der Reaktanten, erhöht auf ihre jeweiligen stöchiometrischen Koeffizienten. Die Proportionalitätskonstante heißt kinetische Konstante.
Somit hängt die Geschwindigkeit von S N 2 von der Konzentration des Substrats (CH 3 I) und des Nukleophils (OH - ) ab und ist daher eine bimolekulare Reaktion.
v=k[CH 3 I][OH – ]