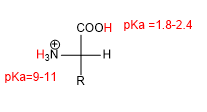
 Das Vorhandensein von sauren (-COOH) und basischen (-NH 2 ) Gruppen verleiht Aminosäuren charakteristische Säure-Base-Eigenschaften.
Das Vorhandensein von sauren (-COOH) und basischen (-NH 2 ) Gruppen verleiht Aminosäuren charakteristische Säure-Base-Eigenschaften.
In stark sauren Medien sind sowohl die Aminogruppe als auch die Säuregruppe protoniert und die Aminosäure hat die folgende Form:
Wenn der pH-Wert ansteigt, wird die saurere Gruppe, H mit einem niedrigeren pKa, deprotoniert und bildet eine neutrale Spezies namens Zwitterion.
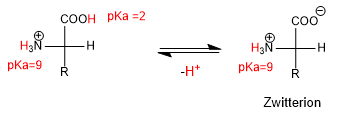
Wenn sich die Aminosäure in basischen Medien befindet, verliert sie das Proton der Aminogruppe, wodurch die deprotonierte Spezies entsteht.
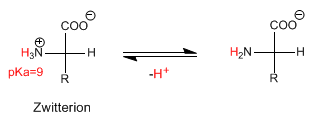
Der pH-Wert, bei dem die Zwitterionenkonzentration maximal ist (die Aminosäure hat keine Nettoladung), wird als isoelektrischer pH-Wert oder isoelektrischer Punkt bezeichnet.
Eine andere Definition des isoelektrischen Punkts ist: pH-Wert, bei dem sich die Konzentration von protonierten und deprotonierten Spezies ausgleicht.
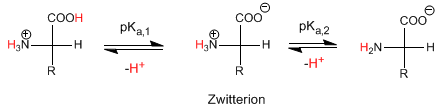
Der isoelektrische pH-Wert wird als Durchschnitt von pK a,1 und pK a,2 berechnet, d. h. als Durchschnitt der pKas der Stufen, die das Zwitterion bilden und zersetzen.