Bimolekulare (E2) Eliminierungen finden schneller statt, wenn sich die Abgangsgruppe auf der gegenüberliegenden Seite des entfernten Wasserstoffs befindet. Diese räumliche Anordnung ist als "ANTI" bekannt.
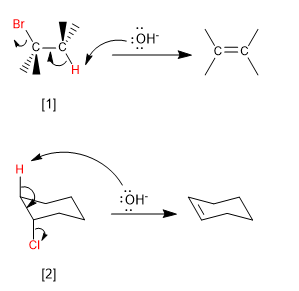
[1] H und Br in "ANTI"
[2 ] H und Cl in "ANTI"
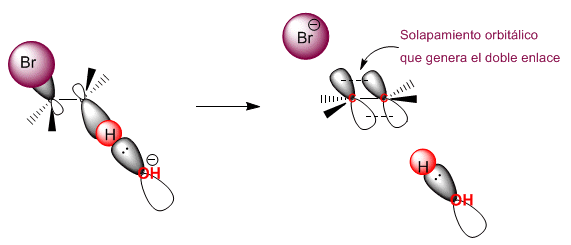
Die "ANTI"-Deletion wird bevorzugt, da sie die Überlappung zwischen den beiden entstehenden p-Orbitalen maximiert, was zu einer pi-Bindungsbildung führt.
Im folgenden Beispiel haben die beiden b- Kohlenstoffe Wasserstoffatome, die Base entfernt jedoch hauptsächlich den Wasserstoff, der in Bezug auf Chlor ANTI ist (roter Wasserstoff).
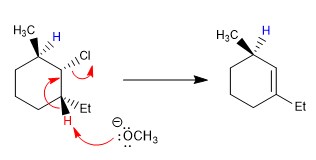
H Wasserstoff ANTI gegenüber Chlor
H Wasserstoff SYN in Bezug auf Chlor.