BENZOL-THEORIE
- Details
- Germán Fernández
- BENZOL-THEORIE
- Zugriffe: 152372
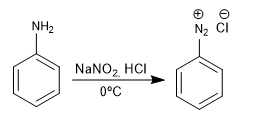
Monosubstituierte Benzole werden benannt, indem der Name des Substituenten in Benzol endet.
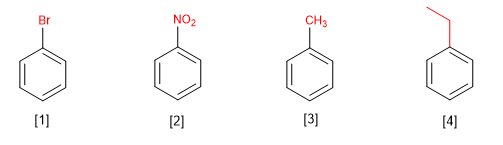
[1] Brombenzol
[2] Nitrobenzol
[3] Methylbenzol (Toluol)
[4] Ethylbenzol
- Details
- Germán Fernández
- BENZOL-THEORIE
- Zugriffe: 88159
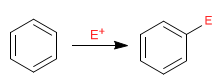
Benzol wirkt als Nucleophil und greift eine große und vielfältige Anzahl von Elektrophilen an.
- Details
- Germán Fernández
- BENZOL-THEORIE
- Zugriffe: 126894
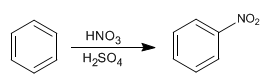
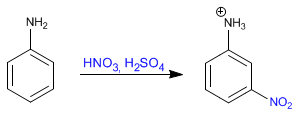
Das Benzol reagiert mit dem Stickstoff-Schwefel-Gemisch unter Anlagerung von Nitrogruppen.
- Details
- Germán Fernández
- BENZOL-THEORIE
- Zugriffe: 117864
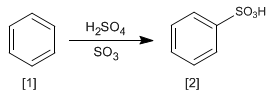
Die Reaktion von Benzol [1] mit einer Lösung von Schwefeltrioxid in Schwefelsäure ergibt Benzolsulfonsäuren [2].
- Details
- Germán Fernández
- BENZOL-THEORIE
- Zugriffe: 102850
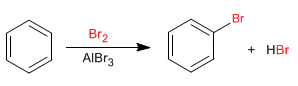
Benzol reagiert mit Halogenen in Gegenwart von Lewis-Säuren unter Bildung von halogenierten Derivaten.
- Details
- Germán Fernández
- BENZOL-THEORIE
- Zugriffe: 74399
Weiterlesen: Benzol - Schutz und Entschützung der Aminogruppe
- Details
- Germán Fernández
- BENZOL-THEORIE
- Zugriffe: 5606
Die Aminogruppe wird durch Reduktion des Nitros in den aromatischen Ring eingeführt.
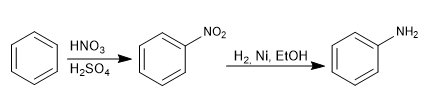
Die bei der Reduktion verwendeten Reagenzien können sein:
- Sn, HCl
- H2 , Ni, EtOH
- Fe, HCl
Weiterlesen: Reduktion von Nitro zu Amino und Oxidation von Amino zu Nitro
- Details
- Germán Fernández
- BENZOL-THEORIE
- Zugriffe: 2374
Die Reversibilität der Sulfonierung ermöglicht ihre Verwendung zum Schutz aktivierter Positionen von Benzol. Sehen wir uns ein Beispiel an:
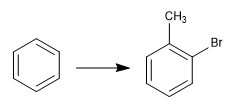
Um o-Bromtoluol zu erhalten, führen wir die folgenden Schritte durch:
- Details
- Germán Fernández
- BENZOL-THEORIE
- Zugriffe: 3394
Die Reaktion von 1-Chlor-2,4-dinitrobenzol mit Nucleophilen (Hydroxid, Ammoniak, Methoxid usw.) führt zur Substitution von Chlor durch das entsprechende Nucleophil. Es wird ipso (gleicher Ort) genannt, um anzuzeigen, dass das Nucleophil die gleiche Position wie das Ausgangschlor einnimmt.
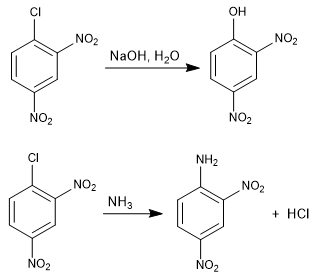
Weiterlesen: Aromatische nukleophile Substitution durch Additions-Eliminierung
- Details
- Germán Fernández
- BENZOL-THEORIE
- Zugriffe: 55288
Halogenierte Benzole reagieren mit verdünnter Soda unter hohen Druck- und Temperaturbedingungen zu Phenolen. Diese Reaktion erfordert keine desaktivierenden Gruppen in der ortho/para-Position und folgt einem anderen Mechanismus als die aromatische nucleophile Substitution durch Additions-Eliminierung.
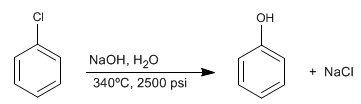
- Details
- Germán Fernández
- BENZOL-THEORIE
- Zugriffe: 3901
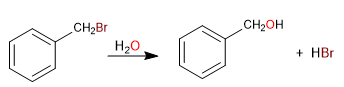
Der direkt an Benzol gebundene Kohlenstoff ist als Benzylposition bekannt. In dieser Position werden aufgrund der Möglichkeit der Delokalisierung der Ladung am aromatischen Ring hochstabile Carbokationen, Carbanionen und Radikale gebildet.
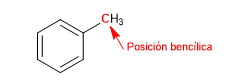
S N 1 in Benzylpositionen
- Details
- Germán Fernández
- BENZOL-THEORIE
- Zugriffe: 3279
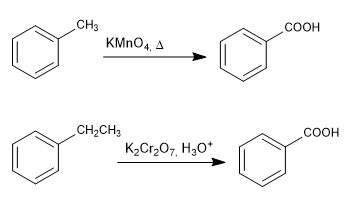
Kettenoxidation mit Permanganat und Dichromat
- Details
- Germán Fernández
- BENZOL-THEORIE
- Zugriffe: 3206
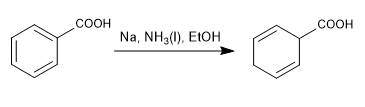
Die Birch-Reduktion verwendet Natrium oder Lithium in Lösung als Reagenzien, ihr Mechanismus ist radikal und reduziert Benzol zu 1,4-Cyclohexadien.
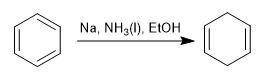
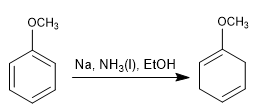
Birke mit aktivierenden Substituenten
- Details
- Germán Fernández
- BENZOL-THEORIE
- Zugriffe: 2407
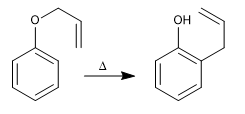
Allylphenylether gehen beim Erhitzen eine konzertierte Reaktion ein, bei der sechs Elektronen bewegt werden, die als Claisen-Umlagerung bezeichnet wird. Das bei der Reaktion gebildete Zwischenprodukt ist energiereich und tautomerisiert schnell zum Endprodukt.
- Details
- Germán Fernández
- BENZOL-THEORIE
- Zugriffe: 3112
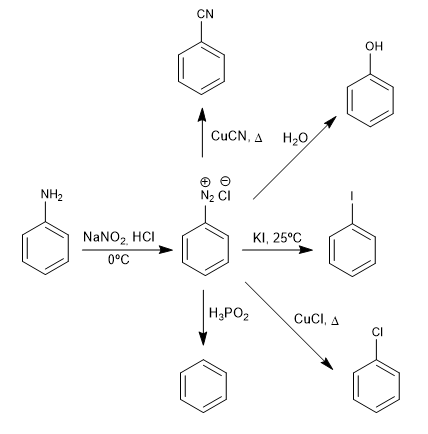
Die Benzoldiazoniumsalze werden von Nucleophilen in Gegenwart von Kupfer(I)-Salzen, die als Katalysator wirken, angegriffen, wobei eine Vielzahl von Produkten erhalten wird.
- Details
- Germán Fernández
- BENZOL-THEORIE
- Zugriffe: 3270
Bildung von Azoverbindungen