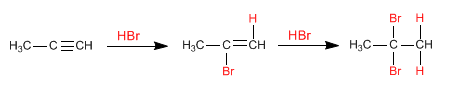
Ähnlich wie Alkene addieren Alkine Halogenwasserstoffe (HBr, HCl, HI) an die Dreifachbindung, um Alkenylhalogenide zu bilden.
Der Reaktionsmechanismus erfolgt über ein Carbokation, das am am stärksten substituierten Kohlenstoff der Dreifachbindung gebildet wird. Daher ist es eine regioselektive Reaktion, die der Markovnikov-Regel folgt und das Halogen an den am stärksten substituierten Kohlenstoff des Alkins addiert.
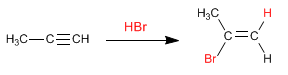
Stufe 1. Elektrophile Addition. Das Proton fügt sich an die Dreifachbindung an und verbindet den am wenigsten substituierten Kohlenstoff.
Stufe 2. Das Halogen fängt das im vorherigen Schritt gebildete Carbokation ein.
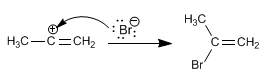
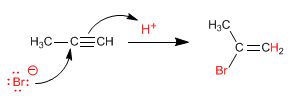
Angesichts der großen Instabilität des gebildeten Carbokations (Alkenylkation) wird der bisherige Mechanismus in Frage gestellt. Ein weiterer alternativer Mechanismus ist der konzertierte (einstufiger Mechanismus ohne Bildung von Zwischenprodukten).
In Gegenwart von zwei Äquivalenten des Halogenwasserstoffs treten aufeinanderfolgende Additionen an das Alkin auf, wobei geminale Dihalogenalkane gebildet werden.