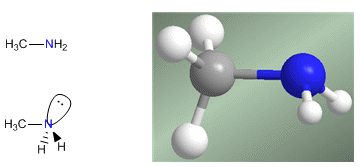
Amine sind stickstoffhaltige Verbindungen mit pyramidenförmiger Struktur, ähnlich wie Ammoniak. Stickstoff bildet über sp 3 -hybridisierte Orbitale drei Einfachbindungen. Das freie Elektronenpaar besetzt das vierte Orbital mit sp 3 -Hybridisierung und ist für das basische und nukleophile Verhalten von Aminen verantwortlich.
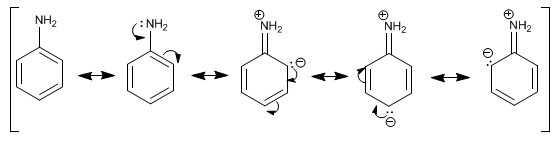
Bei aromatischen Aminen wie Anilin ist das bemerkenswerteste Merkmal die Delokalisierung des freien Elektronenpaars am aromatischen Ring. Diese Delokalisierung führt zu einer Erhöhung der elektronischen Dichte der Phenylgruppe, wodurch die Reaktivität von Anilin bei elektrophilen Substitutionsreaktionen erhöht wird.