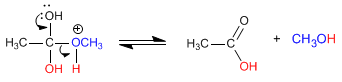Die Ester werden in wässrigen Medien unter Säure- oder Basenkatalyse zu Carbonsäuren und Alkoholen hydrolysiert.
In sauren Medien kann die Hydrolyse von Estern durch die folgende chemische Gleichung geschrieben werden:
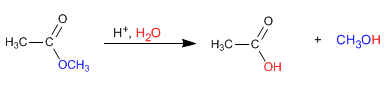
Der Mechanismus der Säurehydrolyse erfolgt in den folgenden Stufen:
Stufe 1. Protonierung des Esters
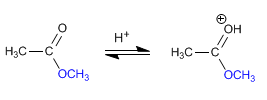
Stufe 2. Nucleophile Addition von Wasser an das Carbonyl
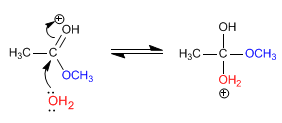
Stufe 3. Säure-Basen-Gleichgewicht, das das Methoxid in eine gute Abgangsgruppe (Methanol) umwandelt.
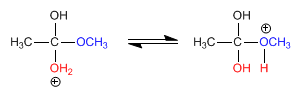
Stufe 4. Eliminierung von Methanol