Амины имеют кислые атомы водорода в аминогруппе. Эти атомы водорода можно вычесть с помощью сильных оснований (металлоорганических, гидридов металлов), образующих амиды (аминные основания).
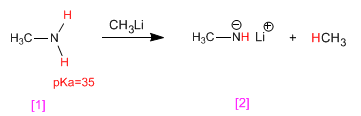
Метиламин [1] реагирует с метиллитием, превращаясь в его сопряженное основание – метиламид лития [2] . Со своей стороны, метиллитий превращается в сопряженную кислоту метан.
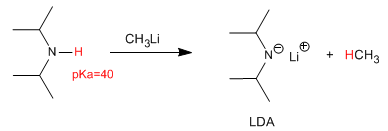
Депротонирование диизопропиламина дает одно из наиболее широко используемых в органической химии оснований — диизопропиламид лития (LDA).
Однако наиболее важным поведением аминов является основное. Амины — самые основные нейтральные органические вещества.
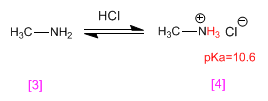
Метиламин [3] протонируется, превращаясь в хлорид метиламмония (соль аммония) [4] . Соли аммония представляют собой сопряженные кислоты аминов и имеют pKas в диапазоне от 9 до 11.
Основность аминов зависит от индуктивных и стерических эффектов. Таким образом, pKa увеличивается с увеличением длины углеродной цепи (индуктивный эффект).
CH3NH2 рКа = 10,6
CH 3 CH 2 NH 2 pKa=10,8
(CH 3 ) 3 CNH 2 pKa=10,4
Углеродная цепь дает заряд аминогруппе за счет индукционного эффекта, увеличивая ее основность. Сильное основание имеет слабую сопряженную кислоту, поэтому pKa увеличивается. Но если цепь очень объемная, начинают преобладать стерические эффекты, вызывающие снижение рКа.