ТЕОРИЯ БЕНЗОЛА
- Информация о материале
- Germán Fernández
- ТЕОРИЯ БЕНЗОЛА
- Просмотров: 151465
Монозамещенные бензолы называются по окончанию названия заместителя в бензоле.
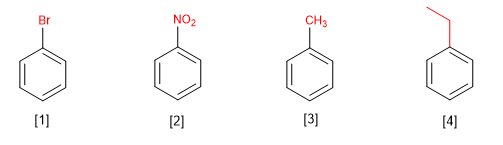
[1] Бромбензол
[2] Нитробензол
[3] Метилбензол (толуол)
[4] Этилбензол
- Информация о материале
- Germán Fernández
- ТЕОРИЯ БЕНЗОЛА
- Просмотров: 87203
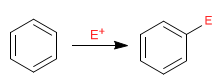
Бензол действует как нуклеофил, атакуя большое и разнообразное количество электрофилов.
- Информация о материале
- Germán Fernández
- ТЕОРИЯ БЕНЗОЛА
- Просмотров: 127215
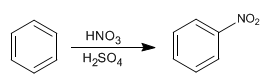
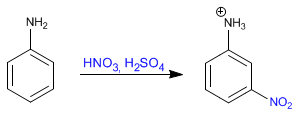
Бензол реагирует с азотно-серной смесью с присоединением нитрогрупп.
- Информация о материале
- Germán Fernández
- ТЕОРИЯ БЕНЗОЛА
- Просмотров: 123235
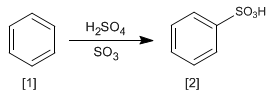
Реакцией бензола [1] с раствором триоксида серы в серной кислоте образуются бензолсульфокислоты [2].
- Информация о материале
- Germán Fernández
- ТЕОРИЯ БЕНЗОЛА
- Просмотров: 106212
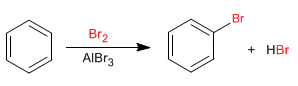
Бензол реагирует с галогенами в присутствии кислот Льюиса с образованием галогенпроизводных.
- Информация о материале
- Germán Fernández
- ТЕОРИЯ БЕНЗОЛА
- Просмотров: 74559
- Информация о материале
- Germán Fernández
- ТЕОРИЯ БЕНЗОЛА
- Просмотров: 4641
Аминогруппа вводится в ароматическое кольцо путем восстановления нитрогруппы.
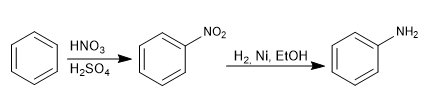
Реагенты, используемые при восстановлении, могут быть:
- Sn, HCl
- Н2 , никель, этанол
- Fe, HCl
Подробнее: Восстановление нитро до амино и окисление амино до нитро
- Информация о материале
- Germán Fernández
- ТЕОРИЯ БЕНЗОЛА
- Просмотров: 2812
Обратимость сульфирования позволяет использовать его для защиты активированных положений бензола. Давайте посмотрим пример:
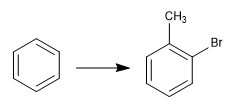
Для получения о-бромтолуола выполняем следующие действия:
- Информация о материале
- Germán Fernández
- ТЕОРИЯ БЕНЗОЛА
- Просмотров: 3074
Реакция 1-хлор-2,4-динитробензола с нуклеофилами (гидроксидом, аммиаком, метоксидом и др.) приводит к замещению хлора соответствующим нуклеофилом. Это называется ipso (на том же месте), чтобы указать, что нуклеофил занимает то же положение, что и исходный хлор.
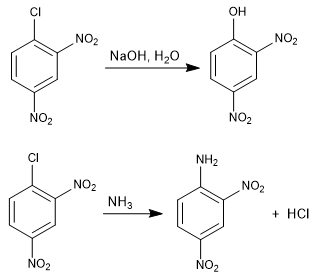
Подробнее: Ароматическое нуклеофильное замещение путем присоединения-отщепления
- Информация о материале
- Germán Fernández
- ТЕОРИЯ БЕНЗОЛА
- Просмотров: 55322
Галогенированные бензолы реагируют с разбавленной содой в условиях высокого давления и температуры с образованием фенолов. Эта реакция не требует дезактивации групп в орто/пара-положении и следует механизму, отличному от механизма ароматического нуклеофильного замещения путем присоединения-отщепления.
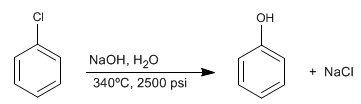
- Информация о материале
- Germán Fernández
- ТЕОРИЯ БЕНЗОЛА
- Просмотров: 3172
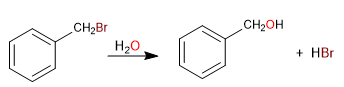
Углерод, присоединенный непосредственно к бензолу, известен как бензильное положение. В этом положении образуются высокостабильные карбокатионы, карбанионы и радикалы за счет возможности делокализации заряда на ароматическом кольце.
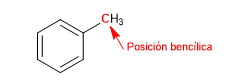
S N 1 в бензильных положениях
- Информация о материале
- Germán Fernández
- ТЕОРИЯ БЕНЗОЛА
- Просмотров: 3121
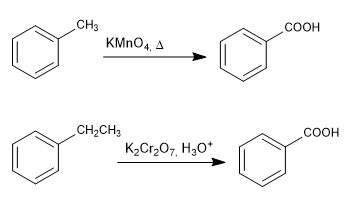
Цепное окисление перманганатом и бихроматом
- Информация о материале
- Germán Fernández
- ТЕОРИЯ БЕНЗОЛА
- Просмотров: 2796
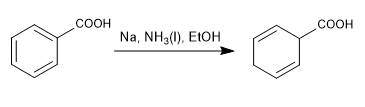
При восстановлении Берча в качестве реагентов используются натрий или литий в растворе, его механизм является радикальным и восстанавливает бензол до 1,4-циклогексадиена.
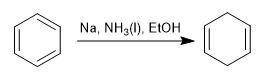
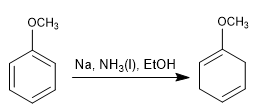
Береза с активирующими заместителями
- Информация о материале
- Germán Fernández
- ТЕОРИЯ БЕНЗОЛА
- Просмотров: 2949
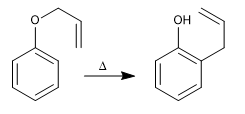
Аллилфениловые эфиры при нагревании вступают в согласованную реакцию, включающую движение шести электронов, называемую перегруппировкой Кляйзена. Промежуточное соединение, образующееся в реакции, обладает высокой энергией и быстро таутомеризуется с образованием конечного продукта.
- Информация о материале
- Germán Fernández
- ТЕОРИЯ БЕНЗОЛА
- Просмотров: 3312
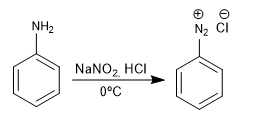
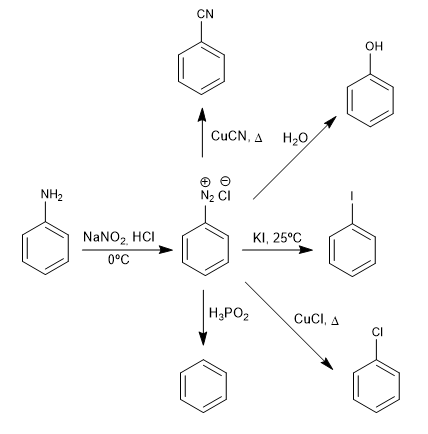
Соли бензолдиазония атакуют нуклеофилы в присутствии солей меди (I), которые действуют как катализатор, с получением широкого спектра продуктов.
- Информация о материале
- Germán Fernández
- ТЕОРИЯ БЕНЗОЛА
- Просмотров: 3284
Образование азосоединений