Пиррол имеет кислый водород при атоме азота с pKa = 17. В случае тиофена и фурана кислые водороды находятся в положении 2, хотя они имеют гораздо более низкую кислотность, чем пиррол.
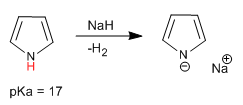
Анион пирролия, образованный депротонированием пиррола, имеет важный ионный характер, который позволяет ему действовать как нуклеофил против разнообразной группы углеродных электрофилов.
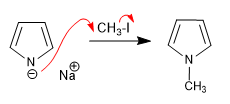
Алкилирование катиона пирролия.
Ацилирование катиона пирролия
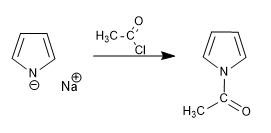
Ионный характер иона пирролия связан с основанием, которое его породило. Таким образом, основания натрия и калия (амиды или гидриды натрия и калия) генерируют ионные пирролы. Однако металлорганические соединения лития и магния или амиды лития производят пирролы с важным ковалентным характером, которые удерживают пару азота заблокированной, вызывая нуклеофильную атаку через кольцо.
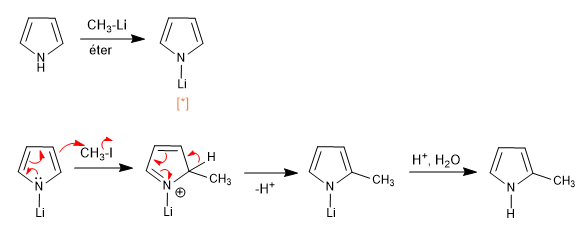
[*] Пирролиды лития или магния имеют важный ковалентный характер, который блокирует пару азота, вызывая атаку электрофила через кольцо.
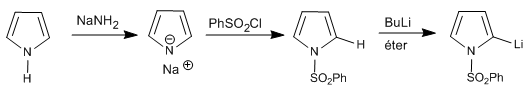
В тиофене и фуране отсутствуют атомы водорода на гетероатоме, но мы можем вычесть атомы водорода из положений 2,5, используя сильные основания (металлоорганические соединения).
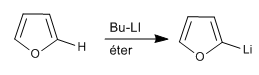
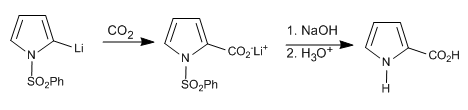
Реакция органолита с различными электрофилами позволяет добавлять цепи в положение 2.
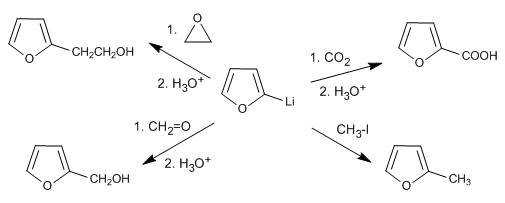
Также возможно депротонировать положение 2 пиррола, если в азоте нет водорода.
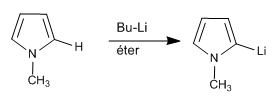
В случае 1H-пирролов можно выполнить следующие шаги для депротонирования положения 2.