СЕРА, ФОСФОР И КРЕМНИЙ
- Информация о материале
- Germán Fernández
- СЕРА, ФОСФОР И КРЕМНИЙ
- Просмотров: 3484
Тиолы характеризуются содержанием функциональной группы -SH. Они названы окончанием названия основной цепи на -тиол, аналогично спиртам, оканчивающимся на -ол.
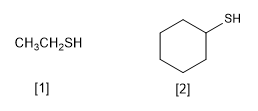
[1] Этанотиол
[2] Циклогексантиол
Тиолы имеют более высокую кислотность, чем спирты, из-за большего размера серы по сравнению с кислородом. Значения pKa составляют около 10-11 по сравнению со спиртами, которые имеют значения между 16-18.
- Информация о материале
- Germán Fernández
- СЕРА, ФОСФОР И КРЕМНИЙ
- Просмотров: 4183
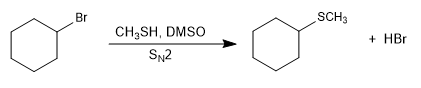
Это соединения, подобные эфирам, в которых кислород заменен серой (RSR). Их также называют сульфидами.
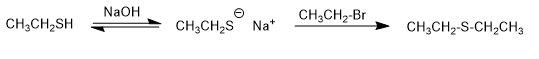
- Информация о материале
- Germán Fernández
- СЕРА, ФОСФОР И КРЕМНИЙ
- Просмотров: 2369
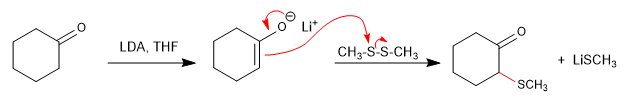
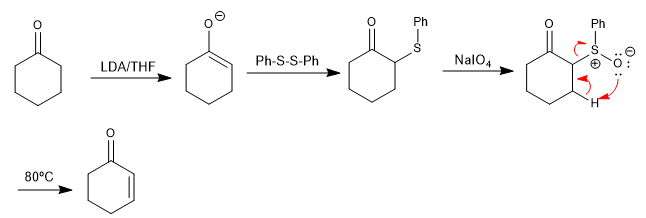
Сульфоксиды вступают в реакции отщепления при небольшом нагревании с образованием алкенов. Сульфоксид можно легко получить путем окисления тиоэфира, который легко образуется в альфа-положении карбонила из дисульфида. Эта процедура позволяет получать α,β-ненасыщенные карбонилы.
- Информация о материале
- Germán Fernández
- СЕРА, ФОСФОР И КРЕМНИЙ
- Просмотров: 3547
Илиды серы получают из тиоэфиров алкилированием с последующим депротонированием.
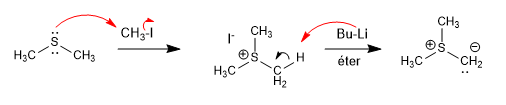
[1] Илид серы
- Информация о материале
- Germán Fernández
- СЕРА, ФОСФОР И КРЕМНИЙ
- Просмотров: 3662
Реакция карбонилов с тиолами приводит к образованию тиоацеталей, которые можно использовать в качестве защитных групп или для восстановления карбонила до алкана.
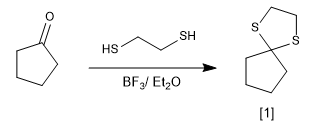
[1] Тиоацеталь
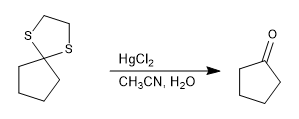
Тиоацеталь устойчив в кислых средах, но может гидролизоваться солями ртути(II).
- Информация о материале
- Germán Fernández
- СЕРА, ФОСФОР И КРЕМНИЙ
- Просмотров: 3216
1,3-дитианы позволяют изменять полярность карбонильного углерода альдегидов за счет вычитания кислого водорода, получая органолит, способный атаковать широкий спектр электрофилов.
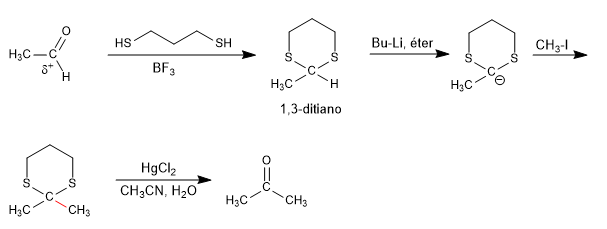
Исходный карбонил с положительной полярностью на углероде превращается в реакции умполунга в карбоанион. Сера 1,3-дитиана жизненно важна для стабилизации отрицательного заряда, и реакция с кислородсодержащим эквивалентом нежизнеспособна.
- Информация о материале
- Germán Fernández
- СЕРА, ФОСФОР И КРЕМНИЙ
- Просмотров: 3627
Фосфины получают взаимодействием треххлористого фосфора с металлоорганическими реагентами. Так, трихлорид фосфора реагирует с бромистым фенилмагнием с образованием трифенилфосфина.
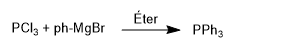
Эта реакция хорошо контролируется и позволяет вводить только две группы.