Следующие модели показывают структуру, расстояния и валентные углы этилена. Каждый атом углерода в молекуле находится в $sp^2$-гибридизации. Его геометрия плоская, с валентными углами, близкими к 120º.
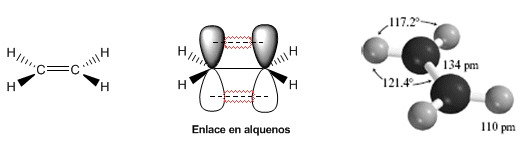
Двойная связь образована $\sigma$-связью, образованной перекрыванием гибридных $sp^2$-орбиталей, и $\pi$-связью, образованной перекрытием p-орбиталей, не подвергшихся гибридизации (чистые p-орбитали ).
Двойная связь прочнее и короче одинарной. Энергия двойной связи в этилене составляет 605 кДж/моль по сравнению с 368 кДж/моль одинарной связи углерод-углерод в этане.