Алканы представляют собой sp 3- гибридные соединения по всем атомам углерода. Четыре заместителя, которые начинаются от каждого атома углерода, расположены по направлению к вершинам тетраэдра.
Расстояния и углы связи показаны на следующих моделях. 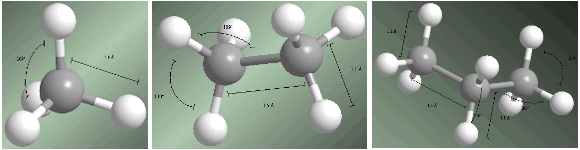
Меньшие алканы, метан, этан, пропан и бутан, являются газами при комнатной температуре. Линейные алканы от C 5 H 12 до C 17 H 36 являются жидкостями. алканы из  большее количество атомов углерода находится в твердом состоянии при комнатной температуре.
большее количество атомов углерода находится в твердом состоянии при комнатной температуре.
Температуры плавления и кипения алканов увеличиваются с увеличением количества атомов углерода в молекуле. Также замечено, что разветвленные алканы имеют более низкую температуру кипения, чем их линейные изомеры.
На следующем графике показаны температуры кипения линейных алканов (черным цветом) и соответствующих их изомеров 2-метилалканов (синим цветом). 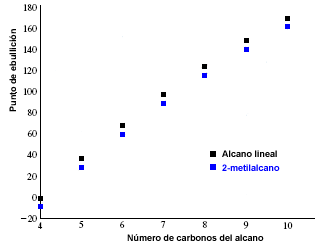
В жидкой фазе между молекулами действуют силы притяжения, удерживающие их вместе. Для перехода вещества в газовую фазу необходимо преодолеть эти межмолекулярные силы за счет подвода энергии. 
В нейтральных молекулах, таких как алканы, силы притяжения обусловлены ван-дер-ваальсовыми взаимодействиями, которые могут быть трех типов: диполь-дипольные, диполь-индуцированные дипольные и индуцированные диполь-индуцированные дипольные взаимодействия.
Формирование индуцированных диполей, создающих притяжение между нейтральными молекулами, можно увидеть на следующей схеме: 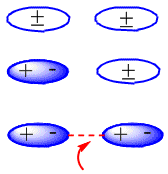
Рассмотрим изомеры пентана как пример понижения температуры кипения при переходе от линейных алканов к разветвленным.
Пентан имеет большую площадь поверхности, которая допускает большое количество индуцированных диполь-индуцированных дипольных взаимодействий. 2-Метилбутан более компактен и имеет меньшую площадь поверхности, меньше межмолекулярных взаимодействий и более низкую температуру кипения.