Спирты являются амфотерными (амфипротонными) видами, они могут действовать как кислоты или основания. В водном растворе устанавливается равновесие между спиртом, водой и сопряженными с ними основаниями.
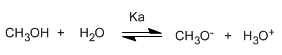
Запись константы равновесия (Ka)
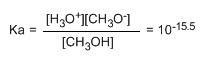
Малое значение константы говорит нам о том, что равновесие полностью смещено влево. Измененный логарифм константы равновесия дает нам pKa метанола, параметр, который показывает степень кислотности органического соединения.
рКа = - log ка = 15,5
Увеличение pKa означает снижение кислотности. Таким образом, метанол с pka 15,5 немного более кислый, чем этанол с pka 15,9.
На pKa спиртов влияют некоторые факторы, такие как размер углеродной цепи и электроотрицательные группы.
По мере увеличения длины углеродной цепи спирт становится менее кислым.
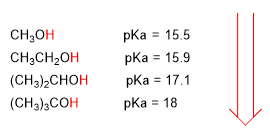
пониженная кислотность
Электроотрицательные группы (галогены) повышают кислотность спиртов (снижают рКа)
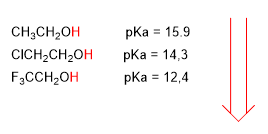
более высокая кислотность









