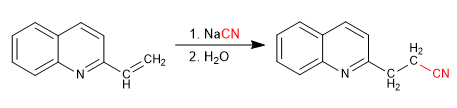
Les pyridines avec des groupes alkyle en position 2,4 ont des hydrogènes acides sur le carbone adjacent au cycle pyridine.
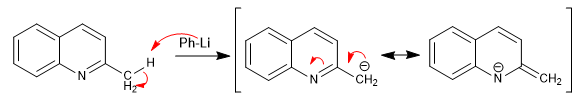
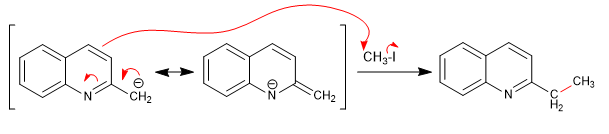
Les hydrogènes peuvent être soustraits à l'aide de bases fortes. La base formée est un bon nucléophile et permet l'attaque de divers électrophiles carbonés.
L'isoquinoléine a des hydrogènes acides en position 1.
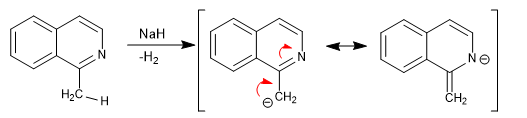
La délocalisation de la charge vers l'atome d'azote est la clé pour que l'hydrogène présente de l'acidité. Les hydrogènes en position 3 (dans l'isoquinoléine) sont beaucoup moins acides car une telle délocalisation provoque la rupture de l'aromaticité dans le carbocycle.
Les quinoléines avec des groupes 2,4-vinyle ou les isoquinolines avec des groupes 1-vinyle sont attaquées par des nucléophiles sur la double liaison vinyle.