La synthèse de Friedländer prépare des quinoléines à partir d'un nitrobenzène ortho-acétylé et d'une cétone. La synthèse débute par une condensation aldolique en milieu basique. La réduction du groupe nitro en amino permet la cyclisation par formation d'imine.
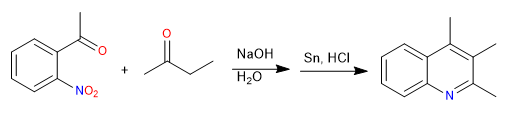
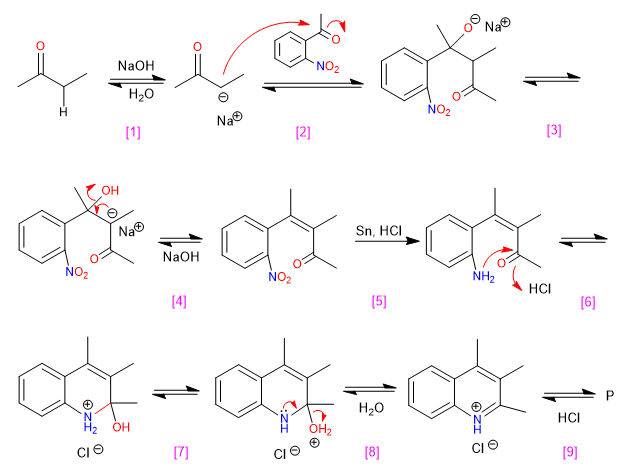
Mécanisme:
Cette synthèse peut également être réalisée par réaction directe de l'o-aminoacétophénone et d'un carbonyle énolisable en milieu basique.
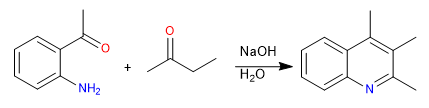
Le mécanisme peut se produire de deux manières :
1. Formation de l'imine, tautomérie en énamine et attaque du carbonyle
2. Condensation aldol et formation ultérieure de l'imine.