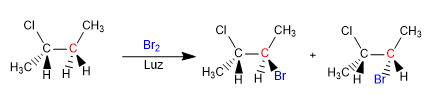
Wir werden sehen, wie chemische Reaktionen Chiralität in Moleküle einführen können, wobei Produkte in Form von racemischen Mischungen oder Mischungen von Diastereoisomeren erhalten werden.
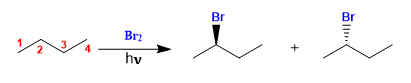
Butan wird in Gegenwart von Brom und Licht an Kohlenstoff 2 halogeniert, um ein Enantiomerengemisch zu bilden. Das gebildete Radikal weist enantiotope Seiten auf, die mit gleicher Wahrscheinlichkeit halogeniert werden, wodurch ein racemisches Gemisch entsteht (Enantiomere in gleichen Anteilen).
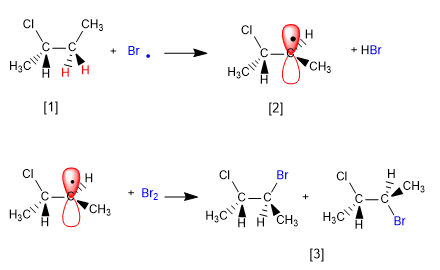
Der Mechanismus dieser Reaktion besteht aus drei Stufen: Initiierung, Ausbreitung und Beendigung. Die Vermehrung ist der Schritt, der die Stereochemie des Endprodukts bestimmt.
Butanhalogenierung
Stufe 1. Einweihung
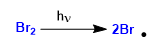
Stufe 2. Ausbreitung
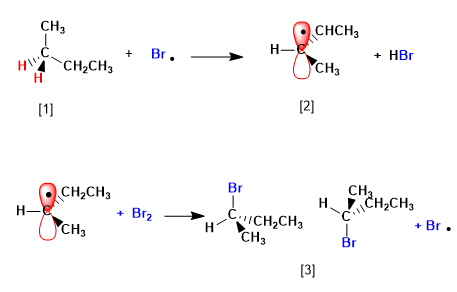
[1] H (Enantiotopen Wasserstoffe)
[2] Radikal mit enantiotopen Flächen
[3] Enantiomerenpaar
Das Produkt wird aufgrund der Bildung eines planaren Radikals, das auf beiden Seiten halogeniert ist, als racemisches Gemisch erhalten. Die enantiotopischen Wasserstoffatome sind chemisch äquivalent und werden mit der gleichen Rate durch Brom subtrahiert.