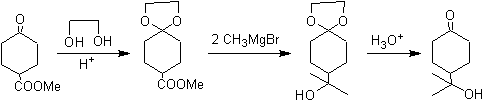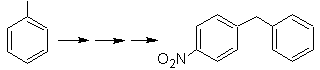SINTESIS ORGANIK
SINTESIS ORGANIK
- Detail
- Wilbertrivera
- SINTESIS ORGANIK
- Dilihat: 45294
METODOLOGI SINTESIS ORGANIK
Sintesis total suatu senyawa organik harus dimulai setiap saat dari unsur-unsur penyusunnya. Namun, diketahui bahwa senyawa organik sederhana seperti urea, metana, metanol, asetilena, asam asetat, etanol dapat diperoleh dari unsur-unsurnya, dan seterusnya, struktur yang semakin kompleks dapat dibangun.
Namun, ini tidak praktis dan tidak perlu karena ada sejumlah besar senyawa organik yang tersedia secara komersial atau tersedia secara ekonomis dan ini dapat digunakan sebagai bahan awal. Tegasnya, semuanya berasal dari unsur-unsur penyusunnya atau dapat diturunkan darinya, sehingga setiap sintesa yang dilakukan dari bahan baku tersebut akan “secara formal” merupakan sintesa total.
Metodologi sintesis untuk menghadapi sintesis yang sukses telah berubah seiring berjalannya waktu dan perkembangan ilmu kimia itu sendiri, sehingga dikenal sebagai berikut:
- Metodologi “asosiasi langsung”
- Metodologi “pendekatan menengah”
- Metodologi "analisis logis"
- Detail
- Wilbertrivera
- SINTESIS ORGANIK
- Dilihat: 30354
Elaborasi " pohon sintesis " berdasarkan pembangkitan molekul perantara atau prekursor, selangkah demi selangkah ke arah antitesis (retrosintesis), yaitu dimulai dari molekul tujuan, merupakan metode yang dapat dipahami dengan lebih baik dengan mempertimbangkan prinsip-prinsip umum berikut dari proses tersebut.
1. Mulailah dengan struktur akhir (MOb). Mulai dari struktur akhir, molekul target, bekerja mundur (retrosintesis) hingga diperoleh bahan baku yang mudah dijangkau. Jika bahan baku awal ditentukan dalam masalah sintesis, ini hanya membatasi jumlah rute sintetik yang mungkin untuk ditangani.
2. Karakterisasi molekul target (MOb ). Saat memeriksa struktur molekul target, perlu dijawab pertanyaan-pertanyaan berikut:
ke. Apa jenis senyawa itu?
B. Grup fungsional apa yang dikandungnya?
C. Apa sifat kerangka karbon?
D. Apakah molekul tersebut memiliki rantai alkil normal atau bercabang?
Dan. Apakah itu mengandung cincin dan apakah itu sikloalkil atau aromatik?
F. Apakah MOb memiliki simetri aktual atau potensial?
3. Gugus Fungsional . Dalam hal ini, ada baiknya juga menjawab pertanyaan-pertanyaan berikut:
ke. Apakah reaktivitas, sensitivitas, dan ketidakstabilan gugus fungsi yang dimiliki MOb diketahui?
B. Metode umum apa yang tersedia untuk persiapannya?
C. Manakah dari mereka yang berlaku untuk kelompok fungsional tertentu dari molekul masalah?
- Detail
- Wilbertrivera
- SINTESIS ORGANIK
- Dilihat: 36347
Sintesis n-Hexanol ( MOb 02)
Solusi : n-Hexanol (MOb 02) adalah alkohol primer yang rantai karbonnya tidak bercabang. Oleh karena itu, strategi dikurangi untuk mencari reaksi yang memungkinkan rantai tumbuh dalam jumlah atom karbon yang baik. Tidak disarankan pertumbuhan rantai satu per satu, karena jalur ini akan mengarah pada rencana sintesis dengan banyak tahapan, akibatnya hasil yang rendah.
Dengan demikian, pembukaan cincin epoksida oleh senyawa Grignard cukup memadai untuk tujuan ini; karena juga dapat dikombinasikan dengan sintesis asetilena (penggunaan turunan natrium asetilida dan saturasi berikutnya dari ikatan rangkap tiga).
Epoksida yang diperlukan untuk bergabung dengan Grignard dibuat dari alkena dan asam perasam. Dengan demikian, rencana sintesis ini disimpulkan, di mana bahan awal dapat berupa asetilena dan etanol.
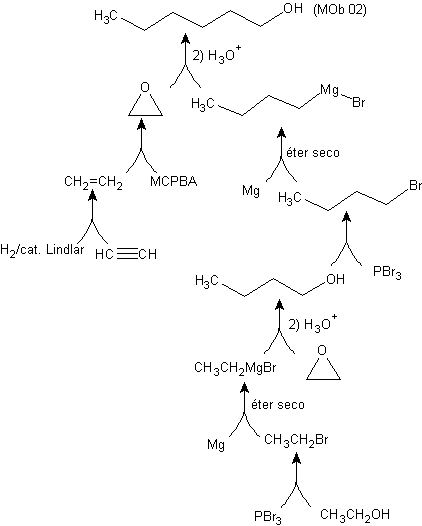
Selengkapnya: Masalah Sintesis, diselesaikan dengan metode Pohon Sintesis
- Detail
- Wilbertrivera
- SINTESIS ORGANIK
- Dilihat: 41943
Pembentukan enol dan enolat
Karbon alfa dari senyawa yang mengandung gugus karbonil (aldehida, keton, ester, diketon, diester, nitrat, nitril, dll.), Merupakan pusat dari banyak reaksi pembentukan ikatan CC. Karena keasaman H a , mereka mengalami -deprotonasi dengan adanya basa yang cocok, dengan konsekuensi pembentukan karbanion. Muatan negatif yang dihasilkan pada C a hingga C=O distabilkan resonansinya oleh gugus karbonil yang sama.
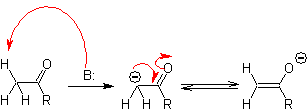
Pemilihan basa, untuk pembentukan enolat, tunduk pada fakta bahwa pKa asam konjugasi basa harus lebih besar setidaknya tiga unit daripada pKa senyawa karbonil yang memiliki asam H .
| pKa = 20 | MeO- pKa = 15 | Pembentukan enolat yang tidak menguntungkan |
| pKa = 10 | tBuO- _ pKa = 19 | Pembentukan enolat sangat menguntungkan |
Pembentukan enolat:
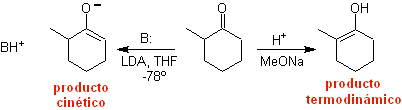
¨ Enolat kinetik
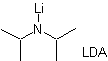
Itu terjadi karena substrat memiliki H α , mudah diakses untuk deprotonasi melalui basis tipikal seperti LDA (pKa
kira-kira 30) LDA (lithium diisopropylamide) adalah basa yang kuat, non-nukleofilik, dan terhalang secara sterik. |
|
¨
Enolat dari ester:
Ester rentan terhadap reaksi substitusi untuk basa, LDA bisa menjadi masalah, itulah sebabnya basa non-nukleofilik (lithium isopropylcyclohexyl amide) digunakan dengan ester.
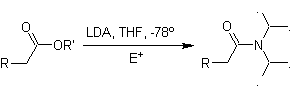
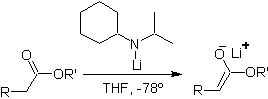
¨
Enolat termodinamika:
Deprotonasi reversibel dapat menghasilkan enolat yang lebih stabil, yang terjadi ketika lebih banyak C=C tersubstitusi dari bentuk enol diperoleh.
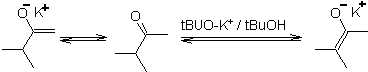
Kondisi umum untuk membentuk enolat termodinamika adalah: RO-M+ dalam ROH sebagai pelarut protik (pKa ROH = 15 sampai 18).
Enolat kinetik dan termodinamika dapat dijebak, diisolasi, dipisahkan, dan dimurnikan untuk mendapatkan enolat murni secara regiokimia. Hal ini dapat dicapai dengan pembentukan asetat enol dan silylene eter.
- Detail
- Wilbertrivera
- SINTESIS ORGANIK
- Dilihat: 47100
Reaksi Enol dan Enolat
Reaksi aldol dan yang disebut reaksi kondensasi senyawa karbonil dan lainnya jenis ini, yang dapat membentuk struktur enol dan enolat, berpartisipasi dalam sekelompok besar reaksi penting yang memungkinkan kita untuk memahami keberadaan sejumlah besar molekul yang dihasilkan dari interaksi enol atau enolat dengan serangkaian gugus elektrofilik.
Studi tentang jenis reaksi ini telah memungkinkan untuk memverifikasi dan menetapkan keberadaan dua mekanisme reaksi yang terjadi, seperti yang dijelaskan di bawah ini:
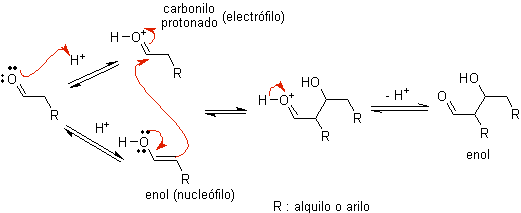
KE)
Ketika asam digunakan sebagai katalis, senyawa karbonil mula-mula terprotonasi dan kemudian diautomerisasi menjadi bentuk enolnya , yang merupakan nukleofil pada karbon alfa menjadi gugus karbonil. Media asam yang sama cukup untuk mengaktifkan gugus karbonil dari molekul lain, menjadikannya sangat elektrofilik, yang menghasilkan kondisi optimal untuk menghasilkan senyawa karbonil tak jenuh.
Reaksi biasanya berlangsung sampai dehidrasi enol terbentuk, dikatalisis oleh asam yang sama dari reaksi.
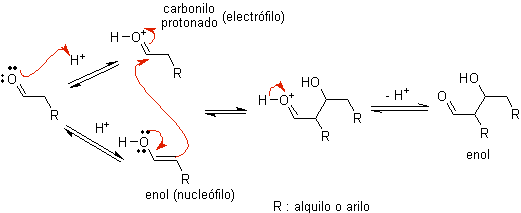
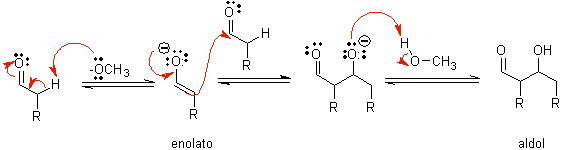
B) Ketika katalis adalah basa, seperti alkoksida, reaksi tipe aldol berlangsung melalui serangan nukleofilik dari enolat yang distabilkan oleh resonansi pada gugus karbonil dari molekul lain.
Dengan dehidrasi aldol, dikatalisis oleh basa, produk akhir dehidrasi terbentuk.
Seperti pada kasus sebelumnya, dehidrasi yang dikatalisis oleh basa (kadang-kadang ditulis sebagai langkah tunggal), memungkinkan untuk mengontrol reaksi dan menghasilkan produk akhir yang terdehidrasi. Dalam beberapa kasus, pembentukan enolat bersifat ireversibel.
bagaimana tampilannya hanya sejumlah katalitik basa yang diperlukan dalam beberapa kasus, prosedur yang paling umum adalah menggunakan sejumlahestequiométrica basa kuat seperti LDA atau NaHMDS . Dalam hal ini, pembentukan enolat bersifat ireversibel, dan produk aldol tidak terbentuk hingga logam alkoksida dari produk aldol terprotonasi pada langkah selanjutnya.
- Detail
- Wilbertrivera
- SINTESIS ORGANIK
- Dilihat: 35629
Sintesis organik, jantung dari kimia organik , pada dasarnya adalah kegiatan heuristik , yaitu, itu adalah proses di mana kegiatan kreatif yang sangat prediktif dari pemikiran logis dan prosedur empiris, kaya akan elaborasi artistik, bergabung, menjadikan ahli kimia organik benar-benar inovatif.
Seperti metode apa pun, " metode pemutusan atau sinton " memiliki struktur, simbologi, dan bahasanya sendiri, yang pada awalnya harus diasimilasi dan dipahami oleh mereka yang ingin menggunakan alat sintetik ini.
Metode sintesis pemutusan atau synthon , termasuk Dua fase;
![]() Fase analisis retrosintetik . Ini menunjukkan semua transformasi yang akan dilakukan dalam proses penyederhanaan struktur
Fase analisis retrosintetik . Ini menunjukkan semua transformasi yang akan dilakukan dalam proses penyederhanaan struktur
![]() Fase sintesis . Di mana apa yang "berpikir", berdasarkan kriteria rasionalitas mekanistik dan reaktivitas senyawa organik, terwujud dalam jalur sintesis yang akan ditulis, seperti yang diharapkan terjadi di laboratorium kimia. Di sinilah pengalaman muncul dan memanifestasikan " seni melakukan atau ". menciptakan ”dari ahli kimia, yaitu.
Fase sintesis . Di mana apa yang "berpikir", berdasarkan kriteria rasionalitas mekanistik dan reaktivitas senyawa organik, terwujud dalam jalur sintesis yang akan ditulis, seperti yang diharapkan terjadi di laboratorium kimia. Di sinilah pengalaman muncul dan memanifestasikan " seni melakukan atau ". menciptakan ”dari ahli kimia, yaitu.
Itu istilah, definisi atau operasi sintesis, yang sering digunakan dalam metode ini, adalah sebagai berikut:
Molekul Sasaran (MOb) .
Ini adalah nama yang diberikan untuk setiap molekul yang akan disintesis atau disiapkan dari bahan yang sederhana dan terjangkau, yang dalam suatu masalah dapat ditentukan sebelumnya atau disesuaikan dengan pilihan yang dihasilkan ahli kimia dalam rencana atau desain sintesisnya.
transformasi . ( ![]() ).
).
Panah retrosintesis satu arah khusus harus dipahami sebagai representasi simbolis dari ungkapan " dipersiapkan dari " dan juga mewakili semacam transformasi dalam struktur
Jenis-jenis transformasi yang dimaksud sebenarnya adalah operasi retrosintetik seperti: Disconnections, Reconnections, Rearrangements, Interconversion of Functional Groups (IGF), Addition of Functional Groups (AGF), Deletion of Functional Groups (SGF), dll.
- Detail
- Wilbertrivera
- SINTESIS ORGANIK
- Dilihat: 27861
PEMUTUSAN SENYAWA 1,3-DIOKSIGEN
Senyawa organik teroksigenasi adalah yang paling melimpah di alam dan khususnya dioksigenat, itulah sebabnya banyak peneliti kimia memodelkan pemutusan retrosintetik dari molekul-molekul ini, suatu aspek yang akan dipelajari dalam paragraf berikut.
Pertama-tama, model pemutusan molekul terdioksigenasi telah dibagi menjadi dua kelompok besar, berdasarkan sifat sinton yang dihasilkan dengan penerapan operasi sintetik dasar yang disebut " PEMUTUSAN" ke molekul yang akan disintesis dan umumnya itu disebut sebagai molekul target (MOb) .
Kelompok besar tersebut adalah:
![]() Model pemutusan “ logis ”, dan
Model pemutusan “ logis ”, dan
![]() Model pemutusan “ anomali ” atau “ tidak logis ”.
Model pemutusan “ anomali ” atau “ tidak logis ”.
Apa yang disebut model pemutusan "logis" adalah yang, dengan menerapkan "pemutusan" satu atau beberapa ikatan kimia di
Senyawa yang dapat diklasifikasikan sebagai 1,3-dioksigen dan 1,5-dioksigen, ketika mengalami retrosintesis, umumnya membentuk sinton yang dianggap "logis". Di sisi lain, molekul organik yang terkait dengan 1,2-dioksigenasi, 1,4-dioksigenasi, dan 1,6-dioksigenasi, menghasilkan sinton
dianggap “tidak logis”
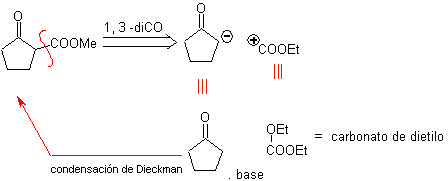
Model cut-off 1,3-dioksigen
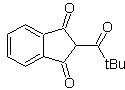
![]() senyawa β-dikarbonil
senyawa β-dikarbonil
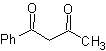
Senyawa 1,3-dikarbonil diperoleh dengan hasil yang baik melalui reaksi kondensasi tipe Claisen, yang melibatkan reaksi antara ester dan senyawa dengan hidrogen aktif, seperti: ester, keton, aldehida, nitril, turunan nitro, dan beberapa hidrokarbon dengan adanya reagen alkali.
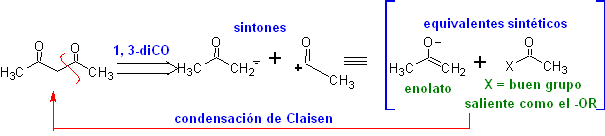
β-diketon dan β-ketoaldehida diperoleh dengan kondensasi silang Claisen, menggunakan keton dan ester yang sesuai. Dalam kondensasi Claisen silang dari keton dan ester, hasil yang baik diperoleh karena keton lebih asam daripada ester, oleh karena itu, dalam media basa, keton terdeprotonasi ke tingkat yang lebih besar daripada ester.
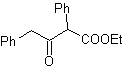
Contoh : Usulkan desain sintesis dari bahan sederhana, untuk molekul berikut:
MOb 16
| massa 17
| MOb 18
|
Larutan:
MOb 16 . Rupanya dua alternatif pemutusan (a) dan (b), ditunjukkan pada
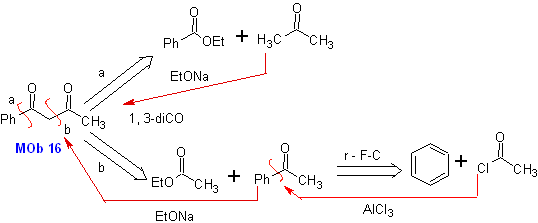
Namun, alternatif (b) ternyata yang paling cocok, karena, dalam media reaksi basa, karbanion yang terbentuk PhCOCH 2 - akan lebih stabil, karena efek resonansi dan induktif.
- Detail
- Wilbertrivera
- SINTESIS ORGANIK
- Dilihat: 25760
Senyawa 1,5-dioksigenasi umumnya merupakan hasil reaksi adisi konjugasi nukleofil dari senyawa karbonil, dengan asam H α (enol, enolat, enamina, dll.), serta nitril dan nitrat, pada substrat alfa beta tak jenuh sehubungan dengan ke gugus karbonil dan sejenisnya, yang dikenal sebagai reaksi Michael, dengan opsi komplementer menjadi reaksi Nef dan reaksi anulasi (anulasi) Robinson.
Putuskan model 1, 5 dioksigen (1,5-diO)
Model pemutusan 1,5-diO dapat diterapkan, setelah fungsionalisasi yang diperlukan, untuk senyawa seperti: 1,5-dihidroksil, 1,5-hidroksialdehida, 1,5-hidroksiketon, 1,5-hidroksiester, 1, 5- ketoaldehida, 1,5-diketon, 1,5-ketoester, 1,5-dialdehida, dll.
Kemungkinan meningkat jika nitroderivatif dan nitril juga diperhitungkan, yang dapat membentuk karbanion yang sangat reaktif dalam media dasar yang mampu menambah senyawa karbonil tak jenuh α,β untuk mendapatkan produk tipe 1,5-diO.
Analisis fundamental pemutusan senyawa 1,5-diO adalah sebagai berikut:
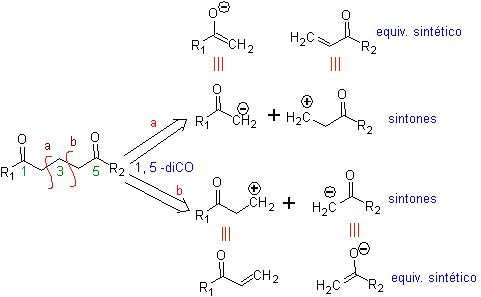
Pilihan pemutusan (a) atau (b), di sekitar C3, akan tergantung pada sifat dari kelompok R1 dan R2, yang dapat memberikan stabilitas yang lebih besar atau lebih kecil untuk sinton atau ekuivalen sintetik yang diperlukan untuk pembentukan
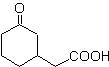
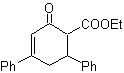
Usulkan desain sintesis untuk MOb 29, 30 dan
MOb 29
| MOb 30
| MOb 31
|
Larutan:
MOb 29 . Analisis retrosintetik: karbanion diperlukan untuk menambah senyawa tak jenuh a , b -CO Ini dapat diperoleh dari dietil malonat dalam media dasar. Yang selanjutnya akan memaksa dekarboksilasi, untuk mencapai
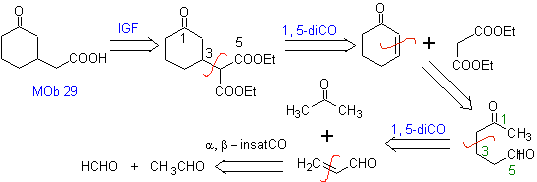
- Detail
- Wilbertrivera
- SINTESIS ORGANIK
- Dilihat: 61324
Dalam desain sintesis molekul dengan beberapa gugus fungsi, sangat umum bahwa reagen yang menghasilkan transformasi pada gugus fungsi juga memengaruhi gugus lain yang ada di bagian lain molekul. Dalam kasus di mana kemoselektivitas yang memadai tidak dapat dicapai pada gugus fungsi yang akan ditransformasikan, gugus yang harus tetap tidak berubah dilindungi dengan mengubahnya sementara menjadi fungsionalitas yang inert terhadap kondisi reaksi.
Operasi perlindungan memerlukan prosedur berikut:
· Lindungi gugus fungsi yang paling reaktif secara selektif dan dalam kondisi ringan.
· Melakukan reaksi pada gugus fungsi yang diperlukan tanpa mempengaruhi gugus yang dilindungi
· Unproteksi grup fungsional, mengalami perlindungan
Itu tindakan perlindungan harus memenuhi persyaratan dasar berikut:
· Reaksi harus bekerja dengan baik dan menjadi chemoselective.
· Gugus fungsi baru harus stabil di bawah kondisi reaksi gugus yang akan bereaksi.
· Fungsionalitas yang diperkenalkan tidak boleh menambahkan pusat kiral ke molekul yang dapat menghasilkan diasteromer
· Gugus fungsi asli harus dapat diregenerasi dengan hasil yang baik dan tanpa mempengaruhi sisa molekul.
Penggunaan pelindung harus dikurangi seminimal mungkin dan pilihannya harus sedemikian rupa sehingga tidak perlu diganti selama sintesis, karena langkah pengenalan dan penghilangan (deproteksi) menambah biaya dan kerja untuk sintesis dan menurunkan hasil. Contoh.
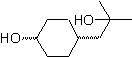
Gugus ketonik dari molekul telah dilindungi dengan mengubahnya menjadi ketal siklik, dengan etanadiol dalam media yang sedikit asam, selanjutnya molekul ini telah direaksikan dengan dua mol fenil magnesium bromida, yang bekerja pada gugus ester, untuk mengubahnya. menjadi alkohol tersier, dengan dua substituen metil yang disumbangkan oleh Grignard. Akhirnya, ketal siklik dihidrolisis untuk meregenerasi keton.
Dalam praktiknya, tidak ada grup pelindung yang sempurna untuk setiap fungsi, sebaliknya dapat dipastikan bahwa ada banyak pelindung yang mungkin, yang masing-masing memenuhi kondisi di atas dalam keadaan tertentu. Daftar singkat perlindungan dari kelompok yang paling umum disertakan dalam bagian berikut:
Selengkapnya: Perlindungan Gugus Fungsional dalam Sintesis Organik
- Detail
- Wilbertrivera
- SINTESIS ORGANIK
- Dilihat: 29397
Kontrol dalam sintesis organik adalah salah satu tugas terpenting untuk mencapai transformasi yang diperlukan atau direncanakan. dan/atau untuk menghindari pembentukan produk sampingan yang secara substansial mengganggu perkembangan optimal sintesis organik yang bersangkutan. Demikian pula, dari perspektif yang lebih umum, kontrol juga dapat mencakup atau mencakup aspek simetri dan selektivitas.
Kemudian, kontrol harus dipahami sebagai serangkaian operasi sintetik yang memungkinkan ahli kimia membentuk kerangka karbon dengan fungsi yang dimaksudkan atau untuk "menempatkan" suatu kelompok atau atom di tempat atau posisi yang diperlukan.
Konsekuensinya, operasi ini mungkin dari berbagai rutinitas dengan maksud yang dicerminkan oleh ahli kimia dan yang menuntut kemampuan dan keterampilan kognitif tertentu yang serupa dengan yang artistik, untuk konstruksi (sintesis) molekul organik.
Oleh karena itu, dalam reaksi kondensasi, seperti yang lainnya, operasi kontrol dapat dimasukkan dalam salah satu kategori berikut.
![]() Reaksi bersaing (self-kondensasi dan/atau kondensasi silang)
Reaksi bersaing (self-kondensasi dan/atau kondensasi silang)
![]() Aktivasi – penonaktifan
Aktivasi – penonaktifan
![]() Selektivitas dan spesifisitas
Selektivitas dan spesifisitas
![]() Proteksi-deproteksi
Proteksi-deproteksi
Dalam reaksi kondensasi senyawa karbonil, penting untuk menetapkan urutan kejadian terlebih dahulu untuk meminimalkan atau, jika perlu, menekan kemungkinan kondensasi sendiri dan terjadinya kondensasi silang, yang sayangnya merupakan ancaman nyata dalam reaksi ini. .
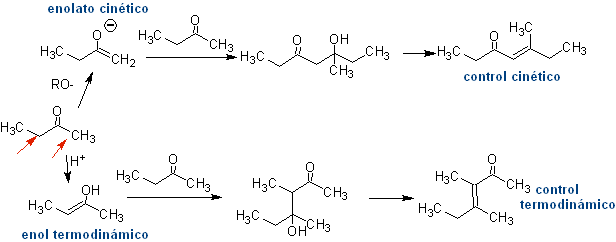
kondensasi diri
Semua senyawa karbonil yang memiliki satu atau lebih hidrogen alfa, pada karbon yang berdekatan dengan gugus karbonil, berisiko mengalami reaksi kondensasi sendiri jika kekakuan yang sesuai tidak diikuti.
Jadi, misalnya, jika basa non-hidroksilasi seperti EtONa ditambahkan ke 2-butanon, enolat akan terbentuk yang pada akhirnya dapat bergabung dengan molekul lain dari keton yang sama. Demikian pula, jika H+ ditambahkan, kondensasi diri juga dapat terjadi, seperti dapat dilihat pada skema berikut: Hal ini dapat diminimalkan dengan menambahkan pada tingkat yang sama, dari pengumpan terpisah, basa atau asam ke senyawa yang akan menghasilkan enol atau enolat dan senyawa karbonil yang akan diserang pada karbon karbonil. . Labu berleher tiga dan pengaduk magnet dapat digunakan.
- Detail
- Wilbertrivera
- SINTESIS ORGANIK
- Dilihat: 25782
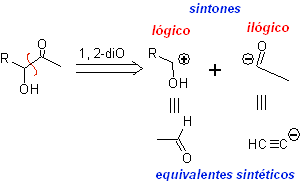
Pemutusan senyawa 1,2-dioksigenasi
1.- Senyawa a -hidroksikarbonil
- Detail
- Wilbertrivera
- SINTESIS ORGANIK
- Dilihat: 26430
PEMISAHAN SENYAWA 1,4-DIOKSIGEN
Kelompok senyawa lain yang sangat penting dalam sintesis kimia terdiri dari molekul teroksigenasi yang ditemukan dalam rasio jarak 1,4. Senyawa-senyawa ini, ketika dikenai analisis pemutusan retrosintetik, menghasilkan sinton, di mana salah satunya, elektrofil atau nukleofil, dapat dianggap "anomali" atau "tidak logis", karena muatan yang diberikan ke salah satu atom tidak dapat dijelaskan dalam hal elektronegativitas intrinsik atau terinduksi.
1. Senyawa 1,4-dioksigen (1,4-diO)
Dalam jenis senyawa ini, pemutusan juga mengarah ke sinton logis dan sinton tidak logis lainnya (non-alami), yang dapat berupa nukleofil atau elektrofil, yang padanan sintetiknya masih harus dikerjakan ulang secara memadai, agar dapat digunakan dalam reaksi kimia.
1. 1. Senyawa 1,4-dikarbonil
1.1.1. senyawa 1,4-diketon
Alternatif pemutusan jenis senyawa atau molekul yang akan disintesis (MOb), dapat menyebabkan pilihan berikut:
ke. Synthon anion yang logis dan synthon kation yang tidak logis
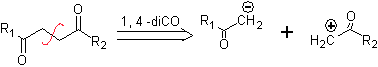
Setara sintetik anion adalah ion enolat atau enol itu sendiri dari senyawa karbonil. Sebaliknya padanan sintetik untuk karbokation adalah alfa halokarbonil. (Umpolung)
- Detail
- Wilbertrivera
- SINTESIS ORGANIK
- Dilihat: 21784
PEMUTUSAN SENYAWA 1,6-DIOKSIGEN
Senyawa 1,6-difungsional lebih disukai menggunakan strategi rekoneksi untuk sintesisnya masing-masing; Strategi ini dapat dikombinasikan dengan sangat baik dengan reaksi Diels-Alder, yang umumnya menghasilkan adisi olefin beranggota enam, atau reduksi Birch dari cincin benzena, yang juga menghasilkan produk olefin beranggota enam.
1. senyawa 1,6-dioksigenasi
Reaksi yang menghasilkan senyawa dikarbonil, dengan berbagai kemungkinan kombinasi: diketon, asam keto, ketoaldehida, asam diasam, dll. Dan pada jarak yang berbeda satu sama lain, tidak diragukan lagi merupakan reaksi dari ozonolisis senyawa olefin.
Bergantung pada struktur substrat dan kondisi reaksi pada zat antara ozonida yang terbentuk, keragaman senyawa yang sangat besar akan dicapai sebagai hasil dari pembelahan ikatan rangkap olefinik. Dari jumlah tersebut, yang berada dalam rasio 1,6-dioksigenasi sangat menarik, seperti yang dapat disimpulkan dari operasi "penyambungan kembali" sintetik berikut:
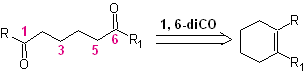
Cara terbaik untuk memahami pengoperasian "operasi rekoneksi sintetik" ini adalah akan dicapai melalui solusi sintesis molekul organik berikut:
MO 50
| MO 51
| MO 52
| ||
MO 53
| MO 54
| MO 55
|
- Detail
- Wilbertrivera
- SINTESIS ORGANIK
- Dilihat: 25311
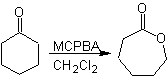
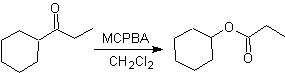
Oksidasi Baeyer–Villiger
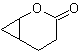
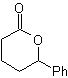
Reaksi lain yang dapat dikaitkan dengan strategi Retrosintesis adalah oksidasi keton oleh asam peroksi, lebih dikenal sebagai reaksi Baeyer-Villiger. Dalam keton siklik, oksidasi dengan peracid menghasilkan lakton. Gugus yang melekat pada keton asimetris memiliki kemampuan migrasi, yang memungkinkan, secara literal, untuk "memasukkan atom oksigen" antara gugus karbonil dan gugus migrasi, sehingga menghasilkan ester atau lakton.
Perlu diperhatikan bahwa enon (α, β tak jenuh keton) bukanlah substrat yang baik untuk oksidasi Baeyer-Villiger, karena alkena jauh lebih reaktif daripada keton. Namun Ada struktur khusus di mana alkena dapat dilindungi oleh substituen terdekat karena efek sterik dan dengan demikian mengarahkan serangan peracid ke arah gugus karbonil.
| … |
|
Ingatlah bahwa kemampuan migrasi dari berbagai kelompok, dalam reaksi Baeyer-Villiger, adalah sebagai berikut:
H> Ph> 3º alkil> sikloalkil> 2º alkil> 1º alkil> Me
Usulkan rencana sintesis untuk molekul-molekul berikut:
MO 56
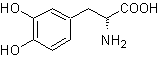
L-Dopa | . | MO 57
| . | MO 58
|
MO 59
| MO 60
| massa 61
|
MO 56. Analisis retrosintetik.
Asam alfa amino
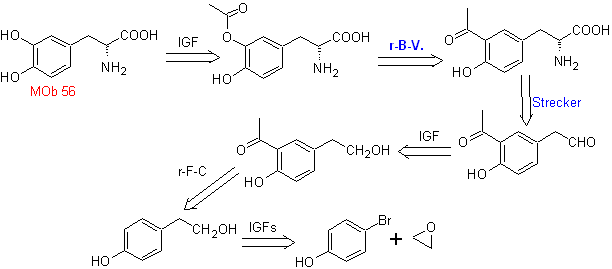
Perpaduan. Untuk Untuk pembentukan Grignard yang diperlukan, orto OH dari benzena dilindungi. Sintesis Strecker memungkinkan pembentukan asam amino alfa, yang dioksidasi menurut Baeyer-Villiger dengan peracid dan produk mengalami hidrolisis asam dari gugus ester, yang mengarah pada pembentukan
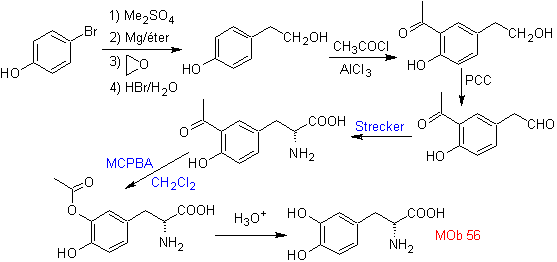
Selengkapnya: Oksidasi Baeyer-Villiger sebagai strategi dalam Retrosintesis
- Detail
- Wilbertrivera
- SINTESIS ORGANIK
- Dilihat: 29495
Transposisi Beckmann sebagai strategi dalam
Penataan ulang oksim dalam media asam, disebut penataan ulang Beckman, menghasilkan amida atau laktam jika keton awalnya linier atau siklik.
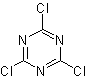
Untuk meningkatkan kinerja jenis reaksi ini, berbagai katalis dan media asam telah dipelajari. Jadi, misalnya, media asam baru yang digunakan sebagai katalis, dengan tujuan yang ditunjukkan, adalah: TCT/DMF, DAST/CH 2 CL 2 , CF 3 SO 3 H, PCl 5 , HgCl 2 /MeCN dan ZnO.
TCT: triklortriazin | …… | DAST: dietilanosulfida trifluorida |
Kecocokan migrasi kelompok sama dengan reaksi Baeyer-Villiger. Usulkan desain sintesis untuk masing-masing molekul berikut:
MO 62 | massa 63 | MO 64 |
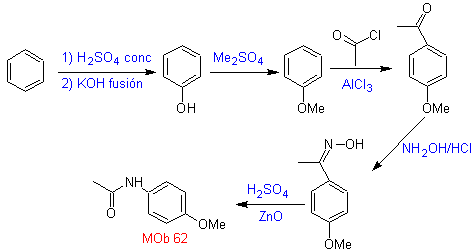
MOb 62 . Analisis retrosintetik.
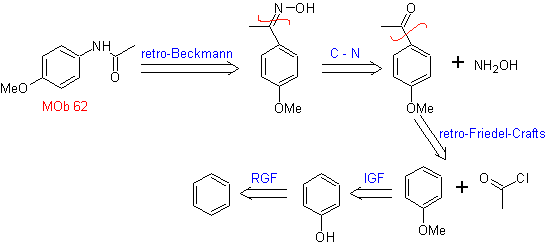
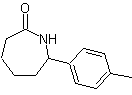
Perpaduan. Reaksi antara keton aromatik dengan NH 2 OH dan perlakuan selanjutnya dengan larutan asam sulfat dan ZnO dalam air, memungkinkan pembentukan amida aromatik MOb 62.
Selengkapnya: Penataan ulang Beckmann sebagai strategi dalam Retrosintesis
- Detail
- Wilbertrivera
- SINTESIS ORGANIK
- Dilihat: 21216
Strategi sintesis lain yang menggunakan sinton "tidak logis".
1.
penambahan ikatan rangkap tiga
Strategi "menambahkan" ikatan rangkap tiga, antara dua fungsi teroksigenasi pada posisi 1,4, memungkinkan bekerja nanti dengan pemutusan berdasarkan kimia asetilida. Untuk mencontohkan strategi ini, mari kita lihat penjabaran rencana sintesis untuk
Massa. 40. Analisis Retrosintetik . IGF pertama masuk
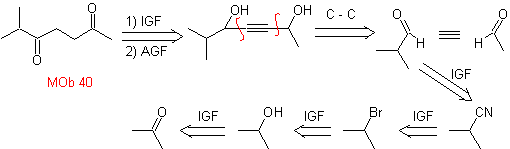
Perpaduan. Diacetylide atau acetylide secara bertahap, bergabung dengan molekul aldehida yang berbeda, molekul perantara yang terbentuk dihidrogenasi dan kemudian alkoholnya dioksidasi menjadi senyawa diketonik Mob 40.
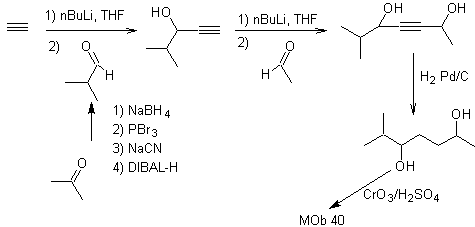
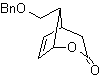
γ-lakton juga dapat dibuat dengan cara yang analog, seperti yang ditunjukkan di bawah ini:

2.
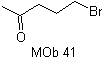
Menambahkan grup COOR sebagai grup pengaktif
Penambahan gugus COOR, selain mengaktifkan sinton anion, memfasilitasi pemutusan molekul 1,4 diX.
mempersatukan |
|
MOb 41. Analisis retrosintetik.
Selengkapnya: Strategi sintesis lain yang menggunakan sinton "tidak logis".
- Detail
- Wilbertrivera
- SINTESIS ORGANIK
- Dilihat: 51079
SINTESIS SENYAWA AROMATIK I
(Metode Pohon Sintesis)
Usulkan rencana sintesis, menggunakan toluena atau xilena sebagai bahan awal, untuk molekul-molekul berikut:
(MOb 12)
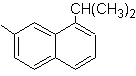
1-isopropil-7-metilnaftalena | (MOb 13)
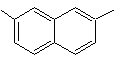
2,7-dimetilnaftalena |
(MOb 14)
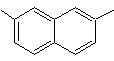
1-isopropil-6-metilnaftalena | (MOb 15)
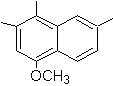
4-metoks-1,2,7-trimetilnaftalena |
Solusi: (MOb 12).
Dalam strategi yang diasumsikan, diperhitungkan bahwa tahap terakhir dapat merespons proses "aromatisasi", yang diusulkan agar molekul prekursor menghadirkan cincin non-aromatik, dengan ikatan rangkap.
pada karbon yang mengandung ikatan rangkap dan gugus alkil.
Struktur ini dapat dicapai dengan aksi Grignard pada karbonil dan dehidrasi selanjutnya dari alkohol yang terbentuk. Keton dibentuk oleh asilasi pada senyawa benzena yang sesuai dengan anhidrida suksinat dan penutupan asilasi intramolekul Friedel-Crafts berikutnya.
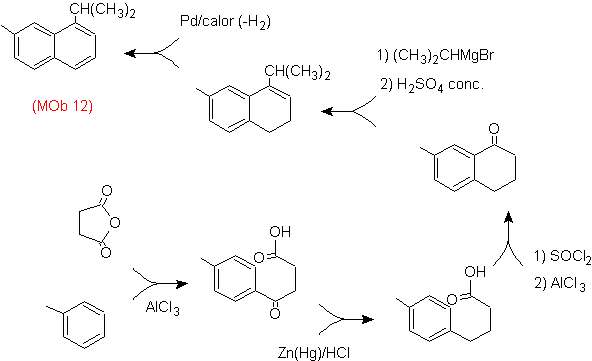
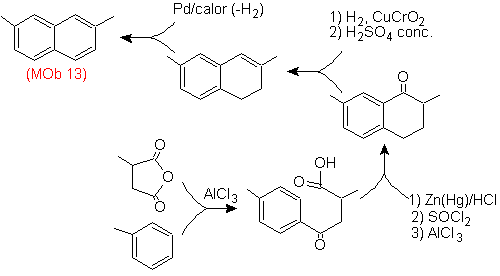
Solusi (MOb 13).
Sekali lagi, molekul prekursor harus "diaromatisasi", strategi yang paling tepat di antara yang lain Ini didasarkan pada kombinasi asilasi dengan anhidrida suksinat tersubstitusi dan reduksi Clemmensen.
Karbonil terakhir direduksi menjadi alkohol yang kemudian akan didehidrasi dengan molekul hidrogen dan katalis yang disebut kromil tembaga.
- Detail
- Wilbertrivera
- SINTESIS ORGANIK
- Dilihat: 29290
SINTESIS SENYAWA AROMATIK II
(Metode Pohon Sintesis)
Meskipun salah satu masalah pertama yang harus diselesaikan dalam sintesis senyawa aromatik multisubstitusi adalah kontrol efek orientasi dan pembentukan isomer yang tidak diinginkan, penting juga untuk mempelajari reaktivitas arena, karena pada beberapa titik di rasa kehadiran gugus alifatik dalam senyawa aromatik, berkali-kali, mereka menunjukkan karakteristik dan reaktivitas, tipikal dari jenis senyawa organik yang mereka miliki dan yang khusus yang dihasilkan dari interaksi timbal balik antara gugus alifatik dan aromatik.
Pada tujuan ini, didasarkan, the sintesis molekul No. 20 hingga 27, kali ini dari bahan yang ditentukan, sehingga pertanyaan yang disajikan sebagai berikut: Apa reaksi itu Benarkan transformasi berikut?
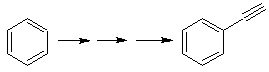
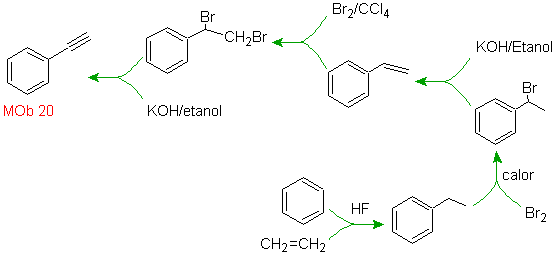
Solusi massa 20.
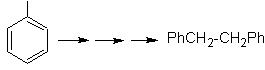
Kita tahu bahwa tidak ada kemungkinan ion asetilida bekerja langsung pada benzena ikatan rangkap tiga diperoleh dari gugus alkil
vec-dibrominated, yang diperoleh dengan brominating styrene, sebelumnya diperoleh dengan dehydrobrominating dari benzil halida yang dibentuk oleh brominasi oleh mekanisme radikal bebas pada etilbenzena
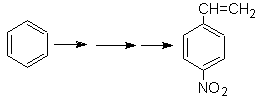
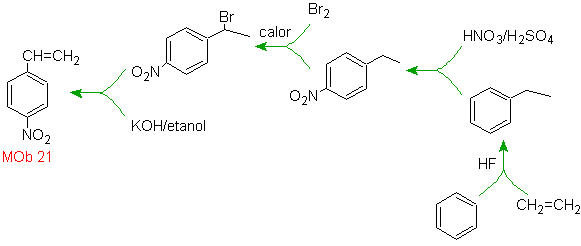
Solusi Massa 21.
Para nitrostirena tidak dapat diperoleh dengan nitrasi langsung dari stirena, karena gugus etenil yang terikat pada cincin tidak stabil dalam kondisi nitrasi.
Dengan demikian, molekul prekursor akan memiliki gugus yang mudah didehidrobrominasi. Prekursor ini diperoleh dengan brominasi radikal dari gugus etil yang berikatan dengan cincin benzena, yang sebelumnya dinitrasi terutama pada posisi para.
- Detail
- Wilbertrivera
- SINTESIS ORGANIK
- Dilihat: 32534
SINTESIS DARI ALKOHOL
(Metode Pohon Sintesis)
Usulkan rencana sintesis untuk molekul target yang ditunjukkan dari molekul tunggal yang ditunjukkan (MOb 30 -41). Untuk melakukan ini, gunakan reagen dan kondisi reaksi yang menurut Anda perlu:
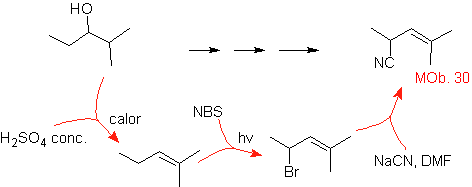
Solusi MOb 30.
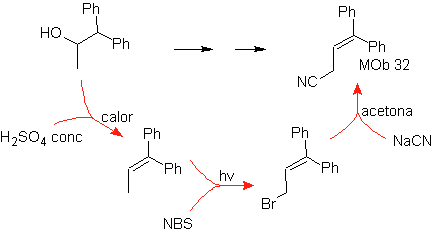
Strategi: Diamati bahwa molekul awal telah mengalami dehidrasi dan pada posisi alilik yang awalnya tidak tersubstitusi, sebuah hidrogen telah digantikan oleh gugus siano atau nitril. Reaksi terakhir ini dapat terjadi hanya jika molekul prekursornya adalah alilik halida, oleh karena itu diusulkan sebagai prekursor dari
Br diperkenalkan pada posisi yang diinginkan dengan NBS dan alkena adalah produk dari dehidrasi molekul awal.
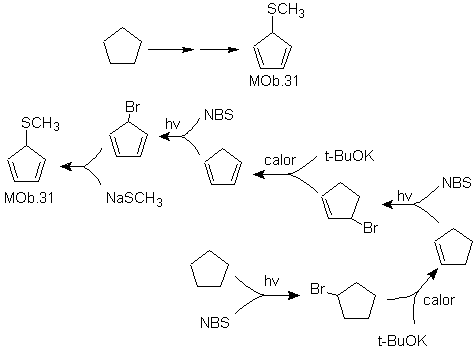
Solusi MOb 31.
Strategi : Ini adalah eter paman, molekul prekursor yang diperlukan adalah 1,3-siklopentadiena halida.
Halida ini dibuat dengan aksi NBS pada diena sikloalkena, yang selanjutnya dibuat dengan dehidrobrominasi molekul prekursor, yang dicapai dengan aksi NBS pada sikloalkena yang terbentuk. sebelumnya dengan dehidrohalogenasi molekul awal yang dibrominasi oleh radikal
Solusi Mob 32.
Strategi : Ini mirip dengan yang digunakan dalam memperoleh
- Detail
- Wilbertrivera
- SINTESIS ORGANIK
- Dilihat: 25074
Reaksi ini biasanya membentuk cincin heterosiklik beranggota lima, yang membutuhkan reaksi antara senyawa n1,3 dipolar dan alkena. Reaksinya adalah sikloadisi [3-2]. Senyawa 1,3-dipolar yang paling banyak digunakan untuk membentuk heterosiklik pentagonal adalah:
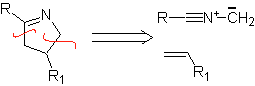 | 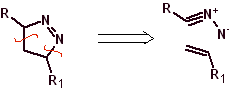 |
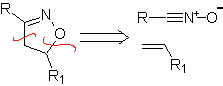 | 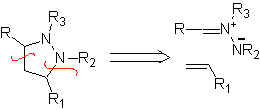 |
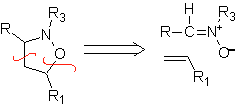 | 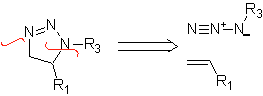 |
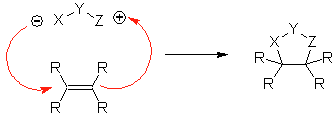
| MOb: 86
| . | MOb: 87 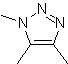 | .. | MOb: 88 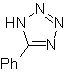 |
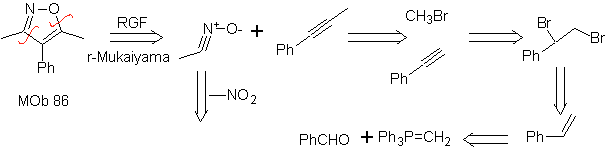
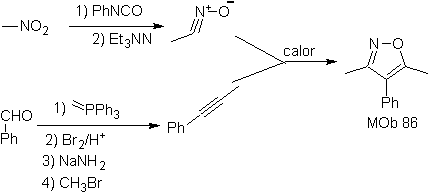
Selengkapnya: Sintesis heterosiklik dengan siklisasi antarmolekul