Les nucléophiles durs (organométalliques, amides, hydrures de lithium et d'aluminium) attaquent la position 2 du cycle pyridine, donnant lieu à des réactions d'addition nucléophiles. Dans le cas où une dernière étape d'oxydation se produit, avec perte d'hydrure, on peut parler de substitution nucléophile.
a) Ajout d'organométalliques
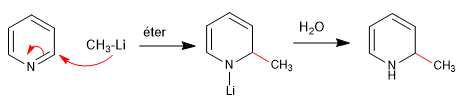
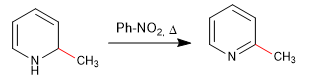
La réaromatisation du cycle est possible en ajoutant un oxydant qui élimine "H 2 "
b) Ajout d'amide. La réaction de Chichibabin
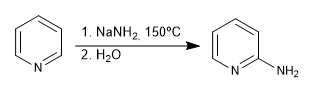
Mécanisme:
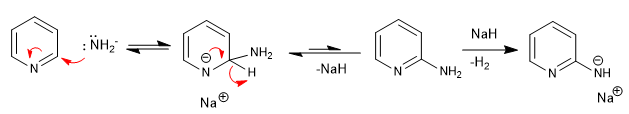
L'amide de sodium formé est protoné dans l'étape finale du traitement aqueux.
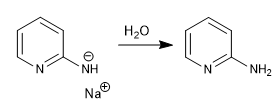
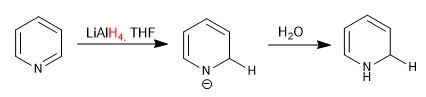
c) Ajout d'hydrures
L'hydrure de lithium et d'aluminium ajoute des hydrures à la position 2 de la pyridine.
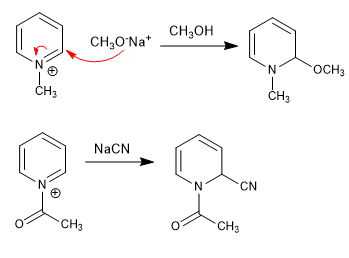
Les nucléophiles les plus faibles (cyanure, hydroxyde, méthoxyde) n'attaquent pas la position 2 de la pyridine, mais réagissent sur les sels de pyridinium, grâce à la plus grande polarité de la position 2.