ОРГАНИЧЕСКИЙ СИНТЕЗ
- Информация о материале
- Wilbertrivera
- ОРГАНИЧЕСКИЙ СИНТЕЗ
- Просмотров: 25226
СИНТЕЗ ГЕТЕРОЦИКЛОВ МЕТОДОМ ВНУТРИМОЛЕКУЛЯРНОГО ЦИКЛИРОВАНИЯ
Построение гетероциклических систем также использует те же самые реакции, с тем отличием, что гетероциклическая система должна присутствовать или содержать по крайней мере один атом, отличный от углерода. Наиболее распространены азот, кислород, сера и фосфор.
Циклическая система синтезируемой молекулы может происходить в результате модификации циклической системы, присутствующей в одном из реагентов, участвующих в синтезе, или быть результатом циклизации нециклических предшественников, которая была построена в ходе развития синтеза. внутримолекулярной циклизацией или методами, основанными на межмолекулярной циклизации (циклоприсоединения).
1. Внутримолекулярная циклизация
Общие закономерности разъединения гетероциклов, возникающих в результате внутримолекулярной циклизации, были адекватно систематизированы Дж. И. Боррелем. , те же, что и в этом разделе (Het = N, O, S)
1.
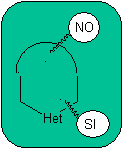
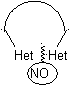
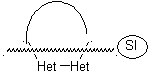
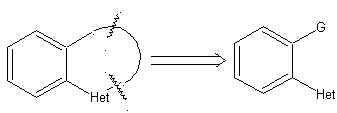
В синтезе моноциклического соединения замыкание кольца обычно включает образование связи углерод-гетероатом.
Модель: |
|
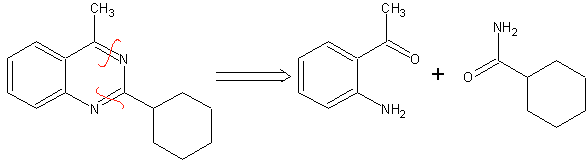
Пример: |
|
|
|
Пример : |
|
Модель: |
|
Пример: |
|
Подробнее: Синтез гетероциклов путем внутримолекулярной циклизации
- Информация о материале
- Wilbertrivera
- ОРГАНИЧЕСКИЙ СИНТЕЗ
- Просмотров: 21266
Моб: 75 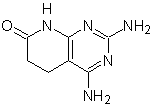 | Моб: 76 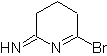 |
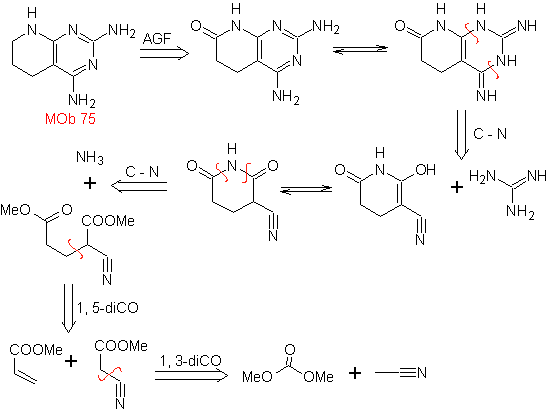
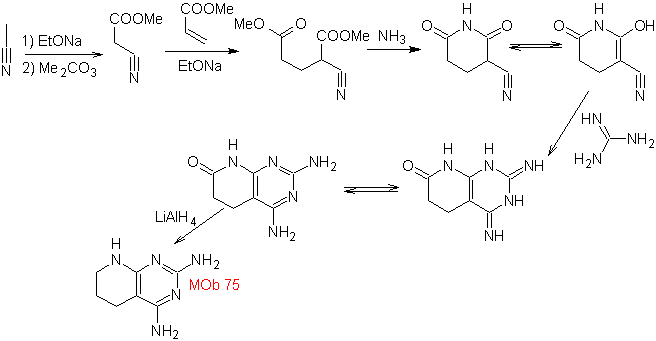
- Информация о материале
- Wilbertrivera
- ОРГАНИЧЕСКИЙ СИНТЕЗ
- Просмотров: 26070
Синтез гетероциклов с несколькими гетероатомами
Гетероциклические соединения, как уже упоминалось, имеют широкий спектр применения: они преобладают среди соединений, используемых в качестве лекарственных средств, агрохимикатов и для ветеринарии; их используют как полировальные добавки, антиоксиданты, ингибиторы коррозии, как красители и пигменты; и во многих других приложениях.
Поэтому вполне естественно, что в настоящее время большая часть исследований в области химии связана с синтезом и свойствами гетероциклических соединений. С этой целью и ориентирована данная статья, целью которой является предоставление студентам-химикам основных инструментов ретросинтеза.
Процесс разрыва для молекул с несколькими гетероатомами может осуществляться для каждой углерод-гетероатомной связи по ранее изученным моделям или одновременно, для чего используются доступные полигетероатомные реагенты.
1. Расстояние гетероатомы (1, 2)
Наиболее представительными и обычными реагентами являются гидразины и замещенные гидразины, а также гидроксиламины.
гидразин |
гидроксиламин |
Предложите схему синтеза из простых материалов следующих молекул:
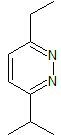
моб 77
пиразолы | Моб 78
изоксазолы | МОБ 79
пиридазины |
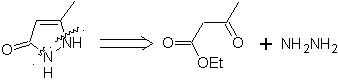
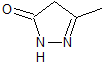
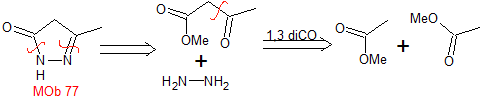
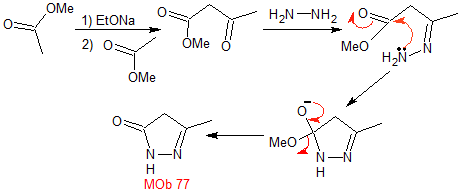
МОБ 77 . Ретросинтетический анализ. MOb является производным пиразола и напрямую разъединяется связями CN с образованием простых предшественников, таких как гидразин и соединение 1,3-диСО.
|
синтез . Метилацетат является хорошим предшественником для образования соединения 1,3-диСО, которое в сочетании с гидразином образует MOb 77. |
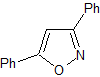
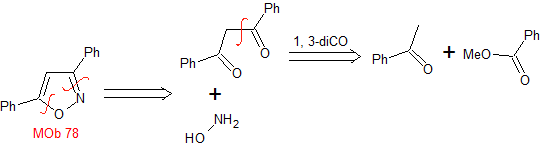
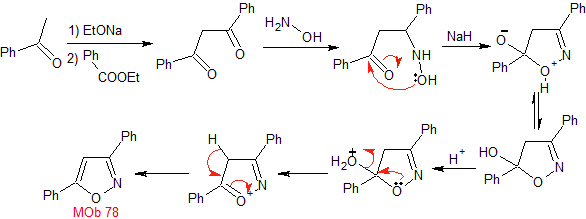
MOb 78- Ретросинтетический анализ .
|
Синтез. Безофенон и этилбензоат позволяют образовать необходимый 1,3-диСО, реагировать в слабокислой среде с гидроксиламином и после добавления NaH происходит циклизация, для чего требуется больше кислоты для
обезвоживать и, наконец, производить
|
- Информация о материале
- Wilbertrivera
- ОРГАНИЧЕСКИЙ СИНТЕЗ
- Просмотров: 20316
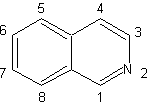
Синтез изохинолина
(методом разъединений)
| Изохинолины структурно отличаются от хинолинов положением азот, так как последний не расплавляется, поэтому он обладает «алифатической реакционной способностью». Он не встречается в природе в свободном виде, но изохинолиновый цикл встречается в некоторых алкалоидах в ароматической или восстановленной форме, например в папаверине. |
Наиболее известные синтетические методы получения изохинолинов начинаются с 2-фенилэтиламинов и включают циклизацию за счет дополнительного углерода, обеспечиваемого карбонильной группой другого соединения.
Основными синтетическими методами являются: синтез Померанца-Фрича, синтез Бишлера-Напиральского, синтез Пикте-Гамса и синтез Пикте-Шпенглера.
1. Синтез POMERANZ-FRITSCH.
Этот метод синтеза изохинолина происходит в две стадии:
к.
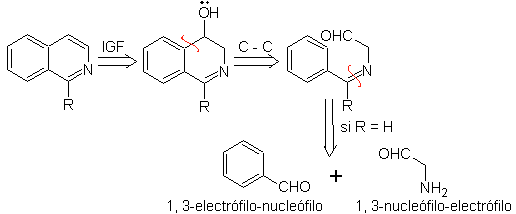
Сначала бензальдегид (1,3-электрофил-нуклеофил) конденсируют с диэтилацеталем аминоацетальдегида (1,3-нуклеофил-электрофил) с образованием стабильного альдимина.
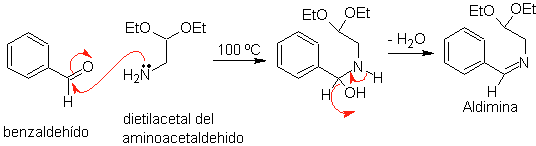
б.
Впоследствии альдимин циклизуется в сильнокислой среде в имин с одновременным удалением этанола с образованием изохинолина.
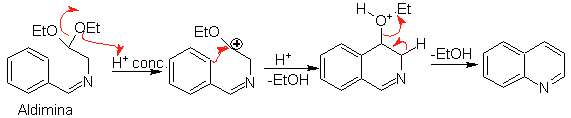
Эта вторая стадия, представляющая собой электрофильное замещение, подвержена влиянию электронодонорных или акцепторных заместителей на бензольное кольцо в указанной реакции. Однако из-за гидролиза образующегося имина в сильнокислой среде, используемой в реакции, снижается выход процесса.
Этот метод позволяет получить доступ к C-1-замещенным изохинолинам, для которых были протестированы ароматические кетоны, с очень низкими выходами. Однако был достигнут больший успех при использовании варианта соответствующим образом замещенных бензиламинов в качестве 1,4-динуклеофилов и диэтилацеталя глиоксаля в качестве 1,2-диэлектрофилов.
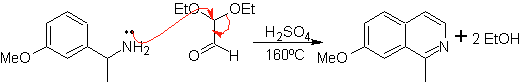
Следует уточнить, что метод Померанца-Фрича и его вариант, проанализированные ранее, не позволяют получать изохинолины, замещенные в положениях С-3 и С-4 гетероатома. Ретросинтетический анализ этого метода показывает возможные промежуточные продукты, участвующие в реакции, и вероятные исходные материалы.
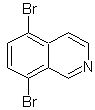
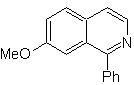
Предложите схему синтеза каждого из следующих изохинолинов: | МОБ 107
| МОБ 108
|
- Информация о материале
- Wilbertrivera
- ОРГАНИЧЕСКИЙ СИНТЕЗ
- Просмотров: 16751
Синтез БЕНЗОДИАЗИНОВ
(методом разъединений)
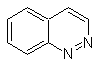
Структуры бензодиазинов находятся в многие алкалоиды, в основном в виде кольцевой системы хиназолона. Другие производные бензодиазина, такие как циннолины, хиноксалины и фтализины, также являются важной частью многих лекарственных средств с широким спектром применения, что делает их в целом очень важными в органическом синтезе и особенно в фармакохимии. Таким образом, они могут быть обнаружены как противовоспалительные, антигипертензивные, антибактериальные, обезболивающие, антибиотики и т. д.
циннолин |
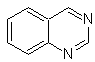
хиназолин | |
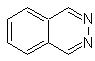
фтализин |
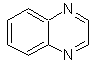
хиноксалин |
Синтез циннолинов
По строению, которое представляет циннолин, возможны следующие варианты его синтеза:
![]() синтез фон Рихтера:
синтез фон Рихтера:
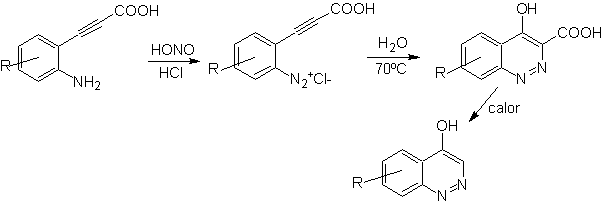
![]() Синтез Видмана – Штёрмера:
Синтез Видмана – Штёрмера:
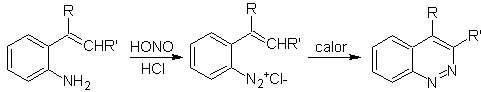
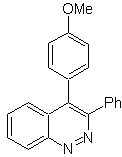
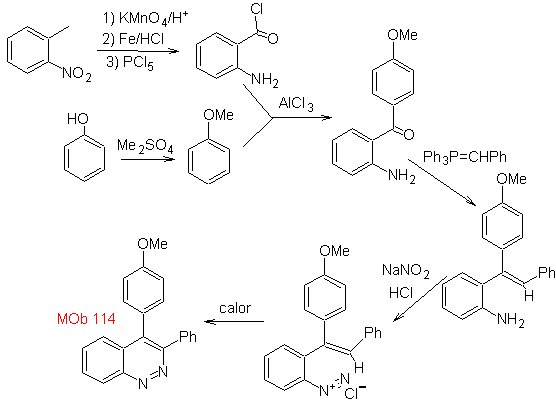
Предложите схему синтеза следующей молекулы : | МОБ 114
|
МОБ 114 . Ретросинтетический анализ.
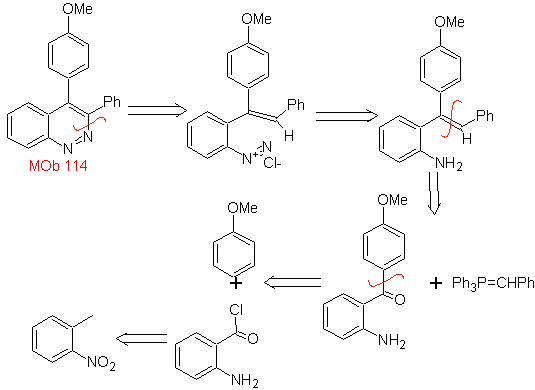
Синтез Образование
- Информация о материале
- Wilbertrivera
- ОРГАНИЧЕСКИЙ СИНТЕЗ
- Просмотров: 64254
Синтез ИНДОЛОВ
(методом разъединений)
Индольная кольцевая система была обнаружена во многих природных соединениях, представляющих большой химический и биохимический интерес, поэтому считается, что она наиболее распространена в природе. Так, триптофан — незаменимая аминокислота, индиго — краситель, а индолил-3-уксусная кислота — гормон роста растений. С другой стороны, интерес к этим молекулам возникает из-за их фармакологического применения, например, суматриптана (антимигренозного средства) и фроватриптана, также антимигренозного средства.
Индол — бесцветное кристаллическое вещество с т.пл. 52°С, легко растворимое в большинстве органических растворителей, кристаллизуется из воды, имеет приятный запах и поэтому также используется в качестве парфюмерной основы.
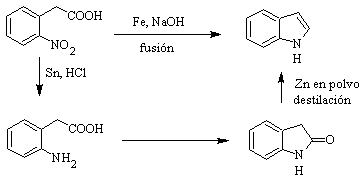
Впервые он был получен в 1866 году путем нагревания оксиндола с цинковой пылью и стал важным коммерческим продуктом. Байер в 1869 году предложил следующий синтез:
Классическими методами синтеза индолов являются методы Фишера, Бишлера, Рейссерта и Леймгрубер-Батчо, Бартоли, Ларок, Гассман, Сугасава, Фукуяма, Хегедус и Доббс.
1.
синтез Фишера
Он заключается в нагревании фенилгидразонов кетонов или альдегидов с безводным хлоридом цинка, трехфтористым бором, полифосфорной кислотой или каким-либо другим кислотным катализатором с получением индолов. Катализируемая кислотой перегруппировка фенилгидразона происходит с отщеплением воды и NH 3 . Электродонорные группы способствуют циклизации, а электроаттракторы препятствуют ей.
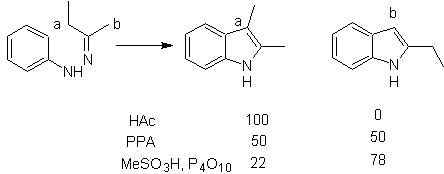
В случае асимметричных кетонов внутримолекулярная циклизация гидразона может приводить к двум изомерным индолам в различных соотношениях в зависимости от используемых условий, в сильнокислых средах может преобладать менее замещенный индол.
При наличии метазаместителей по отношению к азоту гидразона циклизация может происходить в двух положениях, что приводит к двум изомерным индолам:
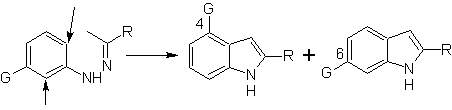
Если заместитель G электроакцепторный, то два изомера (4- и 6-) образуются примерно в одинаковой пропорции. С другой стороны, если G является электронодонорным заместителем, то в основном образуется 6-замещенный изомер.Ретросинтетический анализ индола, образующегося в результате синтеза Фишера, можно рассматривать следующим образом:
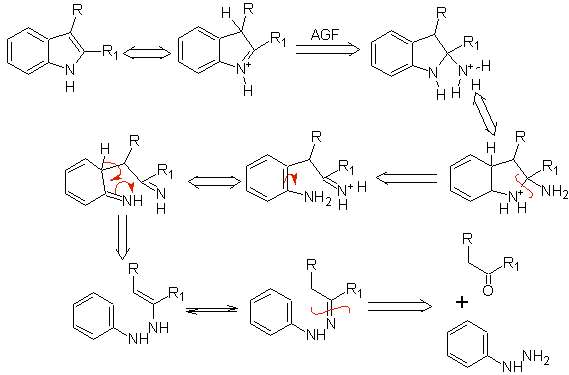
Предложите схему синтеза следующих молекул: | МОБ 119
| МОБ 120
|
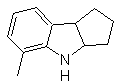
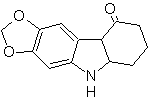
MOb 119. Ретросинтетический анализ. Фундаментальное разъединение индолов, которые, как предполагается, образуются в результате синтеза Фишера, соответствует ретротранспозиции, которая проявляется в разъединении
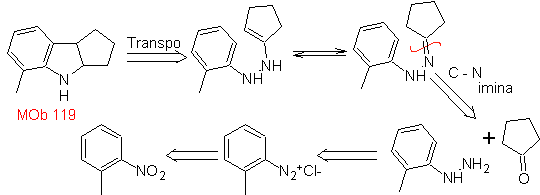
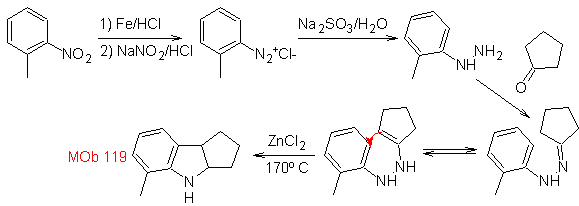
Синтез : из орто-нитротолуола образуется промежуточное производное фенилгидразина, необходимое для синтеза индолов Фишера, имин образуется с циклопентаноном, а при нагревании
- Информация о материале
- Wilbertrivera
- ОРГАНИЧЕСКИЙ СИНТЕЗ
- Просмотров: 21909
Синтез
Бензофураны и бензотиофены
(методом разъединений)
1. Синтез бензофуранов
Бензофуран, обычно называемый кумароном, Это бесцветная жидкость, выделенная из каменноугольной смолы и гораздо более устойчивая к химическому воздействию, чем фуран.
Будут упомянуты и разработаны наиболее классические синтезы для получения бензофуранов:
к. Из кумарина
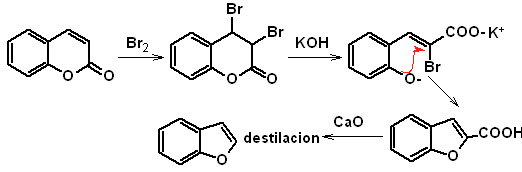
б. Из внутренней реакции конденсации Кляйзена
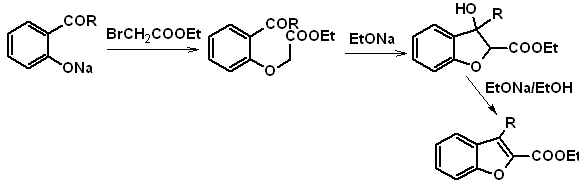
в.
Начиная перестановки Клайзена
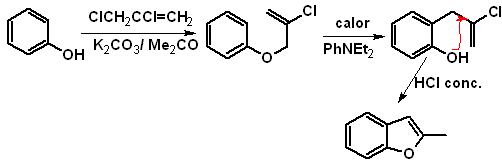
Предложите схему синтеза следующих бензофуранов:
: | МОБ 127
| … | МОБ 128
|
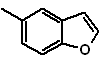
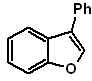
MOb 127, Ретросинтетический анализ. Стратегия разъединения, в
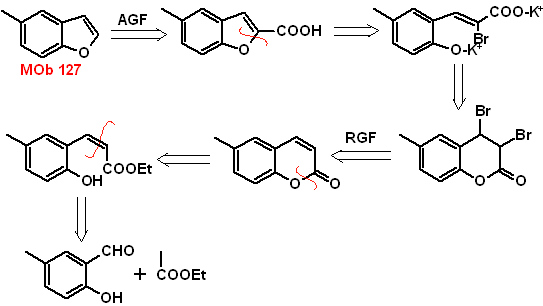
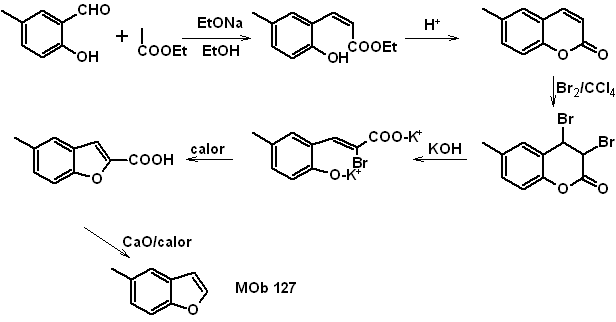
Синтез. Промежуточный 2-гидрокси-5-метилбензальдегид получают из бензола. Образовавшееся производное кумарина галогенируют, гидролизуют в золе KOH и затем нагревают с CaO для декарбоксилирования и, таким образом, образуют
- Информация о материале
- Wilbertrivera
- ОРГАНИЧЕСКИЙ СИНТЕЗ
- Просмотров: 48422
СИНТЕЗ СУЛЬФАМИДОВ
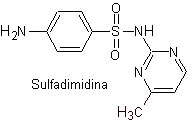
Известно, что сульфаниламиды были первыми противомикробными препаратами, которые применялись системно. Его химическая структура представляет собой бензольное ядро с аминогруппами, которые придают ему активность. Аминогруппа ацетилируется в печени, инактивируя ее. В зависимости от заместителя в указанном секторе лекарство более активно.
Учитывая его сходство с парааминобензойной кислотой, он ведет себя как конкурентный ингибитор этого вещества, которое необходимо вместе с дигидроптеридином для синтеза дигидрофолиевой кислоты, промежуточного соединения в пути синтеза фолиевой кислоты.
В отличие от более продвинутых организмов, бактериям необходимо синтезировать собственные фолаты [они не приобретают их из окружающей среды], поэтому сульфаниламиды, угнетая этот процесс, угнетают процессы синтеза нуклеиновых кислот и являются БАКТЕРИОСТАТИЧЕСКИМИ.
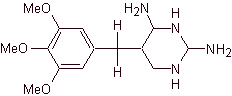
ТРИМЕТРОПРИМ
Триметоприм является производным 2,4-диаминопиримидинов, таких как | Это соединение ИНГИБИРУЕТ фермент дигидрофолатредуктазу и препятствует образованию тетрагидрофолиевой кислоты, то есть действуют по тому же метаболическому пути, что и сульфаниламиды, но в последующей ферментативной реакции. Триметоприм никогда не используется сам по себе, но в сочетании с сульфаниламидами они потенцируются таким образом, что становятся БАКТЕРИЦИДНЫМИ, снижают возможность возникновения резистентности и увеличивают спектр антимикробного действия. Связь между сульфаметоксазолом и триметопримом зафиксирована: 1:5. Например, коммерческие препараты Котримоксазол [форте или нет] поставляются с этой целью. |
сульфаниламиды, обычно их классифицируют по продолжительности действия и способу применения препарата, а также по другим характеристикам. В зависимости от механизма действия сульфаниламиды бывают:
к)
Сульфаниламиды короткого или среднего действия.
к. Сульфонамиды общего назначения
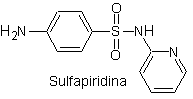
Эй. сульфатиазол
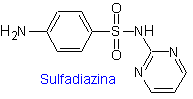
II. сульфадиазин
III. сульфадимидин
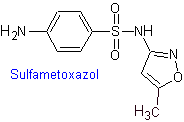
IV. Сульфаметоксазол (отдельно или в комбинации с триметопримом: котримоксазол)
б. Хорошо растворимые соединения первоначально применялись при лечении инфекций мочевыводящих путей.
Эй. сульфизоксазол
II. сульфаметизол
III. сульфазомидин
б)
Сульфаниламиды длительного действия.
IV. сульфаметоксипиридазин
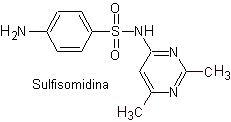
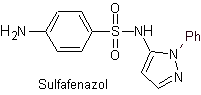
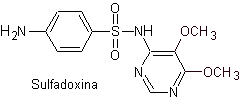
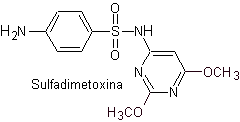
в. сульфадиметоксин
пила. сульфадоксин
в)
Сульфаниламиды ограничены желудочно-кишечным трактом
vii. сульфагуанидин
VIII. сульфаталидин
икс. сульфасуксидин
Икс. Сульфазолазин
г) Местные сульфаниламиды.
xi. мафенида ацетат
xii. сульфадиазин серебра
xiii. сульфацетамид натрия
Основные сульфаты:
| ……… |
|
|
|
| …….. |
|
|
|
- Информация о материале
- Wilbertrivera
- ОРГАНИЧЕСКИЙ СИНТЕЗ
- Просмотров: 25023
Синтез фторхинолоновых антибиотиков
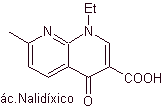
Хинолоны относятся к группе синтетических антибактериальных средств. Самый старый агент в этом семействе, налидиксовая кислота, применявшаяся в начале 1960-х годов, имеет хороший спектр против энтеробактерий (ограниченный антибактериальный спектр), но ее фармакокинетика не очень благоприятна для рутинного клинического применения из-за ее низкой биодоступности в тканях и ее короткой половины. -жизнь.
По этой причине необходимо было синтезировать новые антибактериальные препараты этого семейства для улучшения спектра действия, фармакокинетического профиля, снижения побочных эффектов и появления бактериальной резистентности. Эта новая группа представляет собой так называемые фторхинолоны, созданные в 80-х годах.
|
Многие исследователи сходятся во мнении, что реакция Гулда-Джейкобса , является основной основой для синтеза первых хинолонов для фармакологического применения, который произошел в 1960-х годах, эта реакция представляет собой следующую последовательность:
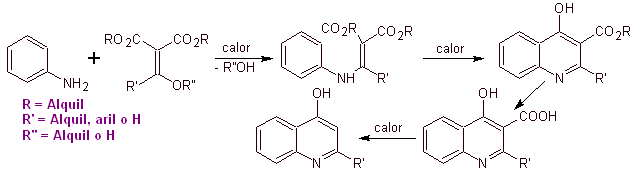
В последующие годы фтор в положении 6 и различные группы гетероциклов в положении 7 были введены в основное кольцо бензохинолонов, что привело к появлению фторхинолонов с более широким антибактериальным спектром.
Важные части методологий, используемых в этих синтезах, были собраны Лейвой С. и Лейвой Э. в очень хорошей работе с биохимической точки зрения.
Метод отключения, примененный к отчету об изучаемых синтезах, и реакции первых стадий синтезов являются исключительной ответственностью автора этой монографии. .
i) Синтез, описанный Koga H. et al.
Ретросинтетический анализ:
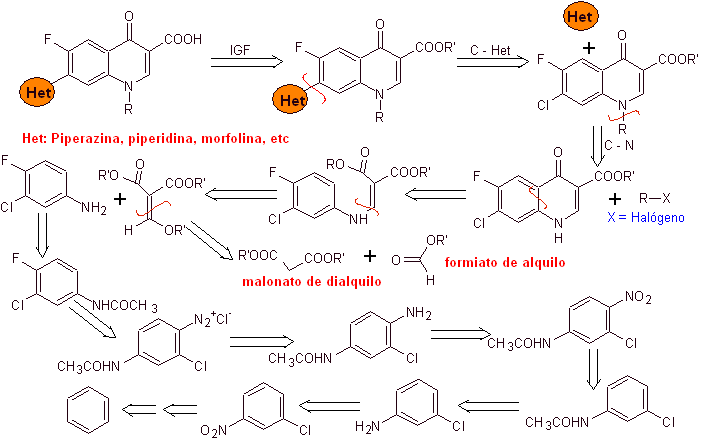
Синтез: Начинается с бензола с образованием 3-хлор-4-фторанилина, который реагирует с диэтиловым ЭММЕ с образованием соответствующего акрилата, который при нагревании образует циклическое соединение. Это соединение, в свою очередь, вводят в реакцию с алкилирующим агентом, а затем вводят азотсодержащее гетероциклическое соединение для окончательного гидролиза и получения целевой молекулы.
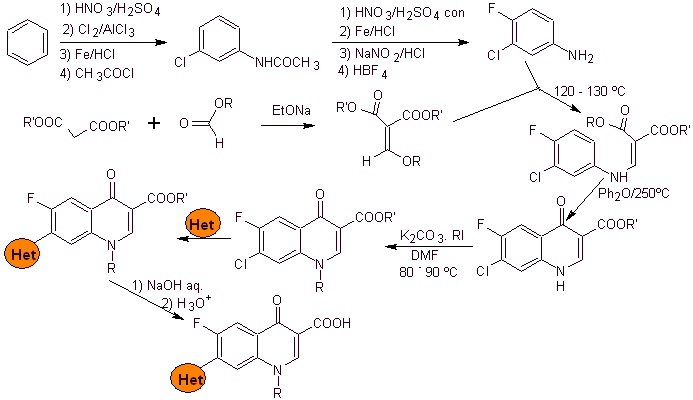
- Информация о материале
- Wilbertrivera
- ОРГАНИЧЕСКИЙ СИНТЕЗ
- Просмотров: 37176
Синтез местных анестетиков на основе бензойной кислоты
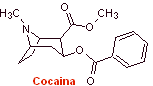
Свойства алкалоидов, выделенных из листьев растения коки, были впервые открыты Гедише в 1855 году, очистка и выделение активного начала, называемого кокаином, Альбертом Ниманом в 1860 году, практически положили начало истории местных анестетиков. Впоследствии Эйнхорн в 1904 году ввел новокаин (новокаин) в качестве местного анестетика в медицину. |
|
С тех пор человечество стало свидетелем непрерывного и устойчивого развития синтеза новых молекул с анестезирующими активными ингредиентами:
![]() В 1925 году Нишер синтезировал нуперкаин.
В 1925 году Нишер синтезировал нуперкаин.
![]() В 1928 году фон Эйслеб тетракаин (пантокаин) и
В 1928 году фон Эйслеб тетракаин (пантокаин) и
![]() В 1946 году Лофгрен и Лундквист синтезировали логникаин (ксилокаин или лидокаин).
В 1946 году Лофгрен и Лундквист синтезировали логникаин (ксилокаин или лидокаин).
![]() Затем в 1954 году Аф Экенштам и Эгнер получили синтез мепивакаина (скандикаина).
Затем в 1954 году Аф Экенштам и Эгнер получили синтез мепивакаина (скандикаина).
![]() Позже, в 1960 и 1964 годах, они были введены в
Позже, в 1960 и 1964 годах, они были введены в
![]() Наконец, в последующие годы в медицину стали внедрять новые анестетики.
Наконец, в последующие годы в медицину стали внедрять новые анестетики.
Местные анестетики – это препараты, которые при нанесении на определенный участок тела вызывают временную и обратимую потерю чувствительности (тепловой, болевой и тактильной), без угнетения сознания больного. Длительность действия препарата зависит от применяемой дозы, его химической структуры, лекарственной формы и лекарственной формы препарата.
В целом местные анестетики реагируют на различную химическую структуру, но все они имеют схожие эффекты или разную интенсивность анестезирующего действия. Однако можно попытаться сгруппировать их в эфиры бензойной кислоты, эфиры аминобензойной кислоты, амиды и т. д.
1 . Химическая структура местных анестетиков
Местные анестетики являются преимущественно слабыми основаниями и образованы ареновой группой, сложного эфира или амида, придающего молекуле липофильные свойства (которые в основном определяют активность препарата), алифатическую третичную аминогруппу (алкильную или алициклическую), придающую молекуле ее гидрофильный характер, и алкильную промежуточную цепь, соединяющую части арен с амином и отвечает за уровень токсичности препарата.
Таким образом, основные местные анестетики, используемые в различных медицинских дисциплинах, можно найти в следующих группах:
к)
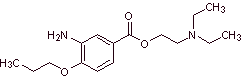
Аминоэфиры бензойной кислоты :
б)
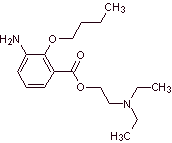
Эфиры м-аминобензойной кислоты :
в)
Эфиры п-аминобензойной кислоты :
г) Амиды:
и)
Кетоны :
Ф)
другие группы
2 . Синтез местных анестетиков на основе аминоэфиров бензойной кислоты
Наиболее представительными препаратами этой группы являются кокаин, гексилкаин, пиперокаин, этиламинобензоат, меприлкаин, амилокаин, циклометикаин и пропанокаин. Эти имена отвечают
Подробнее: Синтез местных анестетиков на основе бензойной кислоты
- Информация о материале
- Wilbertrivera
- ОРГАНИЧЕСКИЙ СИНТЕЗ
- Просмотров: 38268
Синтез местных анестетиков на основе аминобензойной кислоты
Местные анестетики, производные м-аминобензойной кислоты.
Наиболее представительными препаратами этой группы являются
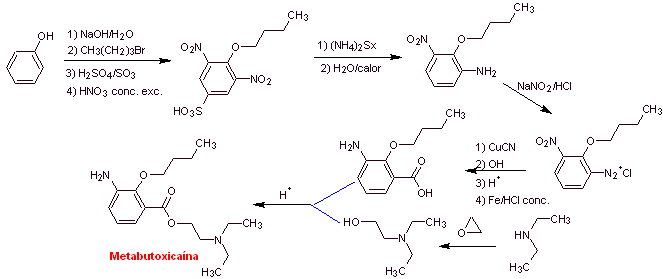
MOb 07: Метабутоксикаин , продаваемый под названием примакаин , является еще одним местным анестетиком , используемым в стоматологии. Предложите схему синтеза этого препарата, исходя из простых и доступных материалов. |
|
Ретросинтетический анализ : при расщеплении ацил-кислорода образуется аминоспирт, расщепляемый до вторичного амина и эпоксида; другой предшественник предлагает получить свою карбоксильную группу путем гидролиза нитрильной группы, которая будет размещена на бензольном кольце по реакции Зандмейера . Селективное восстановление только одной из нитрогрупп проводят полисульфидом аммония или также Na 2 S.
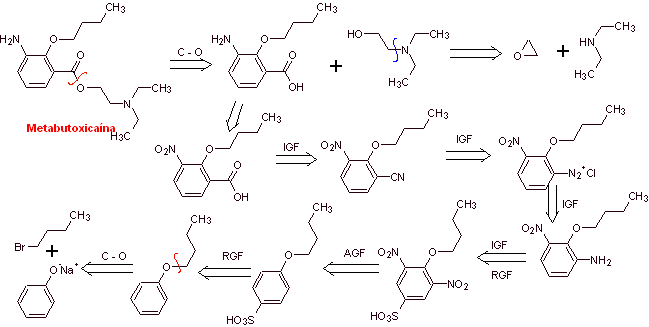
Синтез
MOb 08: Проксиметакаин (МНН) или пропаракаин , известный под торговыми названиями Алкаин, Ак-Таин и др., представляет собой местный анестетик из группы аминоэфиров. Он показан для использования в качестве офтальмологического анестетика для уменьшения боли и дискомфорта в глазах. Предложите схему синтеза этого анестетика, начиная с простых и доступных материалов. |
|
Ретросинтетический анализ : начальное ацил-кислородное отсоединение проксиметакаина снова приводит к м-аминобензойной кислоте с заместителем алкоксида в пара-положении и аминоспирту, который образуется из соответствующего амина и эпоксида.
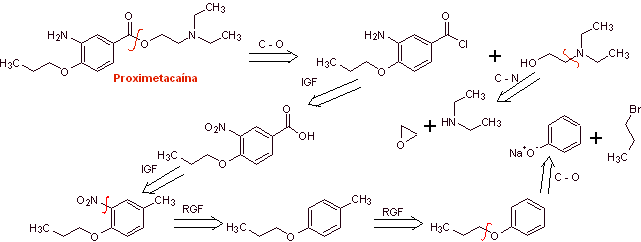
Синтез проксиметакаина :
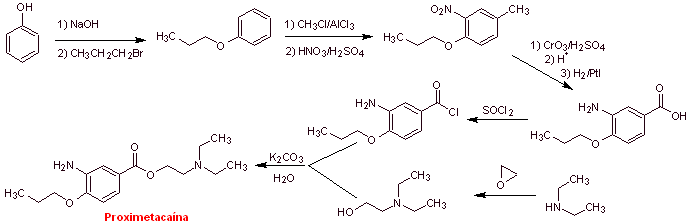
Подробнее: Синтез местных анестетиков на основе аминобензойной кислоты
- Информация о материале
- Wilbertrivera
- ОРГАНИЧЕСКИЙ СИНТЕЗ
- Просмотров: 30278
Синтез местных анестетиков на основе фенилацетамидов.
Представлен перечень основных компонентов этой группы анестетиков. следующий:
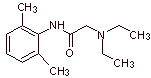
Лидокаин (лигнокаин, ксилокаин), мепивакаин, этидокаин, артикаин (картикаин), бупивакаин, прилокаин, дибукаин (цинкокаин), ропивакаин, тримекаин, бутаниликаин, клибукаин, толикаин, тримекаин, вадокаин или кситазаин , анидикаин, диметизохин, оксетазин, пиррокаин, парамоксин, пропракаин, оксетакаин.
МОБ 19 ; |
|
Ретросинтетический анализ :
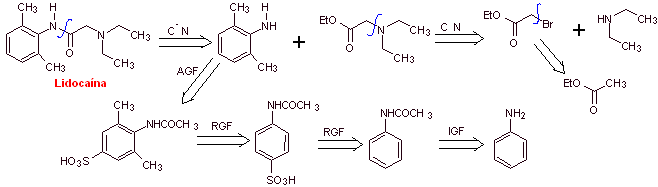
Синтез
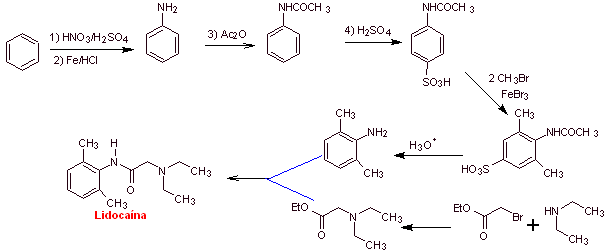
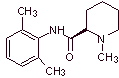
MOb 20: Мепивакаин — местный анестетик амидного типа, действует быстрее, чем новокаин, но его анестезирующее действие короче, чем у новокаина. Как и большинство анестетиков, он поставляется в виде гидрохлоридной соли рацемата. |
|
Ретросинтетический анализ : Первоначальное разъединение амидной связью приводит к образованию двух молекул-предшественников, одна из которых, 2,6-диметиланилин, уже была синтезирована в
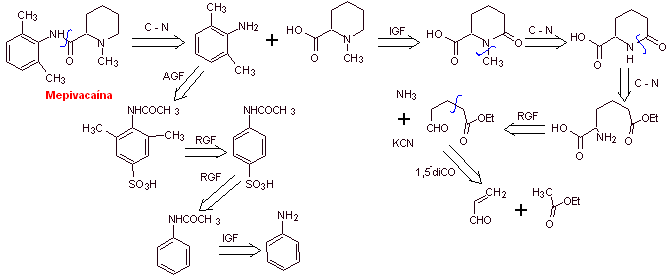
Синтез мепивакаина :
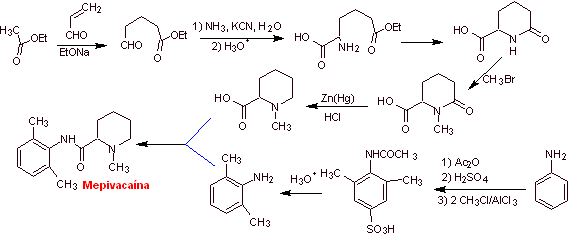
Подробнее: Синтез местных анестетиков на основе фенилацетамидов
- Информация о материале
- Wilbertrivera
- ОРГАНИЧЕСКИЙ СИНТЕЗ
- Просмотров: 18678
Синтез местных анестетиков производных различных функциональных групп
Существуют анальгетики, которые, будучи производными от функциональных групп, отличных от бензойной кислоты, аминобензойной кислоты или фенилацетамида, также обладают обезболивающими свойствами, аналогичными ранее синтезированным лекарствам. Наиболее представительными в этой группе являются следующие:
Фенакаин, промокаин (прамоксин), букрикаин, этилхлорид, диметизохин, диперодон , кетокаин, миртекаин, октакаин, диклонин (диклокаин)
MOb 29 : диклонин — пероральный анестетик в Sucrets, еще одной пастилке от горла. Он также содержится в некоторых разновидностях спрея от боли в горле Cepacol. Предложите синтез препарата. | 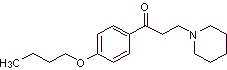 |
Ретросинтетический анализ : структура кетоамина позволяет нам предположить разъединение, связанное с реакцией Манниха (метилкетон + формальдегид + вторичный амин). Последующие разъединения молекул-предшественников связаны с относительно простыми химическими реакциями с высоким выходом.
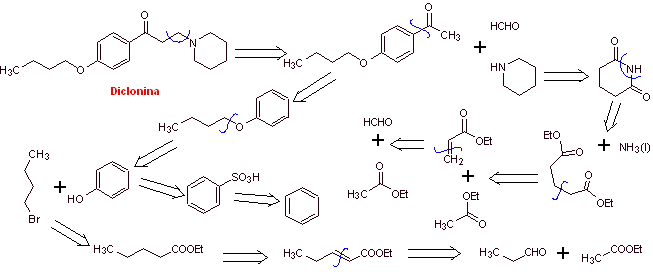
Синтез диклонина :
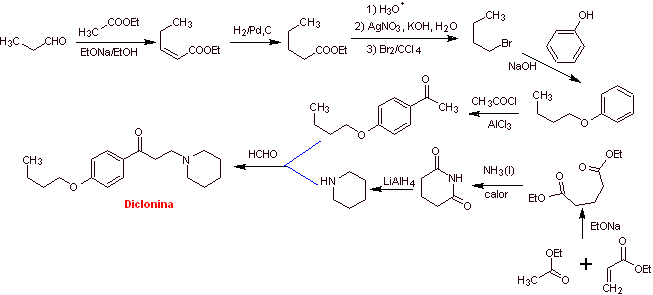
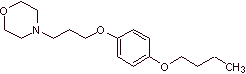
MOb 30 : прамокаин ( также известный как прамоксин) представляет собой местный анестетик, используемый в качестве противозудного средства. Его гидрохлорид растворим в воде и поэтому легче впитывается кожей. Предложите схему синтеза этой молекулы из простых и доступных материалов. |
|
Ретросинтетический анализ :
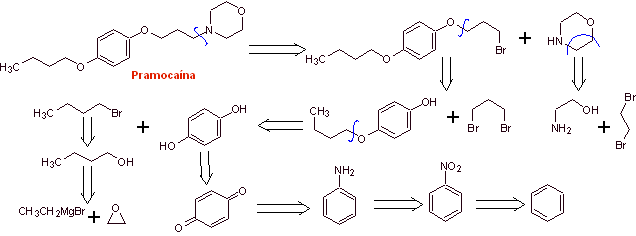
Синтез прамокаина :
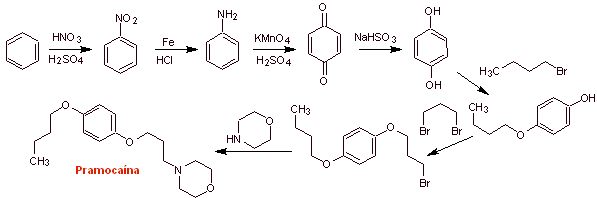
Подробнее: Синтез местных анестетиков производных различных функциональных групп
- Информация о материале
- Wilbertrivera
- ОРГАНИЧЕСКИЙ СИНТЕЗ
- Просмотров: 13643
Синтез полиаспартата (rootGrow)
1. Синтез полиаспартата (rootGrow)
Утверждается, что формула rootGROW связана с формулой нутра-сладкого (аспартама), мощного подсластителя, который снимается или уже был снят с рынка из-за его вредного воздействия на здоровье людей.
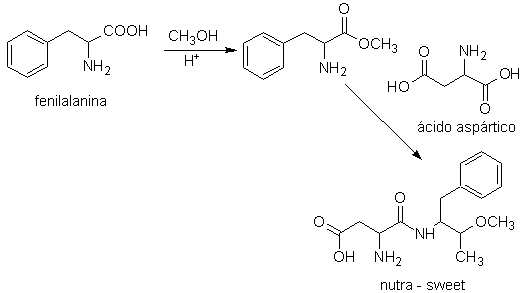
Нутра-сладость можно синтезировать из фенилаланина по следующей схеме:
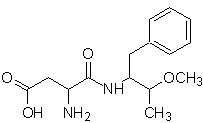
нутра сладкий
В свою очередь, аспарагиновую кислоту, основное основание, для получения корнеплода, который может быть правовращающим (D) или левовращающим (L), получают по следующим схемам синтеза:
Схема A: (процесс трансаминирования)
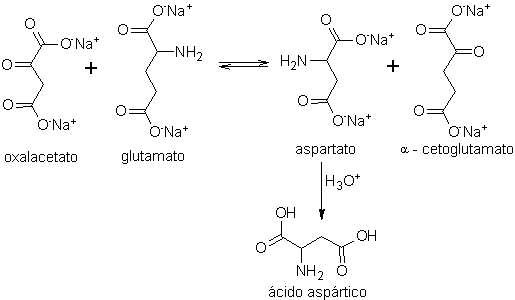
- Информация о материале
- Wilbertrivera
- ОРГАНИЧЕСКИЙ СИНТЕЗ
- Просмотров: 25645
Синтез 1,3- и 1,5-дикарбонильных соединений
Предложите схему синтеза методом разъединения (метод синтона) из простых и доступных материалов, для следующих молекул:
(Помните, что если невозможно предложить прямое отключение, необходимо будет прибегнуть к стратегии предварительной функционализации MOb, пока не будет достигнута применимая модель отключения)
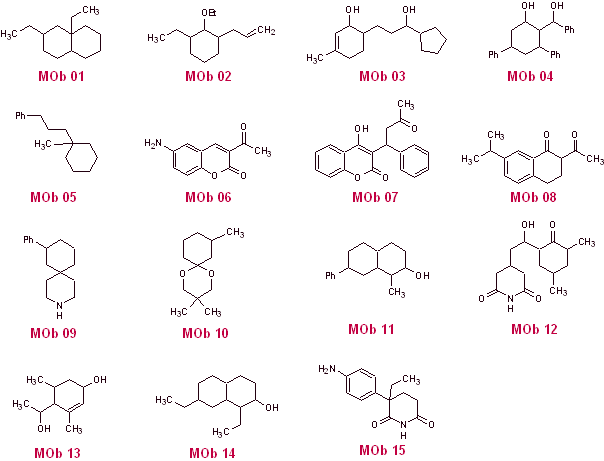
РЕШЕНИЕ ПРЕДЛАГАЕМЫХ ПРОБЛЕМ
MOb 01 не имеет отношения кислорода к кислороду, аспект, который в некотором смысле является преимуществом для химика. То есть используемая стратегия позволит с определенной степенью свободы искать диоксигенированные связи в молекуле предшественника (синтетический эквивалент), то есть можно постулировать, в зависимости от строения МОб, диапазон дикарбонильного и/или гидроксикарбонильные связи, в положениях относительно 1,2, 1,3 , 1,4, 1,5 и/или 1,6 или их варианты, такие как α, β-ненасыщенные карбонильные соединения.
В этом случае синтез будет осуществляться с использованием диоксигенированных соотношений 1,3 и/или 1,5. Таким образом, молекула-мишень и предшественники будут преобразованы в разъединяемые структуры по известному и заранее установленному образцу.
Решение МОБ 01
Ретросинтетический анализ : в рассматриваемой молекуле можно начать с осуществить АГФ, поместив группу С=О в структуру молекулы предшественника, в такое положение, которое позволяет в дальнейшем сделать другой АГФ, с двойной связью, расположенной на альфа- и бета-углероде по отношению к карбонилу, продолжить отключить его.
Ненасыщенность α, β по отношению к C=O следует искать как наиболее замещенный алкен из возможных альтернатив. Наличие заместителя в бета-положении при C=O заставляет нас думать, что он мог присоединяться в качестве нуклеофила к α, β-ненасыщенному карбонильному соединению в соответствии с реакцией сопряженного присоединения Михаэля. Исходя из этих соображений, для MOb 01 можно постулировать следующий ретросинтетический анализ:
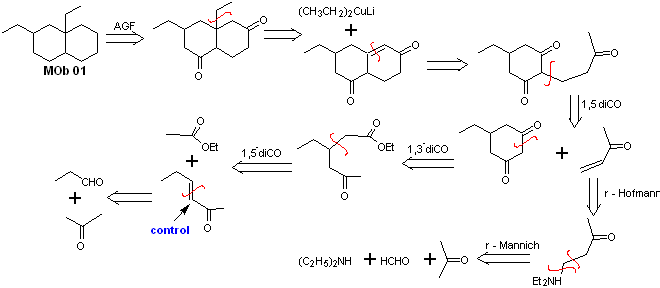
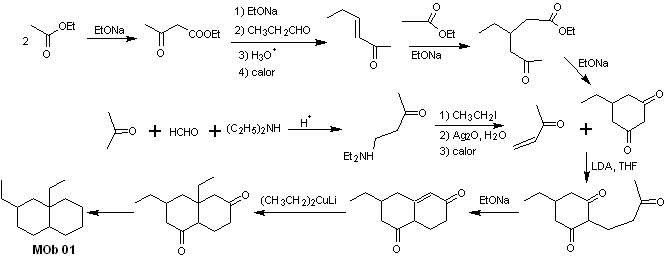
Синтез MOb 01 : Конденсация енолизируемого альдегида и кетона обычно приводит к продуктам самоконденсации или перекрестной конденсации. Этого можно избежать, прибегая к стратегии осуществления контроля, в нуклеофиле кетон, как видно на приложенной схеме.
С другой стороны, когда требуется использовать винилкетоны в качестве субстрата в реакции Михаэля, это будет означать использование формальдегида. К сожалению, этот альдегид, будучи очень реакционноспособным в щелочной среде, имеет тенденцию вызывать реакции полимеризации, которые резко снижают выход синтеза.По этой причине реакция Манниха и отщепление Хофмана адекватно сочетаются для получения винилкетонов с высокими выходами.
Удаление Хофмана можно проводить в той же основной среде, что и для реакции Михаэля, поэтому нет необходимости выделять винилкетон.
Однако из-за все еще ограниченного опыта в синтезе использование оксида серебра в водной среде будет постулировано для достижения удаления амина и образования винилкетона.
- Информация о материале
- Wilbertrivera
- ОРГАНИЧЕСКИЙ СИНТЕЗ
- Просмотров: 43267
синтез фенантрена
(метод дерева синтеза)
Фенантрен — полициклический ароматический углеводород, содержащий три конденсированных бензольных кольца, поэтому он является изомером антрацена.
| или |
|
Традиционные методы синтеза фенантрена, предполагающие образование циклов и их последующую «ароматизацию», связаны с методами, предложенными Хауортом и Бардан-Сенгуптой (1932), как будет видно ниже.
Также можно предложить другие новые методы для фенантрена и вообще для полициклических ароматических соединений, на основе соответствующего использования реакций сочетания Ульмана, реакции Хека, реакции Сузуки и реакции Мак-Мурри, а также варианты и расширения, которые представляют эти реакции.
к) Синтез Хаворта:
Этот метод основан на реакции ацилирования Фриделя-Крафтса и имеет тот недостаток, что окончательная циклизация с образованием третьего кольца, слитого с нафталином, не является селективной, поскольку также возможно, что замыкание происходит в другом углероде, соседнем с группой, содержащей карбоксильную функцию и, таким образом, образует изомер, который из-за условий реакции оказывается меньшинством.
Метод А :
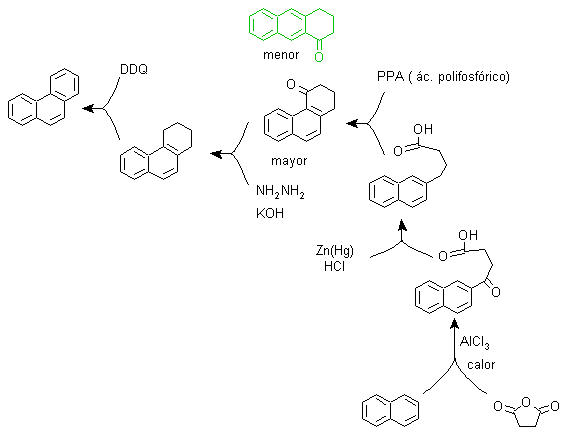
Исходными материалами обычно являются нафталин и янтарный ангидрид. Чтобы реакция ацилирования ангидридом происходила по углероду 2 (бета) нафталина, необходимо проводить реакцию при температуре выше 60 ºC.
При комнатной температуре положением ацилирования будет углерод 1 (альфа), что приводит к варианту метода, который, однако, представляет собой по существу те же самые реакции, которые происходят, и также происходит образование другого изомера, что гораздо менее значимо. чем в первом случае. Поэтому ее предпочтительно использовать в качестве официальной реакции для получения фенантрена по методу Ховорта.
- Информация о материале
- Wilbertrivera
- ОРГАНИЧЕСКИЙ СИНТЕЗ
- Просмотров: 31537
ТОРИН СИНТЕЗ
Аналитическое применение торина, рабочие параметры, его ограничения и перспективы рассматриваются и объясняются достаточно подробно в специализированных публикациях по химическому анализу, таких как Analytical Chemistry . Краткий обзор их показывает следующие приложения:
В кислой среде : используется для количественного определения элементов тория (Th), циркония (Zr), фтора (F), гафния (Hf) и урана (U).
В щелочной среде : Форма дисульфоновой кислоты тора, более известная как Торон, используется для количественного определения лития (Li).
В нейтральной среде : торин используется как индикатор для определения сульфат-ионов (SO 4 2- ) в водных растворах.
Торин также используется для определения SO 2 в воздухе.
Исследовательская проблема.
Учитывая спрос на этот реагент для различных аналитических определений и, в частности, для колориметрического анализа лития в рассолах из Гран-Салар-де-Уюни и малое предложение его на национальном рынке, возникает необходимость синтезировать торин из простых и доступных материалов . в нашей среде.
С этой целью к разработанным маршрутам синтеза подходят из парадигмы РЕТРОСИНТЕЗ , к которым применимы методы Листов Синтеза, Метод Разъединения или Синтона и Метод Дерева. синтеза.
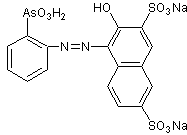
Что касается синтеза торина , то в литературе имеется краткое и обобщенное описание синтеза торона. , согласно предложенному направлению Кузнецовым , т. е. указано, что для получения торона необходимо диазосопопулирование о-аминофениларсоновой кислоты с динатриевой солью 2-наптол-3,6-дисульфокислоты (соль R) в кислая среда.
Синтез дизайна для Thorina .
К дизайну подходит метод отключения или Sintón, который предусматривает два этапа. Первый связан с ретросинтетическим анализом, а второй — с синтезом в направлении того, что происходит в лаборатории, то есть от исходных материалов до достижения молекулы-мишени (МОб).
к) Предметы структурную и реакционную способность, которые необходимо учитывать для ретросинтетического анализа
Торин обычно представляет собой азосоединение, поэтому является красителем. Получение этих соединений обычно включает две основные реакции: диазоирование и диазосочетание (или просто связывание).
С другой стороны, все молекулы-предшественники сочетания, используемые для образования азокрасителей, имеют общий характер, а именно: активный атом водорода, связанный с атомом углерода.
В качестве молекул-предшественников (субстратов) для связывания широко используются следующие соединения: соединения с фенольными гидроксилами, такие как фенолы и нафтолы, ароматические амины, молекулы с енолизуемыми алифатическими кетоновыми группами и гетероциклические молекулы, такие как пиррол, индол и т. д.
В отношении реакции копуляции необходимо учитывать некоторые эвристические принципы, а именно:
· Фенолы связываются легче, чем амины, а члены нафталинового ряда легче, чем бензол.
· Заместители с отрицательным индуктивным эффектом (-I), такие как галогены, нитро, сульфамидные, карбоксильные и карбонильные группы, замедляют связывание.
· Алкильная или алкоксигруппа в орто- или метаположении по отношению к аминогруппе способствует связыванию. А если они находятся в положениях 2 и 5 по отношению к аминогруппе, они являются особенно хорошими связующими.
· В бензольном ряду связывание обычно происходит в пара- положении по отношению к гидроксильной (-ОН) или аминогруппе (-NH 2 ). Если позиция for занята, связь происходит в орто-позиции.
· В ряду нафталина, когда аминогидроксильная группа находится в положении 2 ( б ), реагент связан в положении 1 ( а ). Если гидроксильная или аминогруппа находится в альфа-положении, связь обычно возникает в 4-м положении; но если положение 3 или 6 занято сульфогруппой, то соединение происходит в бета-положении.
· Когда есть два возможных положения связывания, положение связи часто определяется рН среды: связывание происходит в орто-положении к аминогруппе, когда оно осуществляется в кислой среде, и в орто- положении к гидроксильной группе, когда оно осуществляется в кислой среде. осуществляется в основной среде.
- Информация о материале
- Wilbertrivera
- ОРГАНИЧЕСКИЙ СИНТЕЗ
- Просмотров: 58408
СИНТЕЗ БЕНЗОДИАЗЕПИНОВ (БДЗ)
К. Уилберт Ривера Муньос
Адрес электронной почты защищен от спам-ботов. Для просмотра адреса в вашем браузере должен быть включен Javascript.
Эти вещества производят самые разнообразные