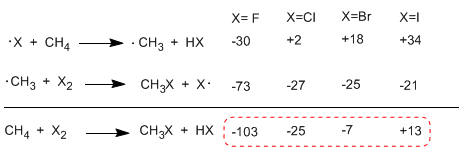Beim Vergleich der Enthalpien der Ausbreitungsstufen der verschiedenen Halogene werden wichtige Unterschiede in der ausgetauschten Wärme beobachtet. Im Fall von Fluor sind beide Schritte exotherm (sogar die Abstraktion von Wasserstoff) mit einer globalen Energiebilanz von -103 Kcal/mol. Die Aktivierungsenergien der Übergangszustände in dieser Reaktion sind sehr niedrig, was es zum reaktivsten Halogen macht.
Das andere Extrem der Reaktivität ist Jod, dessen Reaktion endotherm ist und nicht stattfindet.
Reaktivitätsreihenfolge F 2>Cl 2> Br 2> I 2
Die folgende Tabelle zeigt den Wärmeaustausch in den Ausbreitungsstufen für die Halogenierung von Methan.
Die Reaktion ist im Falle von Fluor (Halogen reaktiver) stark exotherm, während sie im Falle von Jod bei 13 Kcal/mol endotherm ist.