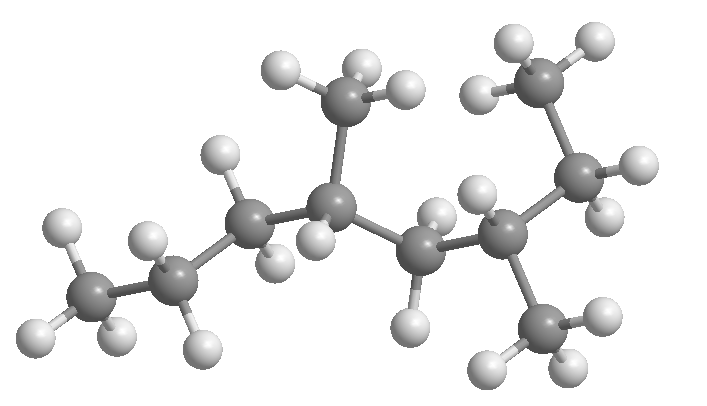
Was sind Alkane?
Alkane sind ausschließlich aus Kohlenstoff und Wasserstoff gebildete Verbindungen (Kohlenwasserstoffe), die nur einfache Kohlenstoff-Kohlenstoff-Bindungen enthalten.
Arten von Alkanen
Alkane werden in lineare, verzweigte, zyklische und polyzyklische Alkane eingeteilt.
Nomenklatur der Alkane
Alkane werden mit der Endung -ane benannt, dem Präfix, das die Anzahl der Kohlenstoffe im Molekül angibt (Methan, Ethan, Propan...)
Physikalische Eigenschaften von Alkanen
Die Schmelz- und Siedepunkte von Alkanen sind niedrig und steigen mit zunehmender Anzahl von Kohlenstoffen aufgrund von Wechselwirkungen zwischen Molekülen durch London-Kräfte. Lineare Alkane haben höhere Siedepunkte als ihre verzweigten Isomere.
Konformationsisomere
Alkane sind aufgrund des Spins um die CC-Bindung nicht starr. Die durch diese Rotationen erzeugten multiplen Formen werden Konformationen genannt.
Newman-Projektion
Die Energie der verschiedenen Konformationen ist in den Newman-Projektionen zu sehen. Daher ist im Fall von Ethan die verfinsterte Konformation aufgrund der Abstoßungen zwischen Wasserstoffatomen diejenige mit der höchsten Energie.
Potentialdiagramme
Die verschiedenen Konformationen von Alkanen können in einem Potentialenergiediagramm dargestellt werden, in dem wir sehen können, welche Konformation stabiler ist (minimale Energie) und welche Energie benötigt wird, um von einer Konformation in eine andere überzugehen.
Verbrennung von Alkanen
Aufgrund ihrer geringen Reaktivität werden Alkane auch als Paraffine bezeichnet. Die wichtigsten Reaktionen dieser Verbindungsgruppe sind radikalische Halogenierungen und Verbrennungen. Verbrennung ist die Kombination von Kohlenwasserstoff mit Sauerstoff, um Kohlendioxid und Wasser zu bilden.