Les sucres en solution se trouvent le plus souvent sous une forme cyclique, appelée hémiacétal. L'hémiacétal est obtenu en attaquant l'un des groupements hydroxyle de la chaîne sur le carbonyle. Les cycles formés sont de cinq ou six membres.
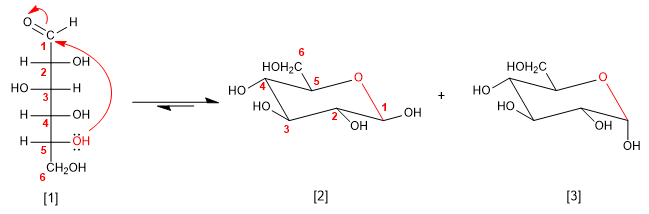
[1 ] D-Glucose
[2] b -D-Glucopyranose
[3] a -D-Glucopyranose
Pour dessiner l'hémiacétal, nous plaçons les -OH qui sont à droite dans la projection de Fischer vers le bas dans la chaise, tandis que ceux de gauche sont orientés vers le haut.
Le -OH en position 1 (-OH attaché au carbone anomérique) peut prendre deux orientations qui donnent naissance à des anomères alpha (-OH down) et bêta (-OH up). Par contre, le -CH 2 OH qui part du carbone 5 sera orienté vers le haut dans les sucres de la série D, alors qu'il sera orienté vers le bas dans les L.
Le glucose peut également se cycliser en 5 cycles (furanose), par attaque de l'hydroxyle en position 4 sur le carbonyle.
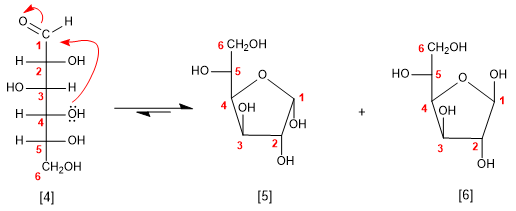
[4 ] D-Glucose
[5] a -D-Glucofuranose
[6] b -D-Glucofuranose
Bien que la forme hémiacétal soit prédominante dans le milieu aqueux, elle existe en équilibre avec une petite fraction de molécules ouvertes. Ainsi, les réactions qui agissent sur le groupement carbonyle (oxydations ou réductions) éliminent la forme ouverte du milieu, provoquant le déplacement de l'équilibre vers la gauche, produisant l'ouverture des hémiacétals.
La forme pyranose est plus stable que le furanose dans le cas du glucose
En suivant les règles indiquées ci-dessus, nous allons cycler la molécule d'arabinose. L'attaque de l'hydroxyle en position 4 génère un hémiacétal à 5 chaînons (furanose).
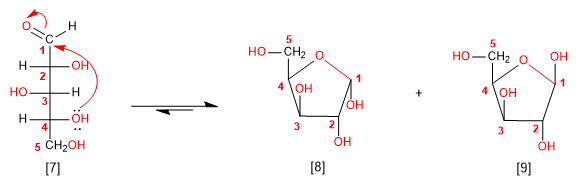
[7] D-arabinose
[8] a -D-arabinofuranose
[9] b -D-arabinofuranose
On peut également cycliser l'arabinose à partir de l'hydroxyle en position 5, générant des cycles à 6 chaînons (pyranose)
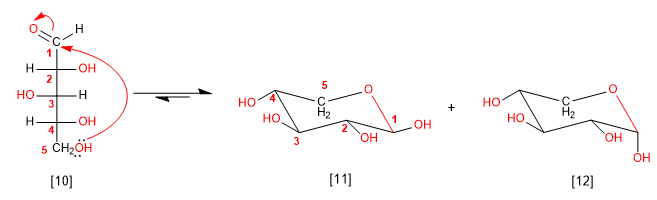
[10] D-arabinose
[11] b -D-Arabinopyranose
[12] a -D-Arabinopyranose