Die Zucker in Lösung liegen meist in zyklischer Form vor, die als Halbacetal bezeichnet werden. Das Halbacetal wird durch Angriff einer der Hydroxylgruppen der Kette am Carbonyl erhalten. Die gebildeten Zyklen bestehen aus fünf oder sechs Mitgliedern.
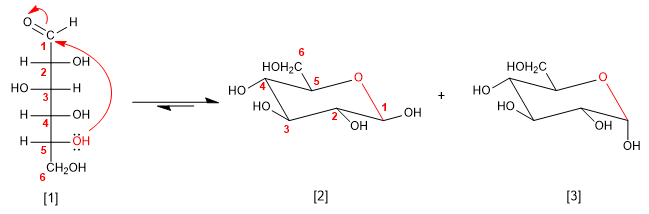
[1] D-Glucose
[2] b -D-Glucopyranose
[3] a -D-Glucopyranose
Um das Halbacetal zu zeichnen, platzieren wir die in der Fischer-Projektion rechts stehenden -OHs im Stuhl nach unten, die linken nach oben.
Das -OH an Position 1 (-OH an den anomeren Kohlenstoff gebunden) kann zwei Orientierungen annehmen, die zu Alpha- (-OH nach unten) und Beta- (-OH nach oben) Anomeren führen. Andererseits wird das -CH 2 OH, das von Kohlenstoff 5 ausgeht, in den Zuckern der D-Reihe nach oben orientiert sein, während es in den L-Zuckern nach unten orientiert sein wird.
Glucose kann auch als 5-Ring (Furanose) cyclisieren, indem das Hydroxyl in 4-Position auf das Carbonyl angegriffen wird.
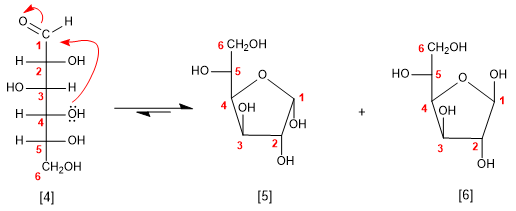
[4] D-Glucose
[5] a -D-Glucofuranose
[6] b -D-Glucofuranose
Obwohl die Halbacetalform im wässrigen Medium vorherrschend ist, existiert sie im Gleichgewicht mit einem kleinen Anteil offener Moleküle. Somit eliminieren die Reaktionen, die auf die Carbonylgruppe einwirken (Oxidationen oder Reduktionen), die offene Form aus dem Medium, wodurch sich das Gleichgewicht nach links verschiebt und die Öffnung der Halbacetale bewirkt.
Die Pyranose-Form ist stabiler als Furanose im Fall von Glukose
Nach den oben angegebenen Regeln werden wir das Arabinose-Molekül cyclisieren. Angriff vom Hydroxyl in 4-Position erzeugt ein 5-gliedriges Halbacetal (Furanose).
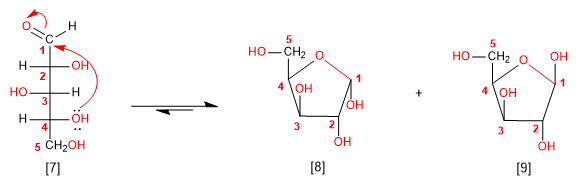
[7] D-Arabinose
[8] a -D-Arabinofuranose
[9] b -D-Arabinofuranose
Wir können auch Arabinose aus dem Hydroxyl an Position 5 cyclisieren, wodurch 6-gliedrige Zyklen (Pyranose) erzeugt werden.
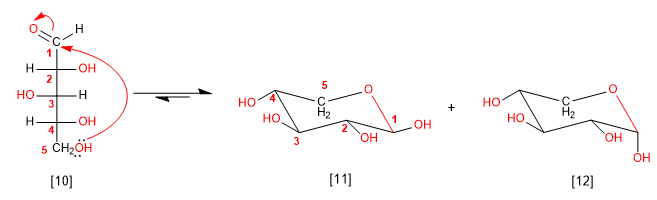
[10] D-Arabinose
[11] b -D-Arabinopyranose
[12] a -D-Arabinopyranose