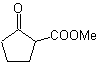
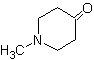
РАЗЪЕДИНЕНИЕ 1,3-ДИОКИСЛОРОДНЫХ СОЕДИНЕНИЙ
Оксигенированные органические соединения наиболее распространены в природе, особенно диоксигенаты, поэтому многие исследователи-химики смоделировали ретросинтетическое разъединение этих молекул, аспект, который будет изучен в следующих параграфах.
Начнем с того, что модели разъединения диоксигенированных молекул были разделены на две большие группы, основанные на природе синтонов, которые генерируются при применении к синтезируемой молекуле базовой синтетической операции, называемой « РАЗЪЕДИНЕНИЕ» , и на том, что, как правило, это называется молекулой-мишенью (MOb) .
Эти большие группы:
![]() « Логические » модели отключения и
« Логические » модели отключения и
![]() « Аномальные » или « нелогичные » модели отключения
« Аномальные » или « нелогичные » модели отключения
Так называемые «логические» модели разъединения — это модели, в которых путем «разрыва» одной или нескольких химических связей в
Соединения, которые можно классифицировать как 1,3-диоксиген и 1,5-диоксиген, при ретросинтезе обычно образуют синтоны, считающиеся «логичными». С другой стороны, органические молекулы, родственные 1,2-диоксигенатам, 1,4-диоксигенатам и 1,6-диоксигенатам, генерируют синтоны.
считается «нелогичным»
Модель отсечки 1,3-дикислорода
![]() β-дикарбонильные соединения
β-дикарбонильные соединения
1,3-дикарбонильные соединения получают с хорошими выходами в результате реакций конденсации типа Кляйзена, которые включают реакцию между сложными эфирами и соединениями с активными атомами водорода, такими как: сложные эфиры, кетоны, альдегиды, нитрилы, нитропроизводные и некоторые углеводороды в присутствии щелочные реагенты.
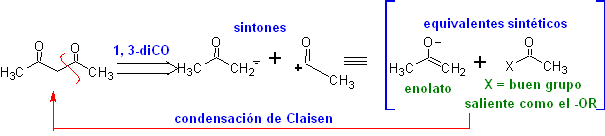
Бета-дикетоны и бета-кетоальдегиды получают перекрестной конденсацией Кляйзена с использованием подходящего кетона и сложного эфира. В перекрестной конденсации Клайзена кетонов и эфиров получаются хорошие выходы, поскольку кетоны заметно более кислые, чем эфиры, поэтому в основной среде кетон депротонируется в большей степени, чем эфир.
Примеры : Предложите план синтеза из простых материалов для следующих молекул:
Моб 16
| моб 17
| МОБ 18
|
Решение:
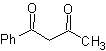
МОБ 16 . По-видимому, два варианта отключения (а) и (б), показанные на рис.
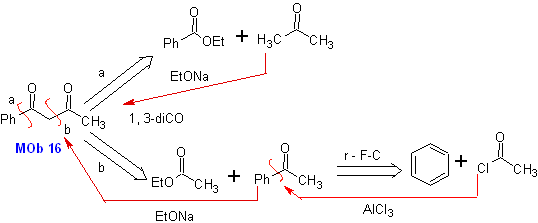
Однако вариант (б) оказывается наиболее подходящим, так как в основной реакционной среде карбанион, образующийся PhCOCH 2 - будет лучше стабилизирован за счет резонансного и индуктивного эффектов.
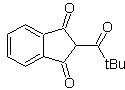
МОБ 17. Отключение (а), в
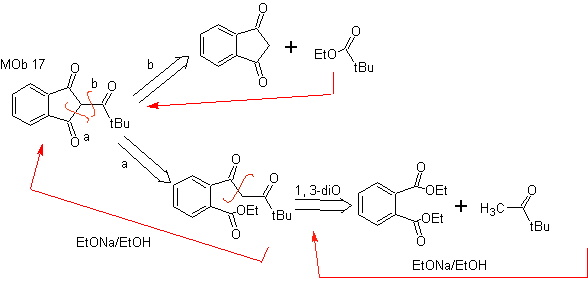
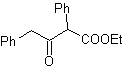
MOb 18. Наилучшей альтернативой отключения в этом MOb является (b), потому что это приводит к симметричным синтетическим эквивалентам. альтернатива (а) имеет важное значение при использовании этилформиата.
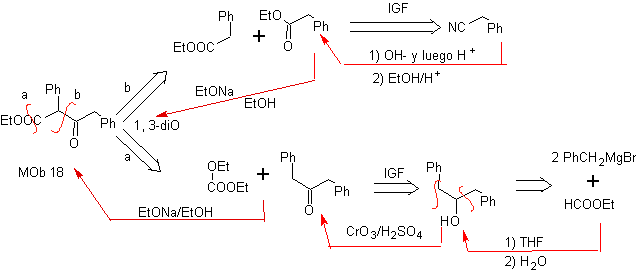
![]() β-дикарбонильные соединения за счет внутримолекулярных конденсаций
β-дикарбонильные соединения за счет внутримолекулярных конденсаций
Предложите возможный план синтеза следующих молекул: | моб 19
| МОБ 20
|
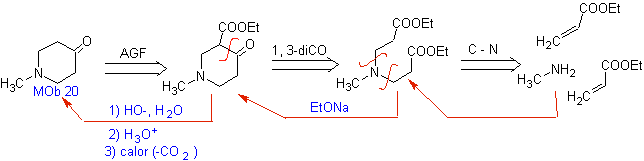
МОБ 19. Разъединение 1,3–диСО, приводит к диэфиру в отношении 1,6. Их легко снова соединить с алкеновым гексациклом, модель которого будет изучена чуть позже. По этой причине предлагается альтернативная схема синтеза, основанная на известных реакциях.
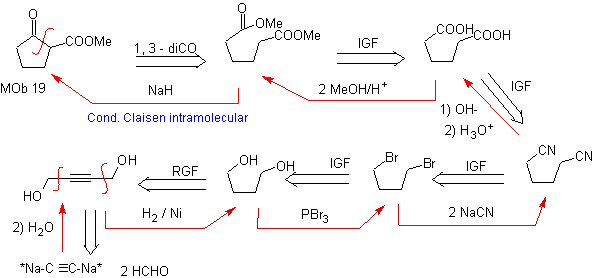
Дизайн, который может быть подвергнут сомнению только большим количеством стадий, что обычно снижает выход синтеза.
Можно подумать о другом отключении 1, 3 – диКО для
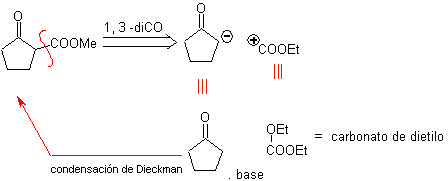
МОБ 20 . Иногда необходимо осуществлять контроль над структурой
Так,
![]() бета -гидрокси соединения
бета -гидрокси соединения
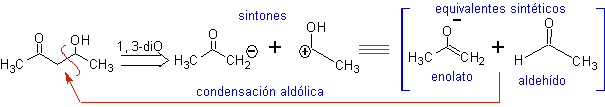
МОБ21 . Наилучшее разъединение в бета-гидроксисоединениях происходит за счет связи, образованной между C и
и C b относительно карбонильной группы. Эти типы соединений являются типичными продуктами реакций альдольной конденсации и т.п., поэтому хорошая схема синтеза для
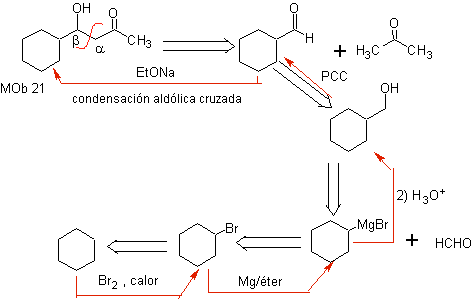
Основание, используемое для образования b -гидроксикарбонилов, должно быть слабым, чтобы избежать дегидратации спиртовой группы и, таким образом, образования a , b- ненасыщенного карбонильного соединения, которое будет предметом нашего исследования в следующем абзаце.
Реакция форм-циклогексанона с ацетоном в щелочной среде является реакцией конденсации альдольного типа. Альдегидная группа является наиболее реакционноспособной и отсутствует риск самоконденсации. альдегида за счет стерических эффектов.
![]() a , b ненасыщенные карбонильные соединения ( a , b ненасыщенный CO )
a , b ненасыщенные карбонильные соединения ( a , b ненасыщенный CO )
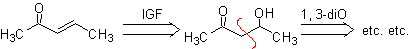
α, β-ненасыщенные карбонильные соединения легко получить путем дегидратации β-гидроксикарбонильных соединений, поэтому их отсоединение включает функционализацию ненасыщенной молекулы до спирта. Олефиновую связь также можно получить с помощью реакции Виттига.
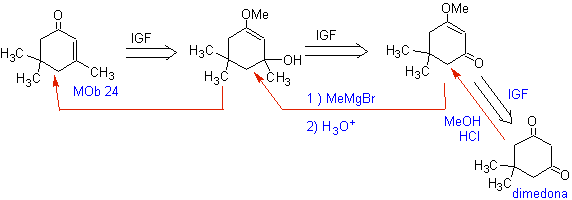
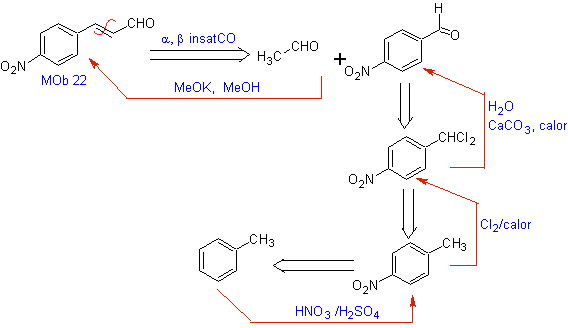
MOb 22. Поскольку a,b-ненасыщенное карбонильное соединение MOb 22 может быть функционализировано до соответствующего спирта, для получения 1,3-диоксигенированной модели можно напрямую разъединить молекулу двойной связью, получая C = Группа О на углероде b и группа -CH 3 на углероде а .
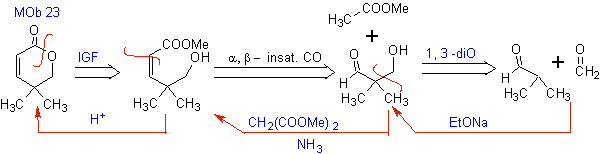
MOb 23. Разрыв этой молекулы начинается с циклического эфира (лактона), так как это наиболее критическая точка, которая затем позволяет разъединить ее как a , b ненасыщенное карбонильное соединение.
MOb 24. Обычное разъединение по двойной связи