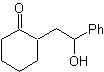
ОТКЛЮЧЕНИЕ 1,4-ДИОКИСЛОРОДНЫХ СОЕДИНЕНИЙ
Другая группа соединений, имеющих большое значение в химическом синтезе, состоит из диоксигенированных молекул, которые находятся в соотношении расстояний 1,4. Эти соединения при ретросинтетическом анализе разрыва генерируют синтоны, причем один из них, электрофил или нуклеофил, можно считать «аномальным» или «нелогичным», поскольку заряд, приписываемый одному из атомов, не может быть объяснен в с точки зрения его внутренней или индуцированной электроотрицательности.
1. Соединения 1,4-дикислорода (1,4-диО)
В соединениях этого типа разрыв также приводит к логическому синтону и к другому нелогичному (неприродному) синтону, который может быть нуклеофилом или электрофилом, чей синтетический эквивалент еще должен быть адекватно переработан, чтобы его можно было использовать в реакция химия.
1. 1. Соединения 1,4-дикарбонил
1.1.1. 1,4-дикетоновые соединения
Варианты отключения этого типа соединений или молекул, подлежащих синтезу (MOb), могут привести к следующим вариантам:
к. Синтон логического аниона и синтон нелогичного катиона
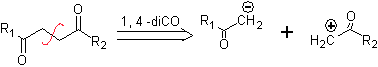
Синтетический эквивалент аниона представляет собой енолят-ион или сам енол карбонильного соединения. Вместо этого синтетическим эквивалентом карбокатиона является альфа-галогенкарбонил. (Умполунг)
б. Синтон логического катиона и синтон нелогичного аниона
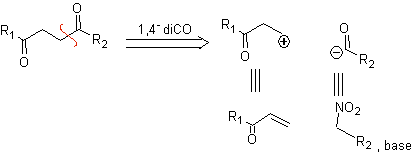
Синтетический эквивалент синтона логического катиона представляет собой α,β-ненасыщенное карбонильное соединение. Подходящим синтетическим эквивалентом синтона аниона может быть анион нитроалкана. Группа –NO 2 в алканах может быть превращена в С=О посредством реакции Нефа или вариантами реакции Мак-Мурри, где под действием TiCl 3 нитроалкан превращается в имин, который затем превращается в имин. гидролизуется в кислой среде до соответствующего карбонильного соединения.
1.1.2.
1,4-кетоэфирные соединения
γ-Кетоэфиры, 1,4-диэфиры и 1,4-дикислоты могут быть отсоединены к природному катиону синтону, синтетическим эквивалентом которого является α,β-ненасыщенное карбонильное соединение, и к неприродному («нелогичному» ) анион синтон (-) COOR, синтетическим эквивалентом которого является цианид-ион.
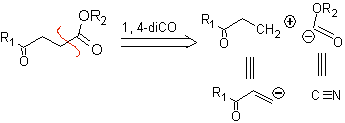
Примеры: Предложите план синтеза из простых и доступных материалов для каждой из следующих молекул:
МОБ 35
| МОБ 36
| |
Моб 37
| Моб 38
|
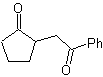
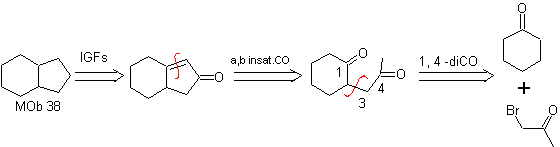
МОБ 35 (а). Ретросинтетический анализ . Молекула может быть разъединена по модели 1,4-диСО. Образовавшийся предшественник циклопентанон должен быть предварительно активирован, чтобы его Cα был более нуклеофильным, а затем использовать в реакции с α-бромацетоном.
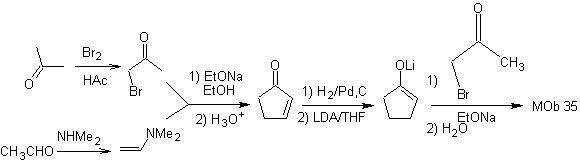
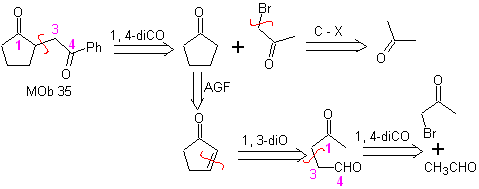 синтез . Нуклеофильность циклопентанона контролируется и гарантируется с помощью LDA, чтобы получить
синтез . Нуклеофильность циклопентанона контролируется и гарантируется с помощью LDA, чтобы получить
МОБ 35 (б). Ретросинтетический анализ . Модель 1,4-диСО, которая представляет
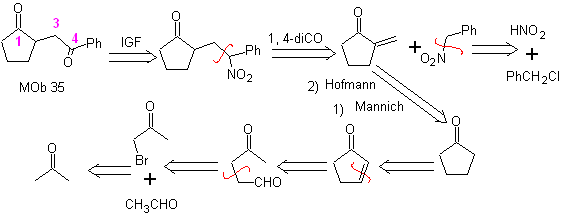
синтез . Аналогично, последний этап, чтобы достичь
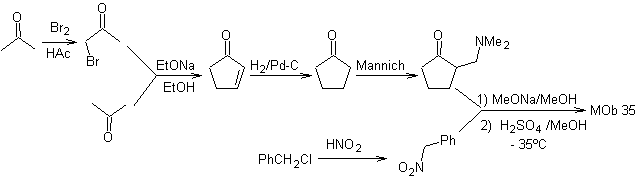
Использование вторичных нитроалканов или нитроаренов приводит к образованию кетонов в качестве продукта реакции Нефа, поэтому эта методология применима только к соединениям 1,4-кетоэфиров, 1,4-кетонов и 1,4-кетоальдегидов.
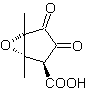
MOb 36. Ретросинтетический анализ. В первом случае карбоксильная группа
Следует понимать, что двойная связь в кольце более реакционноспособна к эпоксидированию, чем другая двойная связь. Последующее разъединение α,β-insat CO позволяет сформировать структуру, которую легче разъединить по моделям. диоксигенаты образуются в промежуточных молекулах.
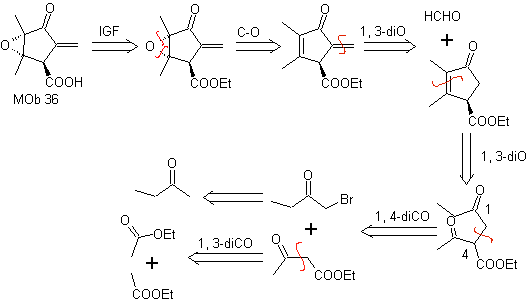
Синтез. Единственная осторожность, которую необходимо соблюдать в этом синтезе, - это эпоксидирование кольцевой двойной связи, более реакционноспособной, чем виниловая двойная связь, а затем реакции для достижения синтеза
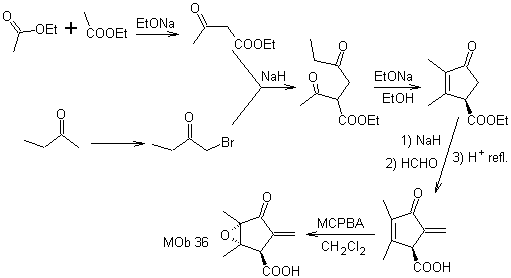
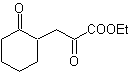
MOb 37. Ретросинтетический анализ: Отключение
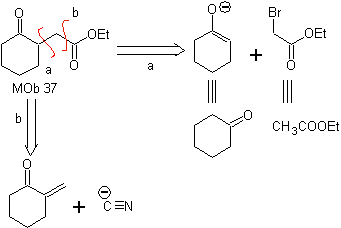
Синтез : следует разъединение (а). гидролиз
в конце концов, его нужно контролировать, чтобы
не влияет на сложноэфирная группа MOb 37
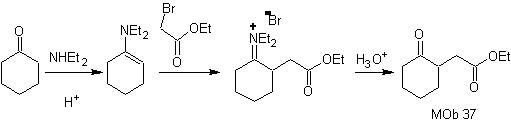
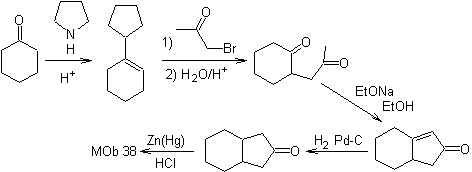
синтез .
Енамин циклогексанона снова используется для замены галогена кетона. Образовавшееся соединение 1,4-диСО циклизуют в щелочной среде.
2.1.2.
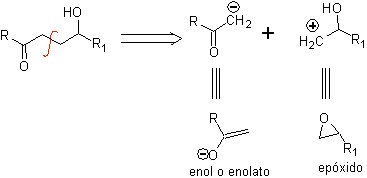
g -Гидроксикарбонильные соединения
γ-гидроксикарбонильное соединение соответствует модели 1,4-диО, поэтому его разъединение дает логичный анионный синтон и нелогичный катионный синтон, синтетическим эквивалентом которого может быть эпоксид.
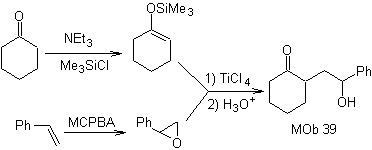
Как можно было синтезировать следующую молекулу? | Моб 39
|
МОБ 39. Ретросинтетический анализ.
Отключение модели
γ-гидроксикарбонил, MOb 39, дает циклогексанон в качестве молекулы-предшественника и ароматический эпоксид. Вы должны искать енол или енолят кетона, который активирует его Cα, чтобы открыть эпоксид на менее затрудненной стороне.
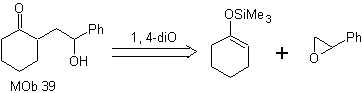
Синтез. Силиленовый эфир является мощным нуклеофилом, способным атаковать эпоксид с менее защищенной стороны в кислой среде и катализируется солью Ti(IV).