La réaction entre le 2-aminoéthylbenzène et un halogénure d'alcanoyle en présence de pyridine forme un amide. L'amide est converti en électrophile de Vilsmeier par réaction avec l'oxytrichlorure de phosphore. La cyclisation se produit par attaque du benzène audit électrophile. Une oxydation finale génère de l'isoquinoline.
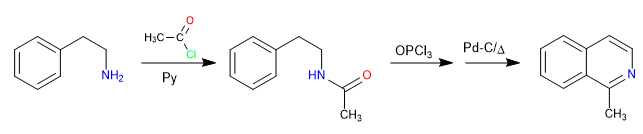
Mécanisme:
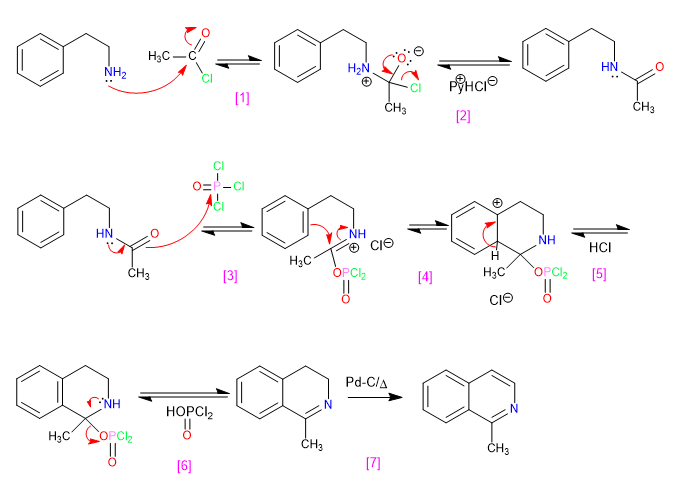
[1] Addition nucléophile à un halogénure d'acide
[2 ] Élimination du chlorure d'hydrogène
[3] Attaque l'oxytrichlorure de phosphore
[4 ] Cyclisation par attaque du benzène à l'électrophile
[5 ] Récupération de l'aromaticité.
[6 ] Supprimer
Oxydation