TEORI ASAM AMINO DAN PEPTIDA
- Detail
- Germán Fernández
- TEORI ASAM AMINO DAN PEPTIDA
- Dilihat: 56990
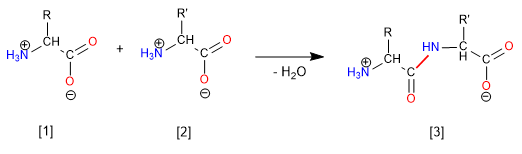
Asam amino adalah senyawa organik yang mengandung asam karboksilat dan fungsi amino. Dua asam amino dapat bergabung dalam kondisi yang sesuai, melalui ikatan amida, membentuk dipeptida. Dipeptida dapat menggabungkan asam amino ketiga, membentuk tripeptida. Rantai dengan lebih dari 50 asam amino disebut protein.
- Detail
- Germán Fernández
- TEORI ASAM AMINO DAN PEPTIDA
- Dilihat: 207787
20 asam amino penyusun protein adalah: Serin (Ser,S), Threonine (Thr,T), Cysteine (Cys,C), Asparagine (Asn,N), Glutamine (Gln,Q) dan Tyrosine (Tyr , Y), Glisin (Gly,G), Alanin (Ala,A), Valin (Val,V), Leusin (Leu,L), Isoleusin (Ile,I), Metionin (Met,M), Prolin (Pro, P ), Fenilalanin (Phe,F) dan Triptofan (Trp,W), Asam Aspartat (Asp,D) dan Asam Glutamat (Glu,E), Lisin (Lys,K), Arginin (Arg,R) dan Histidin (Nya , jam)
- Detail
- Germán Fernández
- TEORI ASAM AMINO DAN PEPTIDA
- Dilihat: 149125
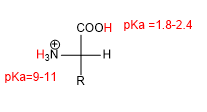 Adanya gugus asam (-COOH) dan basa (-NH 2 ) memberikan sifat asam-basa yang khas pada asam amino.
Adanya gugus asam (-COOH) dan basa (-NH 2 ) memberikan sifat asam-basa yang khas pada asam amino.
- Detail
- Germán Fernández
- TEORI ASAM AMINO DAN PEPTIDA
- Dilihat: 56260
Asam amino dapat diperoleh dengan halogenasi asam karboksilat, diikuti dengan substitusi nukleofilik dengan amonia. Halogenasi posisi asam karboksilat dilakukan dengan reaksi Hell-Volhard-Zelinsky.
- Detail
- Germán Fernández
- TEORI ASAM AMINO DAN PEPTIDA
- Dilihat: 46306
Dalam sintesis ini, garam phthalimide direaksikan dengan ester malonat terhalogenasi. Pada tahap selanjutnya ia dialkilasi, dihidrolisis dan didekarboksilasi, memperoleh asam amino.
- Detail
- Germán Fernández
- TEORI ASAM AMINO DAN PEPTIDA
- Dilihat: 32950
Ini adalah metode yang banyak digunakan untuk menyiapkan asam amino di laboratorium. Ethanamide amidate [1] direaksikan dengan ester malonat terhalogenasi [2] , memperoleh senyawa [3] yang dialkilasi dan dihidrolisis menghasilkan diacid [6] , yang terdekarboksilasi membentuk asam amino [7] .
- Detail
- Germán Fernández
- TEORI ASAM AMINO DAN PEPTIDA
- Dilihat: 54315
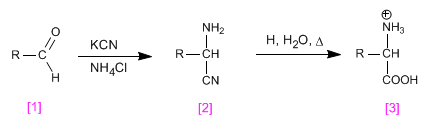
Sintesis Strecker memungkinkan memperoleh asam amino dari aldehida atau keton.
- Detail
- Germán Fernández
- TEORI ASAM AMINO DAN PEPTIDA
- Dilihat: 30518
- Detail
- Germán Fernández
- TEORI ASAM AMINO DAN PEPTIDA
- Dilihat: 29684
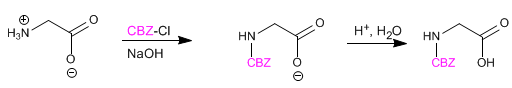
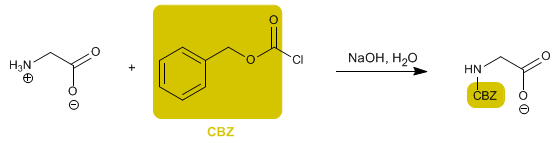
Gugus amino dilindungi untuk mencegah reaksinya dengan gugus asam dari asam amino kedua. Setelah ikatan peptida terbentuk, deproteksi dilakukan, sekali lagi membiarkan gugus amino bebas.
- Detail
- Germán Fernández
- TEORI ASAM AMINO DAN PEPTIDA
- Dilihat: 22656
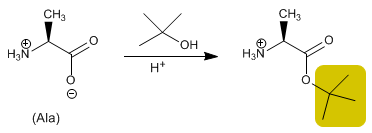
Gugus asam dilindungi dengan mengubahnya menjadi ester melalui reaksi dengan alkohol. Metil, etil atau tert -butil ester dibuat dengan esterifikasi dan dihidrolisis (deproteksi) dalam media basa.
- Detail
- Germán Fernández
- TEORI ASAM AMINO DAN PEPTIDA
- Dilihat: 47338
Sintesis dipeptida Glycine-Alanine (Gly-Ala) terjadi melalui pembentukan ikatan amida (peptida) antara gugus asam Glycine dan gugus amino alanine. Oleh karena itu, perlu untuk melindungi gugus amino Glycine dan asam alanine.