TEORI QUINOLINE DAN ISOQUINOLINE
- Detail
- Germán Fernández
- TEORI QUINOLINE DAN ISOQUINOLINE
- Dilihat: 2666
a) Dasar
Quinoline dan isoquinoline berperilaku seperti basa melalui pasangan bebas nitrogen. Dalam media asam mereka terprotonasi untuk membentuk garam quinolinium dan isoquinolinium.
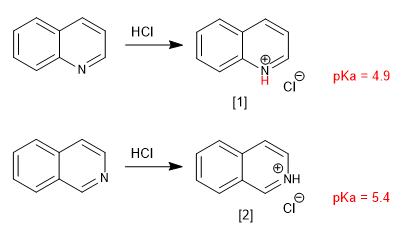
[1] garam Quinolinium
[2] Garam isoquiniolinium
Substituen memodifikasi kebasaan dengan cara yang analog dengan piridin. Kelompok donor meningkatkan kebasaan dan kelompok penarik menurunkannya.
Selengkapnya: Reaksi dengan pasangan bebas nitrogen: quinoline dan isoquinoline
- Detail
- Germán Fernández
- TEORI QUINOLINE DAN ISOQUINOLINE
- Dilihat: 3110
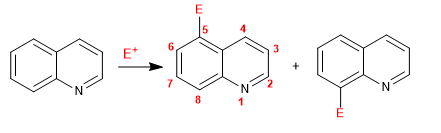
Quinoline dan isoquinoline bereaksi dengan elektrofil melalui cincin benzena (karbosik), karena kekayaan elektroniknya yang lebih tinggi, dibandingkan dengan cincin piridin. Posisi yang paling disukai adalah 5 dan 8.
Selengkapnya: Reaksi substitusi elektrofilik dalam quinoline dan isoquinoline
- Detail
- Germán Fernández
- TEORI QUINOLINE DAN ISOQUINOLINE
- Dilihat: 2513
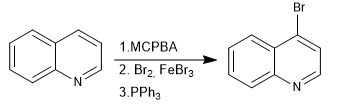
N-oksida memungkinkan elektrofil ditempatkan pada posisi 4 dari quinoline.
- Detail
- Germán Fernández
- TEORI QUINOLINE DAN ISOQUINOLINE
- Dilihat: 2382
Reaksi antara turunan halogenasi quinoline dan isoquinoline dengan organolitik pada suhu rendah menghasilkan pertukaran halogen dengan logam, menghasilkan organolitik baru pada cincin.
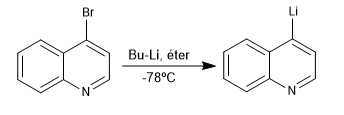
Selengkapnya: Reaksi litiasi dalam quinoline dan isoquinoline
- Detail
- Germán Fernández
- TEORI QUINOLINE DAN ISOQUINOLINE
- Dilihat: 2586
Nukleofil menambah karbon 2 dari quinoline, meskipun dalam kondisi tertentu juga dapat menerima serangan terhadap karbon 4.
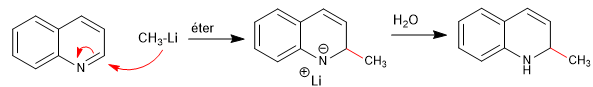
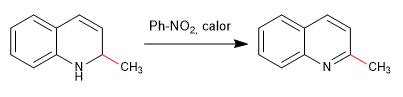
Selengkapnya: Adisi nukleofilik ke quinolines dan isoquinolines
- Detail
- Germán Fernández
- TEORI QUINOLINE DAN ISOQUINOLINE
- Dilihat: 2747
Kuinolin terhalogenasi pada posisi 2,4 sangat mudah mengalami reaksi substitusi nukleofilik. Untuk bagiannya, isoquinoline hanya dapat memberikan reaksi ini pada posisi 1. Semua nukleofil dengan kapasitas untuk memberikan S N 2 dapat berpartisipasi dalam reaksi ini, nukleofil yang buruk seperti air atau alkohol memerlukan masukan panas.
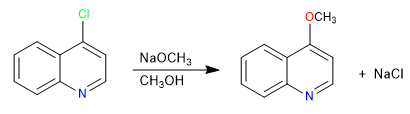
Selengkapnya: Substitusi nukleofilik dalam quinoline dan isoquinoline
- Detail
- Germán Fernández
- TEORI QUINOLINE DAN ISOQUINOLINE
- Dilihat: 2348
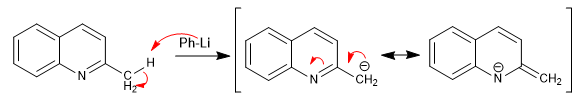
Piridin dengan gugus alkil posisi 2,4 memiliki hidrogen asam pada karbon yang berdekatan dengan cincin piridin.
- Detail
- Germán Fernández
- TEORI QUINOLINE DAN ISOQUINOLINE
- Dilihat: 29583
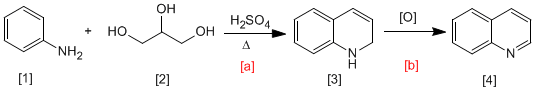
Dalam sintesis Skraup, anilin [1] bereaksi dengan karbonil tak jenuh a,b dalam media asam membentuk 1,2-dihidroquinolin [3], yang diubah menjadi kuinolin melalui oksidasi [4]. Karbonil tak jenuh a,b dapat diperoleh dengan dehidrasi 1,2,3-propanetrium [2].
- Detail
- Germán Fernández
- TEORI QUINOLINE DAN ISOQUINOLINE
- Dilihat: 7571
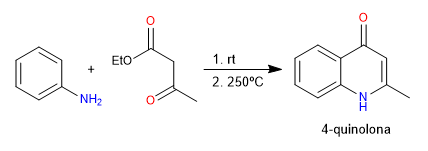
Dalam sintesis Conrad-Limpach, kuinolon diperoleh dengan mereaksikan anilin dengan 3-ketoester. Dalam kondisi kinetik 4-kuinolon diperoleh dan dalam kondisi termodinamika 2-kuinolon.
- Detail
- Germán Fernández
- TEORI QUINOLINE DAN ISOQUINOLINE
- Dilihat: 2477
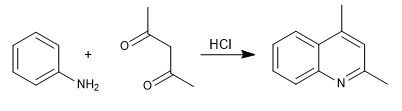
Dalam sintesis Combes, kuinolin diperoleh dengan mereaksikan anilin dengan 1,3-dikarbonil, dengan adanya katalisis asam. Pada tahap pertama, imina terbentuk, yang mengalami tautomerisasi menjadi enamin,a, mengaktifkan cincin aromatik dengan melepaskan pasangan nitrogen. Pada tahap terakhir, siklisasi terjadi dengan penyerangan benzena ke rantai karbonil
- Detail
- Germán Fernández
- TEORI QUINOLINE DAN ISOQUINOLINE
- Dilihat: 2756
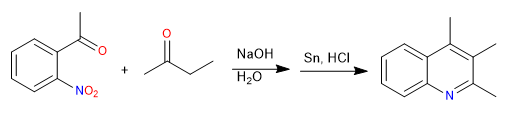
Sintesis Friedländer menyiapkan kuinolin dari nitrobenzena orto-asetilasi dan keton. Sintesis dimulai dengan kondensasi aldol dalam media basa. Pengurangan gugus nitro menjadi amino memungkinkan siklisasi dengan pembentukan imina.
- Detail
- Germán Fernández
- TEORI QUINOLINE DAN ISOQUINOLINE
- Dilihat: 2440
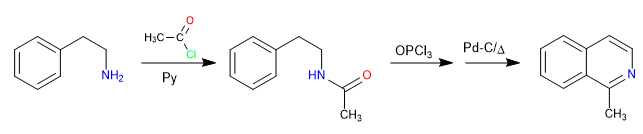
Reaksi antara 2-aminoetilbenzena dan alkanoil halida dengan adanya piridin membentuk amida. Amida diubah menjadi elektrofil Vilsmeier melalui reaksi dengan fosfor oksitriklorida. Siklisasi dihasilkan oleh serangan benzena ke elektrofil tersebut. Oksidasi akhir menghasilkan isoquinoline.
- Detail
- Germán Fernández
- TEORI QUINOLINE DAN ISOQUINOLINE
- Dilihat: 2570
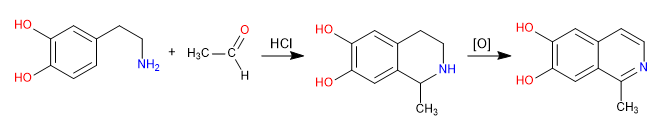
Pictet Spengler adalah reaksi tipe Mannich. Pada tahap pertama, elektrofil Mannich dibentuk oleh reaksi amina dengan aldehida dalam media asam klorida. Pada tahap akhir, siklisasi terjadi dengan serangan benzena pada elektrofil Mannich. Isoquinoline diperoleh setelah oksidasi ganda.
- Detail
- Germán Fernández
- TEORI QUINOLINE DAN ISOQUINOLINE
- Dilihat: 2493
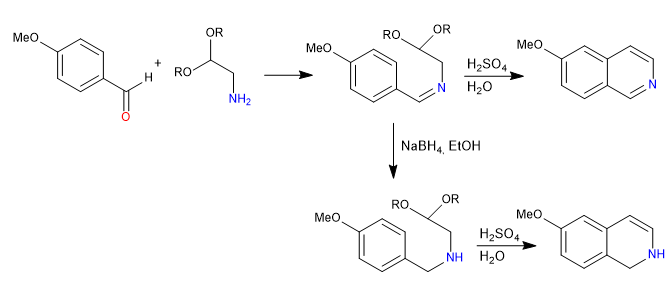
Sintesis Pomeranz-Fritsch menyiapkan isoquinolin dengan mereaksikan benzaldehida dengan a-aminoaldehida terlindungi dalam bentuk asetal. Pada tahap pertama, imina dibentuk oleh reaksi antara benzaldehida dan amina. Pada langkah kedua, asetal dipecah dengan asam sulfat encer, meninggalkan aldehida bebas, yang tersiklis di bawah serangan benzena.