Synthèse d'hétérocycles par cyclisation intermoléculaire
1. Cyclisations 1,3-dipolaires
Ces réactions forment normalement des hétérocycles à cinq chaînons, pour lesquels la réaction entre un composé dipolaire n1,3 et un alcène est nécessaire. La réaction est une [3-2] cycloaddition. Les composés 1,3-dipolaires qui ont eu le plus d'utilisation pour former des hétérocycles pentagonaux sont :
Azides, diazoalcanes, protoxyde d'azote, nitrile imines, oxydes de nitrile, azométhylène imines, composés azoxy, ylures d'azométhane, nitrones, oxydes de carbonyle et ozone.
Les cyclisations et déconnexions suivantes sont assez courantes, montrant la large gamme de réactifs 1,3-dipolaires et leurs structures de résonance ou tautomères utilisés dans le but de former des hétérocycles pentagonaux.
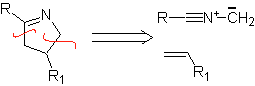 |
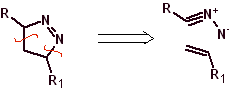 |
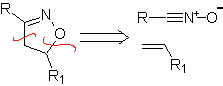 |
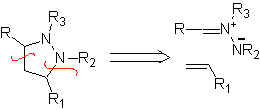 |
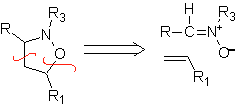 |
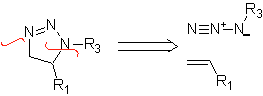 |
Le mécanisme généralement accepté de la réaction 1,3-dipolaire répond à une réaction concertée.
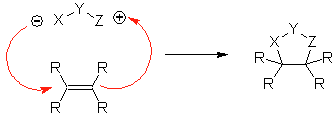
Proposer un plan de synthèse pour les molécules suivantes :
| Mob : 86
|
. |
Mob : 87 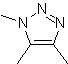 |
.. |
Mob : 88 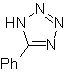 |
MOb 86
. Analyse rétrosynthétique
.
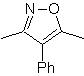
, est un dérivé de l'isoxazole. Sa déconnexion peut être orientée vers l'utilisation d'un oxyde de nitrile et d'un dérivé acétylénique.
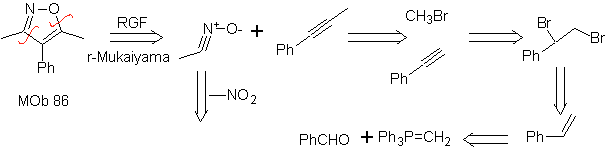
La synthèse. L'oxyde de nitrile peut être préparé à partir de nitrométhane par la réaction de Mukaiyama. Le dérivé acétylénique, issu du benzaldéhyde, faisant croître la chaîne avec insaturation, auparavant, avec la réaction de Wittig. Le diène polaire et le diénophile formé se combinent selon Diels-Alder pour former
86.
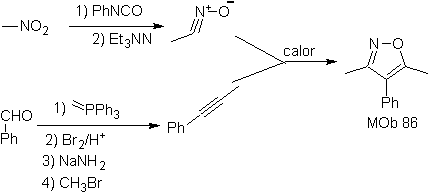
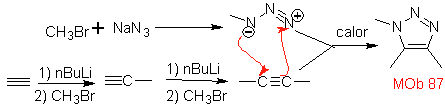
MOb 87
. Analyse rétrosynthétique.
c'est un dérivé du triazole, et il peut être déconnecté selon la réaction de Diels-Alder, ce qui permet de proposer des molécules de départ simples
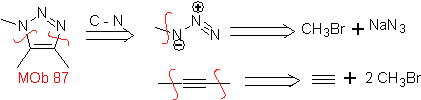
La synthèse. L'azide de sodium et l'acétylène sont de bons produits de départ pour préparer
87.
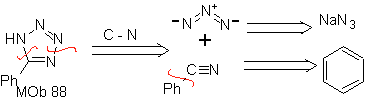
Mob 88. Analyse rétrosynthétique :
le dérivé de tétrazole MOb 88, est déconnecté pour générer des précurseurs d'azoture et de nitrile qui se combinent dans une cycloaddition hétéromoléculaire pour former un adduit hétérocyclique
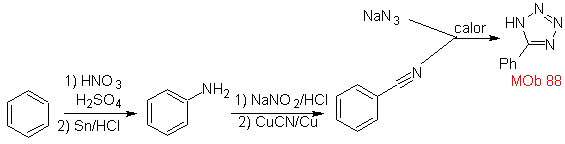
La synthèse: Le benzonitrile requis, un diénophile fort, est formé à partir du benzène par les réactions basiques indiquées. La réaction de cycloaddition, pour former l'adduit MOb 88, est réalisée avec de l'azoture de sodium, en tant que diénophile polaire, catalysé avec un peu de chaleur.
2. Réaction de Diels-Alder hétéronucléaire.
Lors de la réaction de Diels-Alder, un atome de carbone par un hétéroatome sur le diène ou le diénophile de la réaction, un adduit hétérocyclique à six chaînons est formé, avec au moins un hétéroatome dans le cycle.
Toutes les considérations théoriques et de réactivité, étudiées pour la réaction de Diels-Alder pour la formation d'adduits carbocycliques, s'appliquent.
hétérodiènes :
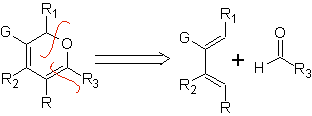
Ce sont de bons hétérodiènes, aldéhydes et cétones conjuguées, 1-azadiènes et 2-azadiènes. Les aldéhydes et cétones conjugués produisent des cycles pyraniques, la réaction est facilitée par les acides de Lewis ou une pression accrue, ainsi que la présence d'un groupe électronique. attractif pour l'alcène.
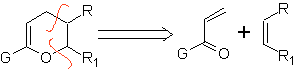
Hétérodiénophiles les plus courants dans la réaction de Diels-Alder :
Hétérodienophiles :
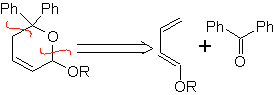
Les aldéhydes, cétones et aldéhydes, s'ils sont déficients en électrons, réagissent dans des conditions douces, sinon ils nécessitent des conditions de pression et de température élevées ou des catalyseurs de type acide de Lewis. Ces hétérodiénophiles permettent la formation de systèmes pyraniques, utiles dans la préparation de précurseurs acycliques de divers médicaments, comme c'est le cas des antibiotiques macrocycliques.
 |
… |
 |
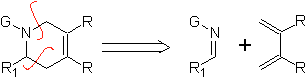
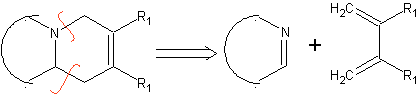
En raison de l'instabilité des imines, ils sont préparés in situ bien qu'ils soient moins utilisés comme hétérodiénophiles que les cétones et les aldéhydes. Les groupes accepteurs sur les imines les rendent plus stables. et permettent la formation d'hydropyridines.
 |
 |
Hétérodiènes les plus courants dans la réaction de Diels-Alder :
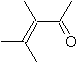 |
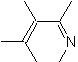 |
|
|
|
||
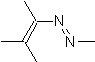 |
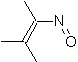 |
|
|
|
Proposer un design de synthèse pour les molécules suivantes :
Mob 89 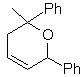 |
… |
Mob : 90 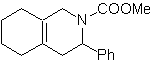 |
. |
Mob : 91 |
| Mob : 92
|
Mob : 93
|
Mob 94 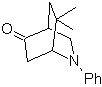 |
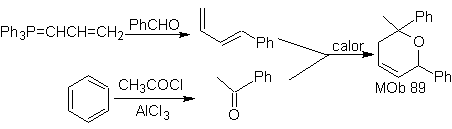
MOb 89
, Analyse rétrosynthétique.
Il présente la structure d'un adduit typique, formé par la réaction de Diels-Alder, c'est pourquoi une déconnexion rétro-Diels-Alder est proposée, avec laquelle un diène et un hétérodiénophile sont produits comme précurseurs appropriés pour faire face à la synthèse.
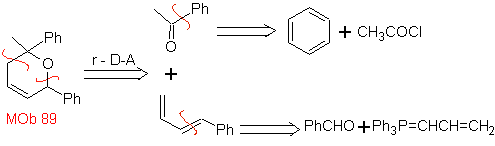
synthèse
. La réaction de Wittig sur le benzaldéhyde permet la formation du diène. L'hétérodiénophile est formé par une réaction d'acylation de Friedel-Crafts sur le benzène. Le diène et le diénophile se combinent avec un chauffage doux pour former
89
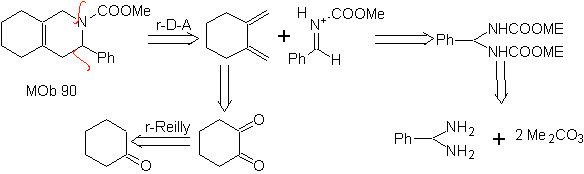
MOb 90
. Analyse rétrosynthétique
.
Il a la structure d'un hétéroadduit de Diels-Alder, pour lequel une déconnexion rétro Diels-Alder est effectuée. Alors les molécules précurseurs sont déjà faciles à synthétiser directement
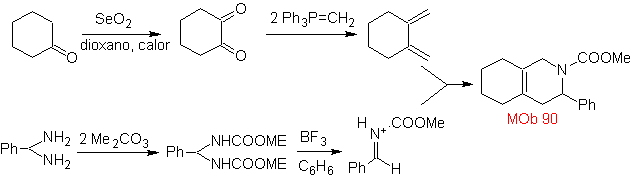
synthèse
. Les réactions d'oxydation de Wittig et de Reilly sont combinées en prenant soin d'activer l'hétérodiénophile pour réaliser la réaction de Diels-Alder et arriver à
90.
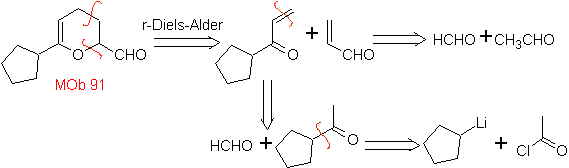
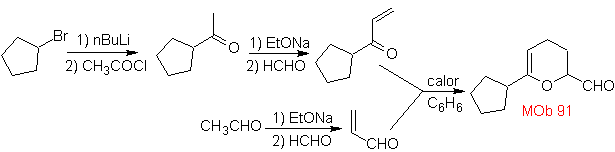
MOb 91 .
Analyse rétrosynthétique
. La première déconnexion
, peut suivre le chemin d'un rétro-Diels-Alder, donnant naissance à un diène commun et à un hétérodiène, qui sont ensuite dissociés pour aboutir à des précurseurs simples
synthèse
.
L'hétérodiène est formé par condensation entre la cétone et le formaldéhyde. Le diénophile est formé par condensation aldolique du l'acétaldéhyde, qui forme alors
91.
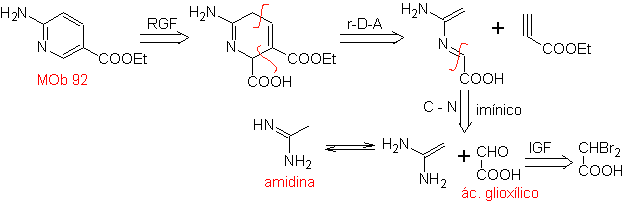
MOb 92.
Analyse rétrosynthétique.
.
un dérivé de pyridine, il est fonctionnalisé vers un adduit, où il se déconnecte selon rDA. La déconnexion de l'hétérodiène produit des molécules de départ simples, le diénophile est un dérivé acétylénique.
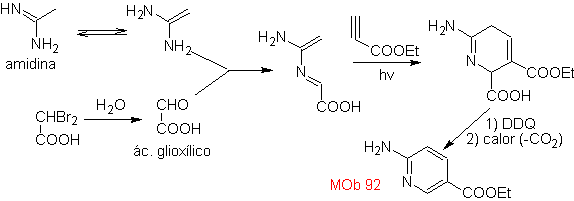
synthèse
. L'hétérodiène est préparé par condensation entre l'amidine et l'acide glyoxylique, pour ensuite associer le produit au diénophile. L'adduit formé est aromatisé avec du DDQ, pour former
92
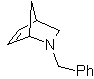
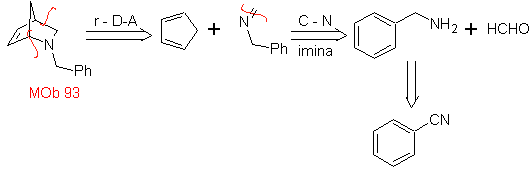
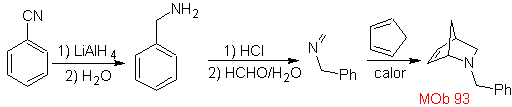
MOb 93.
Analyse rétrosynthétique
.
, il est déconnecté par rDA. Le diène est le cyclopentadiène et l'hétérodiénophile est une imine, qui par déconnexion conduit au benzonitrile, comme produit de départ.
synthèse
. L'imine formée agit comme un diénophile et se combine avec le cyclopentadiène pour former
93
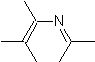
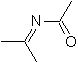
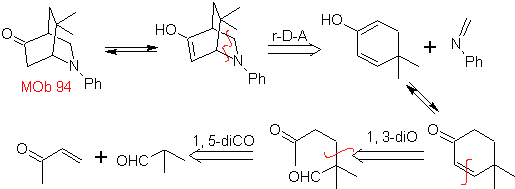
MOb 94.
Analyse rétrosynthétique
. Au tautomère de
, il procède à la déconnexion selon rDA. Le diène formé se tautomérise pour s'éteindre sous forme d'α,β-insat.CO puis continue de s'éteindre sous forme de 1,5-diCO.
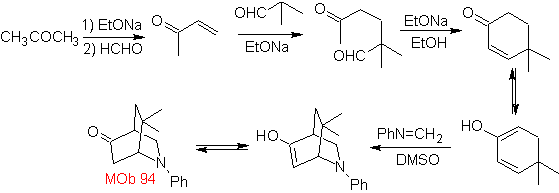
synthèse
. L'aniline imine se combine avec le diène qui est un tautomère α, β-insat.CO, pour former un adduit, qui s'avère être un tautomère de
94
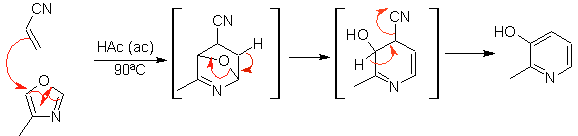
cycloadditions
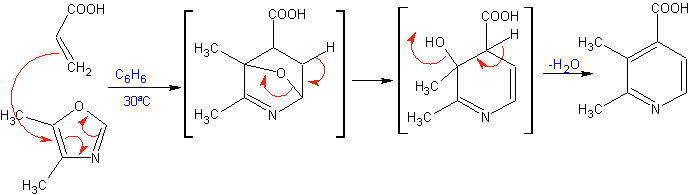
Les cycloadditions les plus étudiées sont celles qui se produisent entre les composés hétérocycliques pentagonaux tels que les oxazoles et certains diénophiles, qui peuvent être combinés avec eux par addition électrocyclique et élimination ultérieure d'une petite molécule, pour produire des cycles pyridiniques. Exemples:
<!--[if !vml]--><!--[endif]-->