Autres stratégies de synthèse utilisant des syntons « illogiques »
1. addition de triple liaison
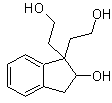
La stratégie de « rajouter » une triple liaison, entre deux fonctions oxygénées en position 1,4, permet de travailler ultérieurement avec une déconnexion basée sur la chimie des acétylures. Afin d'illustrer cette stratégie, voyons l'élaboration d'un plan de synthèse pour
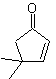
Foule. 40. Analyse rétrosynthétique . Un premier IGF en
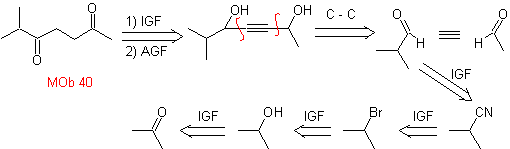
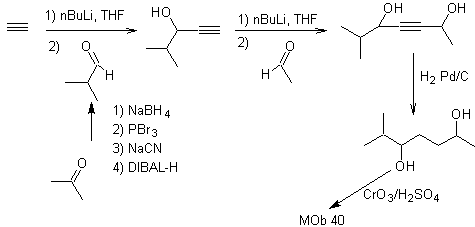
La synthèse. Le diacétylure ou acétylure par étapes, se combine avec des molécules de différents aldéhydes, la molécule intermédiaire formée est hydrogénée puis ses alcools sont oxydés en composé dicétonique Mob 40.
Les γ-lactones peuvent également être préparées de manière analogue, comme indiqué ci-dessous :

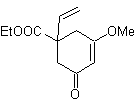
2. Ajout du groupe COOR comme groupe d'activation
L'ajout du groupe COOR, en plus d'activer l'anion synthon, facilite la déconnexion d'une molécule 1,4 diX.
|
synthétiser |
|
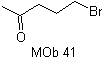
MOb 41. Analyse rétrosynthétique.
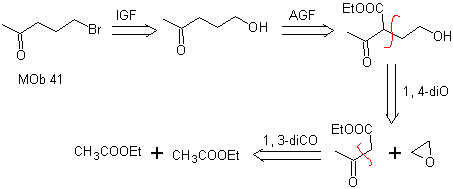
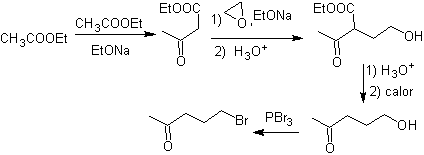
synthèse . L'acétoacétate d'éthyle est un nucléophile qui ouvre l'époxyde en milieu basique.
Le groupe ester est hydrolysé et décarboxylé pour arriver à
Proposer un plan de synthèse pour les molécules suivantes :
|
|
Mob 42
|
|
Mob 43
|
|
Mob 44
|
|
Mob 45
|
|
Mob 46
|
|
Mob 47
|
Mob 42 . Analyse rétrosynthétique . La déconnexion 1,3-diO de
|
Oxydation Wacker : |
|
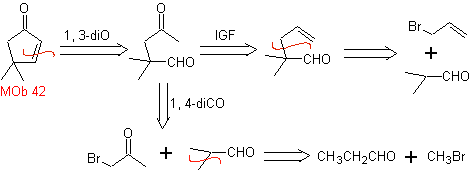
La synthèse. Le bromure d'allyle alkyle l'aldéhyde, le produit est oxydé puis cyclisé en milieu basique, pour former
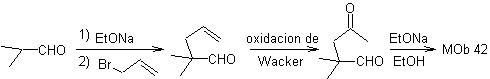
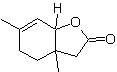
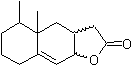
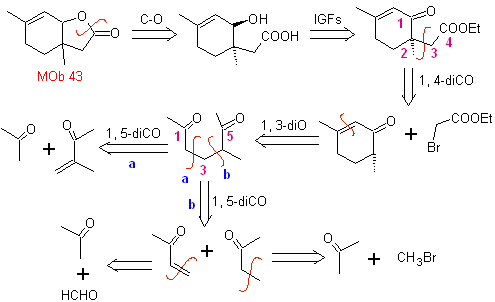
MOb 43, Analyse rétrosynthétique . La lactone, MOb 43, est ouverte, pour donner naissance à un γ-hydroxyacide, qui par les IGF, atteint un 1,4-cétoester, qui est déconnecté selon le modèle.
La cyclohexénone est formée par l'annelation de Robinson et le 1,5-diCO est préparé à partir de la réaction de Michael.
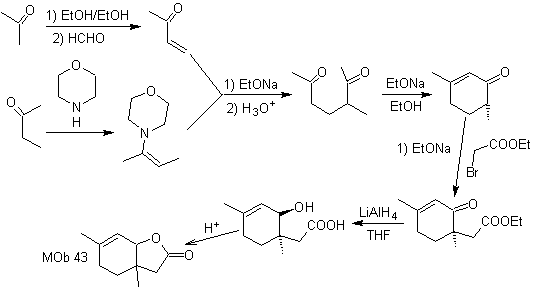
La synthèse. L'énamine carbonée secondaire est obtenue à l'aide d'une amine secondaire volumineuse. Le composé 1,5-diCO est cyclisé par annelation de Robinson puis mis à réagir avec l'ester α bromo en milieu basique. Le composé dicétone résultant est réduit par LiAlH 4 puis, en milieu acide, la lactone MOb 43 est formée.
Mob 44 . Analyse rétrosynthétique. Le premier FGI de
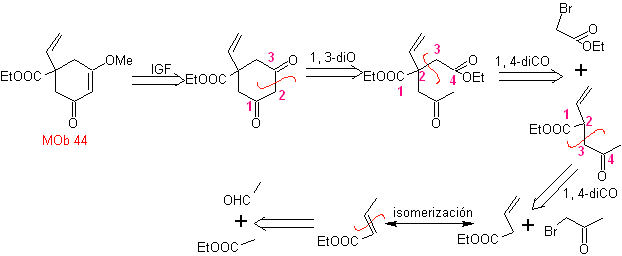
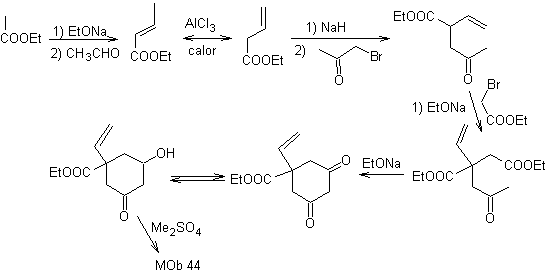
La synthèse. C'est une suite de condensations de type aldol ou Claisen. Afin de synthétiser
Mob 45 . Analyse rétrosynthétique : La déconnexion de la fonction lactone de
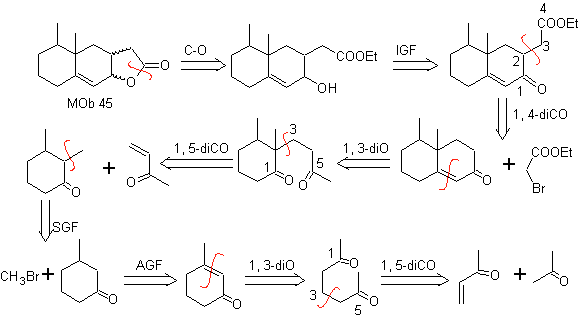
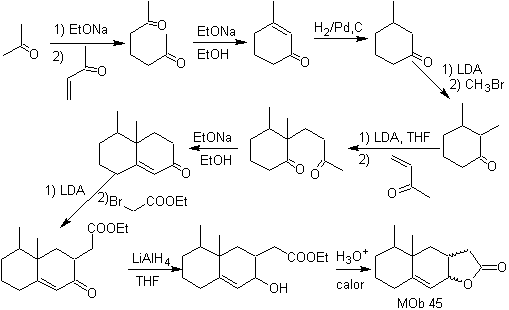
Synthèse : Toutes les réactions utilisées sont liées à la condensation de Michael, l'annelation de Robinson et la réaction de formation d'ester de Fischer, elle permet d'obtenir la lactone, c'est-à-dire
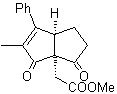
MOb 46. Analyse rétrosynthétique. . Il suit le Déconnexion du 1,4-diCO, car elle permet la séparation en deux parties
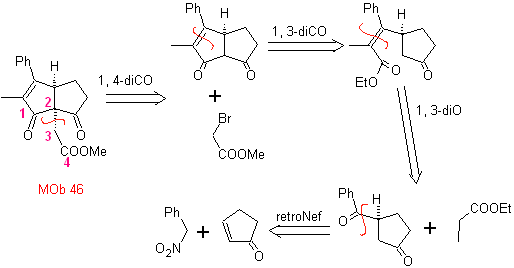
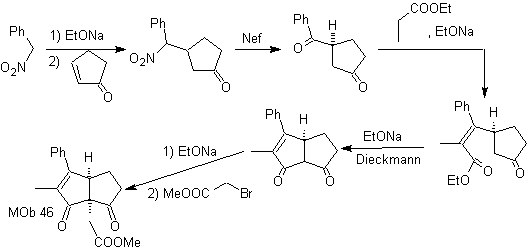
synthèse . Selon Michael, le nucléophile nitroarène s'ajoute à la cyclopentanone α,β-insaturée. Le groupe nitro est transformé en C=O, par la réaction Nef. Le composé dicarbonylé est mis à réagir avec l'énolate de propanoate d'éthyle, suivi de la réaction de Dieckmann, et les réactions nécessaires pour arriver à
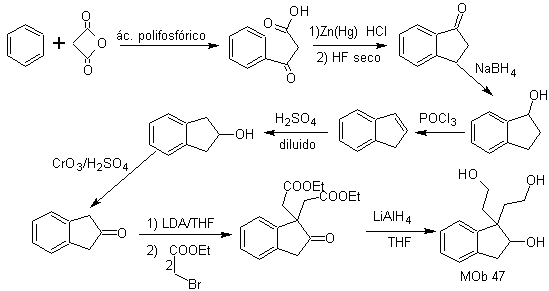
MOb 47. Analyse rétrosynthétique.
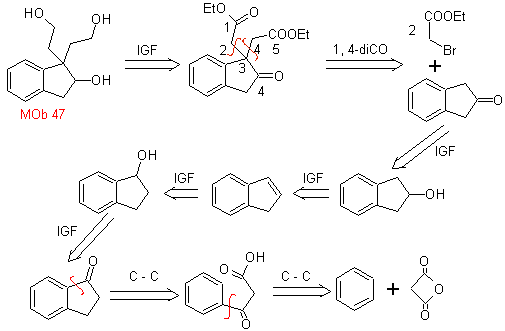
synthèse . La synthèse de