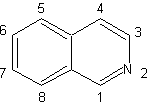
Sintesis isokinolin
(Dengan metode pemutusan)
| Isoquinolines berbeda secara struktural dari quinolines dalam posisi nitrogen, karena yang terakhir tidak menyatu, sehingga menghadirkan "reaktivitas alifatik". Itu tidak ditemukan bebas di alam, tetapi siklus isoquinoline ditemukan di beberapa alkaloid, dalam bentuk aromatik atau tereduksi, misalnya papaverine. |
Metode sintetik yang paling terkenal untuk pembuatan isoquinolines dimulai dengan 2-phenylethylamines dan melibatkan siklisasi melalui karbon tambahan yang disediakan oleh gugus karbonil dari senyawa lain.
Metode sintesis utama adalah: sintesis Pomeranz-Fritsch, sintesis Bischler-Napieralski, sintesis Pictet-Gams, dan sintesis Pictet-Spengler.
1. Sintesis POMERANZ-FRITCH.
Metode sintesis isoquinoline ini terjadi dalam dua tahap:
ke.
Pertama, benzaldehida (1,3-elektrofil-nukleofil) dipadatkan dengan aminoasetaldehida dietilasetal (1,3-nukleofil-elektrofil) untuk membentuk aldimin yang stabil.
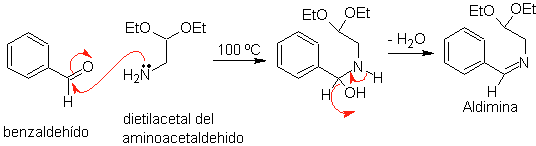
B.
Selanjutnya, aldimin tersiklis dalam media asam kuat, menjadi imina, dengan penghilangan etanol secara bersamaan, untuk menghasilkan isokinolin.
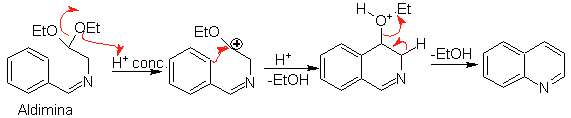
Tahap kedua ini, sebagai substitusi elektrofilik, tunduk pada efek yang dimiliki substituen pemberi atau penerima elektron pada cincin benzena dalam reaksi tersebut. Namun, karena hidrolisis imina yang terbentuk, dalam media asam kuat yang digunakan dalam reaksi, hasil proses berkurang.
Metode ini memungkinkan akses ke isoquinolin tersubstitusi C-1, yang keton aromatiknya telah diuji, dengan hasil yang sangat rendah. Namun, ada keberhasilan yang lebih besar menggunakan varian benzilamin tersubstitusi dengan tepat sebagai 1,4-dinukleofil dan dietilasetal glioksal sebagai 1,2-dielektrofil.
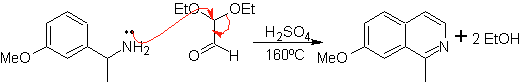
Sesuatu yang harus diperjelas adalah bahwa metode Pomeranz-Fritsch dan variannya, yang sebelumnya dianalisis, tidak memungkinkan pembuatan isoquinolin yang tersubstitusi pada C-3 dan C-4 dari heteroatom. Analisis retrosintetik dari metode ini menunjukkan kemungkinan intermediet yang terlibat dalam reaksi dan kemungkinan bahan awal.
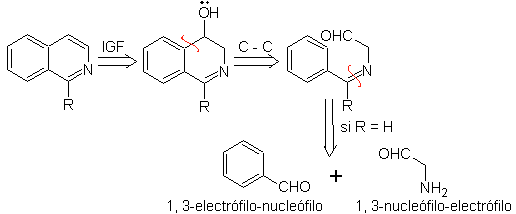
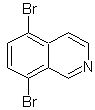
Usulkan desain sintesis untuk masing-masing isoquinolines berikut: | MOb 107
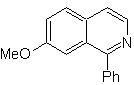
| MOb 108
|
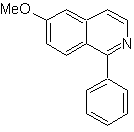
MOb 107 . Analisis retrosintetik . Pemutusan dari
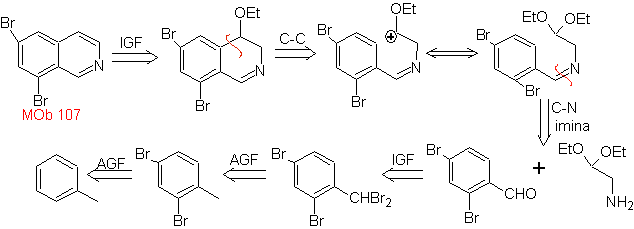
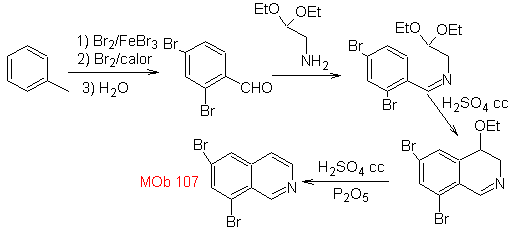
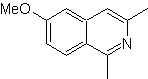
MOb 108. Analisis retrosintetik . Kehadiran substituen pada C1 isoquinoline, mengarah pada pemutusan hubungan
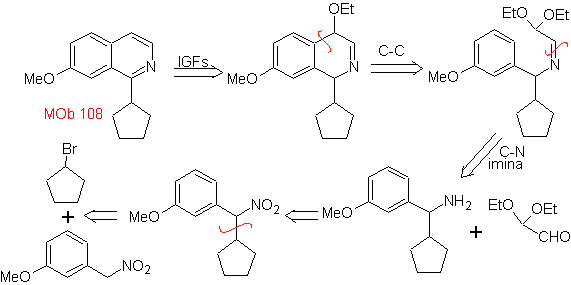
Sintesis Turunan benzyalmine disiapkan untuk bereaksi dengan aminoaldehyde diacetal, menurut sintesis Pomeranz-Fritsch, untuk membentuk
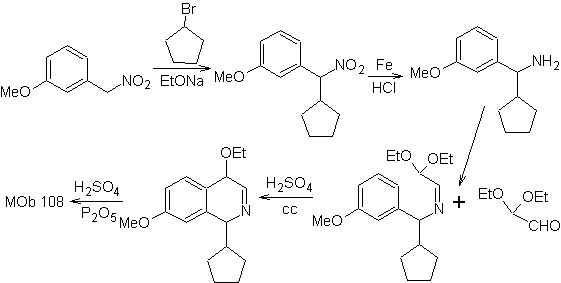
2. Sintesis BISCHLER-NAPIERALSKI .
Metode sintetik isoquinolines ini melibatkan reaksi Phenethylamine (1,5-dinucleophile) dengan asam klorida atau anhidrida (elektrofil) untuk membentuk amida, yang siklisasinya dengan hilangnya air menghasilkan 2,4-dihydroisoquinoline dengan substituen di C-1, yang dioksidasi menjadi isoquinoline dengan Pd-C atau fenil disulfida.
Langkah siklisasi adalah substitusi aromatik elektrofilik dan oleh karena itu akan disukai oleh substituen penyumbang elektron pada cincin aromatik fenetilamina. Fenetilamina tersubstitusi m mengarah secara eksklusif ke isokinolin tersubstitusi C-6, karena siklisasi pada posisi para sehubungan dengan gugus pengaktif.
Analisis retrosintetik dari isoquinolines yang disiapkan dengan metode ini adalah sebagai berikut:
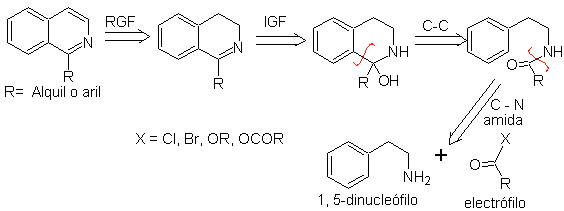
Agen siklisasi yang paling sering digunakan dalam sintesis ini adalah:
ke.
P 2 O 5 (fosfor pentoksida)
B.
POCl 3 (fosfor oksiklorida) dan
C.
SOCl 2 (tionil klorida)
Usulkan rencana sintesis untuk isoquinolines berikut: | MOb 109
| MOb 110
|
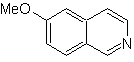
MOb 109 . Analisis retrosintetik .
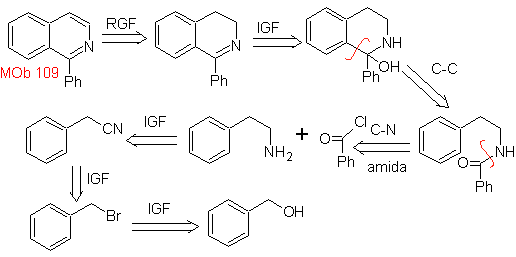
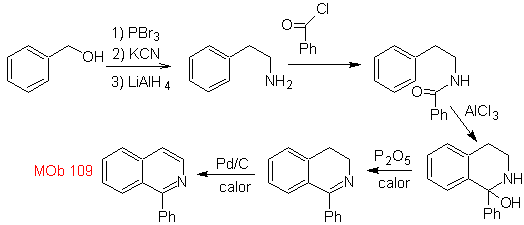
Perpaduan. Benzil alkohol adalah bahan awal yang baik untuk membentuk fenetilamina, yang digabungkan dengan benzoil klorida. Produk disikluskan dan dibumbui dengan Pd/C dan panas untuk dibentuk
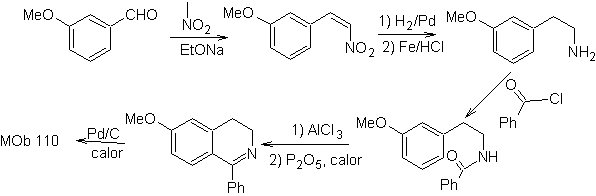
MOb 110. Analisis retrosintetik.
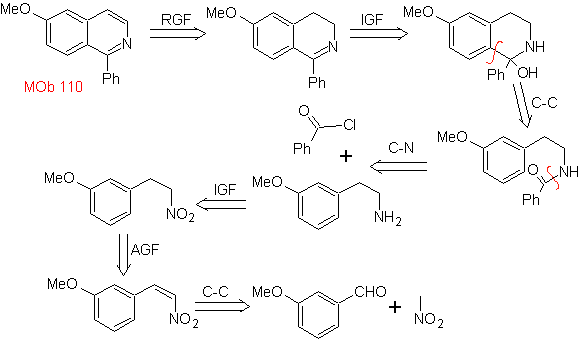
Perpaduan. Sintesis dari
3.
sintesis PICTET-GAMS.
Ini adalah varian dari sintesis Bischler-Napieralski, dalam metode ini digunakan fenetilamina yang berpotensi tidak jenuh, memperoleh heterosiklik aromatik total, oleh karena itu penerapan oksidan tidak diperlukan.
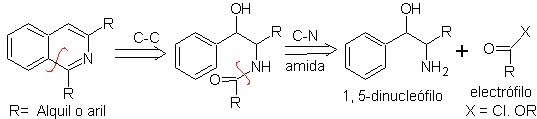
Analisis retrosintetik dari metode ini menunjukkan rekoneksi potensial berikut dan bahan awal.
Usulkan desain sintesis untuk isoquinoline berikut : | MOb 111.
|
MOb 111 . Analisis retrosintetik . Untuk memulai pemutusan
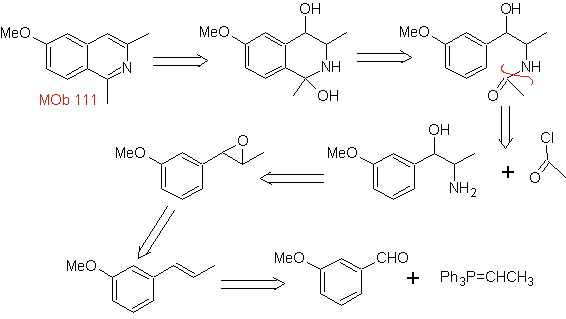
sintesis . Sintesis Pictet-Gams diterapkan, sehingga tidak perlu menggunakan oksidan pada akhirnya, untuk mencapai pembentukan
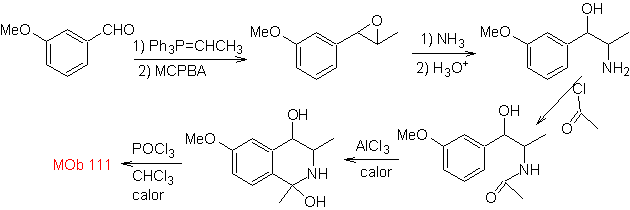
Fenetilamina juga dapat bereaksi dengan aldehida dengan hasil yang baik, menghasilkan aldimina yang dapat tersiklis dalam media asam menjadi 1,2,3,4-tetrahidroisoquinolin, yang harus dioksidasi untuk menghasilkan isoquinolin.
Siklisasi ini membutuhkan substituen pengaktif yang ditempatkan dengan tepat untuk mengaktifkan posisi orto ke gugus aminoetil, oleh karena itu penutupan cincin selalu terjadi pada posisi para ke aktivator.
Ketika cincin aromatik diaktifkan dengan substituen hidroksil, penutupan cincin terjadi dalam kondisi yang sangat ringan, karena efek pengaktifan yang kuat dari OH-
Analisis retrosintetik dari isoquinoline yang dibentuk dengan metode Pictet-Spengler , menunjukkan pemutusan dan bahan awal berikut:
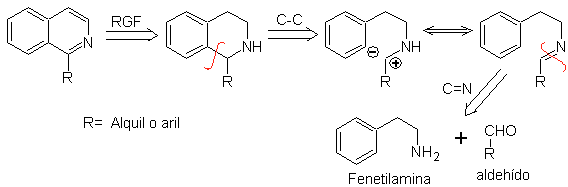
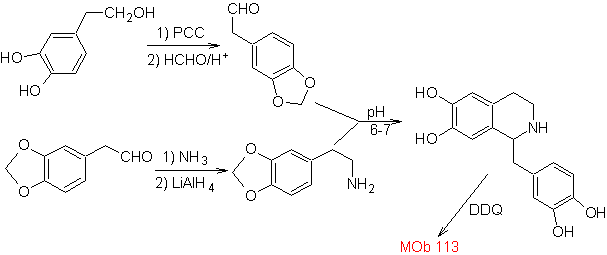
Usulkan rencana sintesis untuk Isoquinolines berikut: | MOb 112
| ….. | MOb 113
|
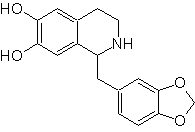
MOb 112. Analisis retrosintetik .
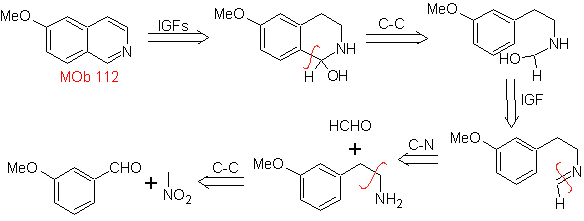
sintesis . Siklisasi terjadi dalam media asam dan DDG digunakan untuk membumbui hidroisokinolin yang dibentuk untuk menyiapkan
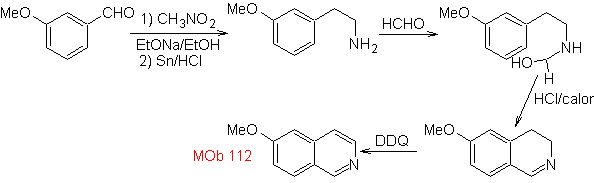
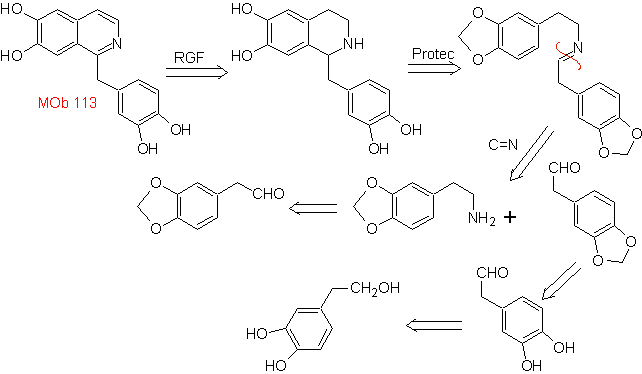
Perpaduan Sintesis Pictet-Spengler diterapkan pada bentuk
Amé Pictet (1857-1937) adalah salah satu dari enam anggota perwakilan Swiss dan bertindak sebagai sekretaris Kongres Kimia Jenewa . Sebagai perwakilan dari