Harte Nucleophile (organometallisch, Amid, Lithiumaluminiumhydrid) greifen die Position 2 des Pyridinrings an und führen zu nucleophilen Additionsreaktionen. Tritt eine letzte Oxidationsstufe mit Hydridverlust ein, spricht man von nukleophiler Substitution.
a) Zugabe von Organometallen
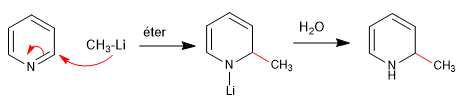
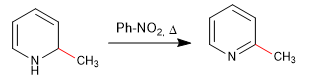
Die Rearomatisierung des Rings ist möglich durch Zugabe eines Oxidationsmittels, das "H 2 " entfernt.
b) Addition von Amid. Chichibabins Reaktion
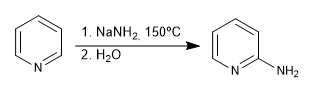
Mechanismus:
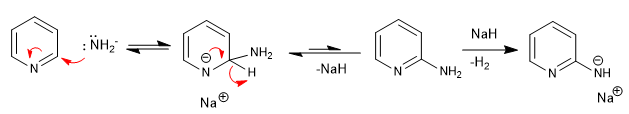
Das gebildete Natriumamid wird in der letzten Stufe der wässrigen Aufarbeitung protoniert.
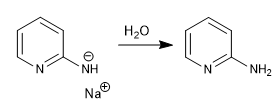
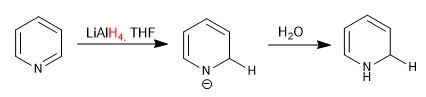
c) Addition von Hydriden
Lithiumaluminiumhydrid addiert Hydride an die 2-Position von Pyridin.
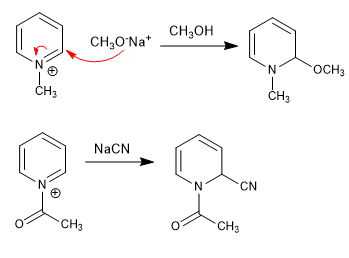
Die schwächeren Nucleophile (Cyanid, Hydroxid, Methoxid) greifen die 2-Position des Pyridins nicht an, reagieren aber dank der größeren Polarität der 2-Position mit Pyridiniumsalzen.