HETEROCYCLEN - AROMATIK
- Details
- Germán Fernández
- HETEROCYCLEN - AROMATIK
- Zugriffe: 1550
- Details
- Germán Fernández
- HETEROCYCLEN - AROMATIK
- Zugriffe: 2173
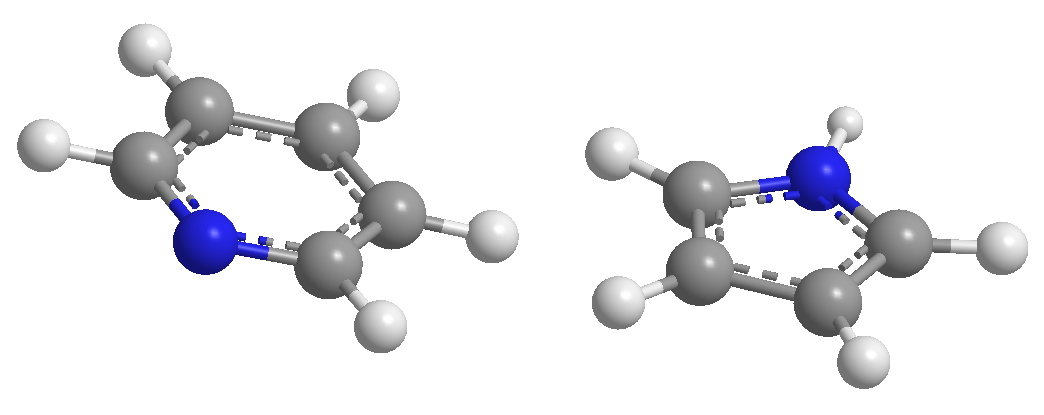
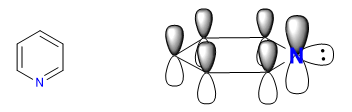
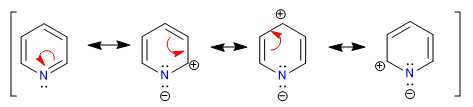
A) Heterocyclen mit 6 Atomen und 6 p -Elektronen.
- Details
- Germán Fernández
- HETEROCYCLEN - AROMATIK
- Zugriffe: 1962
Es gibt mehrere Kriterien, um den Aromatizitätsgrad eines Heterocyclus zu bestimmen:
A) Verbindungslängen.
Ein Heterocyclus ist umso aromatischer, je geringer der Unterschied zwischen den Längen der verschiedenen Bindungen ist, aus denen der Ring besteht. Benzol hat in allen seinen Kohlenstoff-Kohlenstoff-Bindungen die gleiche Länge, was es zur aromatischsten Verbindung macht. Die Heterocyclen weisen Unterschiede in den Bindungsabständen auf, wobei sie umso weniger aromatisch sind, je größer diese Unterschiede sind.
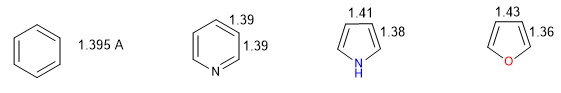
Alle CC-Bindungen in Benzol messen 1,395 Å, ein mittlerer Bindungsabstand zwischen Einfach- (1,48 Å) und Doppelbindungen (1,34 Å). In Furan gibt es einen bemerkenswerten Unterschied in der Länge der Bindungen, was auf eine geringere Aromatizität als in Pyrrol hinweist. Pyridin hingegen hat sehr ähnliche CC-Bindungsabstände zwischen ihnen und ähnlich denen von Benzol, das eine größere Aromatizität als Pyrrol oder Furan zeigt.
Weiterlesen: Kriterien zur Bestimmung der Aromatizität in Heterocyclen
- Details
- Germán Fernández
- HETEROCYCLEN - AROMATIK
- Zugriffe: 1733
6-gliedrige Heteroaromaten mit -OH- oder -SH-Gruppen in 2,4-Stellung liegen vorzugsweise in Lösung in der Keto- oder Thioketo-Form vor. In Lösung liegen Verbindungen mit Aminogruppen in 2,4-Positionen vorzugsweise in der Aminoform statt als Imino-Tautomer vor.
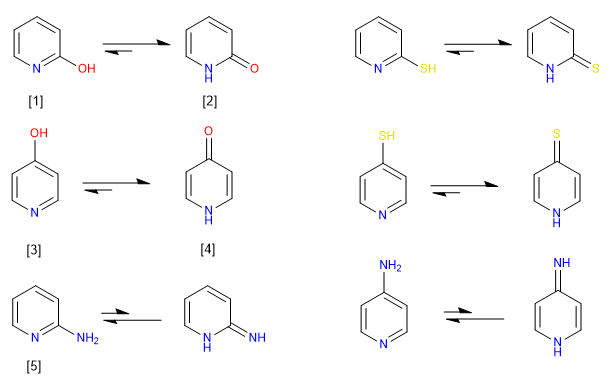
[1] 2-Hydroxypyridin
[2] 2-Pyridon
[3] 4-Hydroxypyridin
[4] 4-Pyridon
[5] 2-Aminopyridin
- Details
- Germán Fernández
- HETEROCYCLEN - AROMATIK
- Zugriffe: 1891
In diesem Abschnitt untersuchen wir den Einfluss ringförmiger Spannungen auf die Eigenschaften von Heterocyclen.
A) Winkelspannung in kleinen Heterocyclen (3 und 4 Mitglieder).
Die natürlichen Bindungswinkel eines sp 3 -Kohlenstoffs betragen 109,5°, jedoch verringert sich dieser Winkel in dreigliedrigen Zyklen auf 60°, was eine enorme Spannung erzeugt. Um diese Spannung zu verringern, sind die Bindungen zwischen Kohlenstoffen nicht mehr gerade, sondern biegen sich, wodurch gekrümmte Bindungen entstehen, die als "Bananenbindungen" bezeichnet werden. Die durch diese Bindungen gebildeten Winkel betragen 104°, eine erträglichere Abweichung.
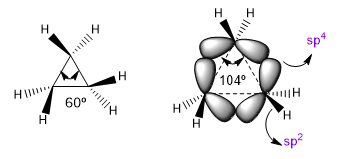
| Hybridisierung | Bindungswinkel |
| sp sp2 sp 3 sp 4 | 180º 120º 109,5º 104. |
- Details
- Germán Fernández
- HETEROCYCLEN - AROMATIK
- Zugriffe: 2690
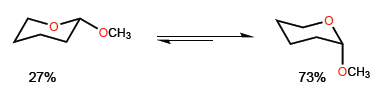
Das Phänomen, durch das die axiale Konformation eines substituierten Heterocyclus in Position 2 stabilisiert wird, wird als anomerer Effekt bezeichnet.Zum Beispiel weist 2-Methoxyoxan ein Verhältnis von 27:73 zugunsten der Konformationmit Methoxid in axialer Position auf.