WAS IST ASYMMETRISCHE SYNTHESE?
Die asymmetrische Synthese oder auch chirale oder enantioselektive Synthese genannt, ist diejenige, die eine gewünschte Chiralität einführt oder begünstigt. Dieser Zweig der organischen Synthese ist für die Herstellung von Arzneimitteln von entscheidender Bedeutung, da diese im Körper durch verschiedene Stoffwechselmechanismen nur auf eine bestimmte Chiralität der dabei vorhandenen Enzyme wirken.
GRUNDLEGENDE KONZEPTE DER ASYMMETRISCHEN SYNTHESE:
REGIOSELEKTIVES VERFAHREN:
Eine Reaktion wird als regioselektiv bezeichnet, wenn eines der möglichen Strukturisomere überwiegend auftritt:
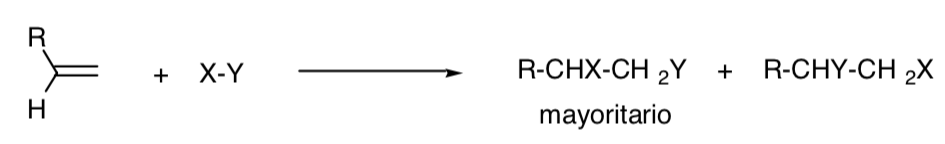
REGIOSPEZIFISCHER PROZESS:
Eine Reaktion wird als regiospezifisch bezeichnet, wenn nur eines der möglichen Strukturisomere gebildet wird:
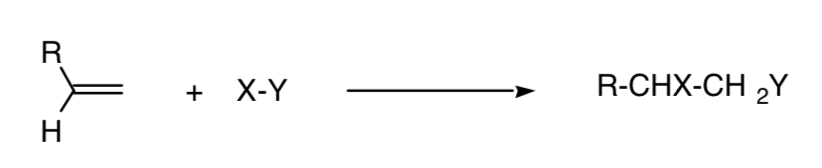
Dieses Konzept kann auf andere Prozesse wie 4 + 2-Cycloadditionsprozesse erweitert werden:
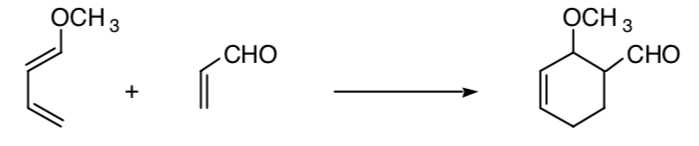
STEREOSELECTIVE SYNTHESE:
Eine Synthese wird als stereoselektiv bezeichnet, wenn ein Stereoisomer einer bestimmten Struktur in einem erheblich höheren Anteil entsteht als die übrigen anderen Stereoisomere derselben Struktur.
Von einem enantioselektiven Verfahren spricht man, wenn eines der Enantiomere überwiegt, und von einem diastereoselektiven Verfahren, wenn ein Diastereomer oder diastereomeres Racemat mehrheitlich gebildet wird.
STEREOSPEZIFISCHE SYNTHESE:
Es ist eines, bei dem verschiedene Stereoisomere des Ausgangssubstrats zu stereoisomer unterschiedlichen Produkten führen:
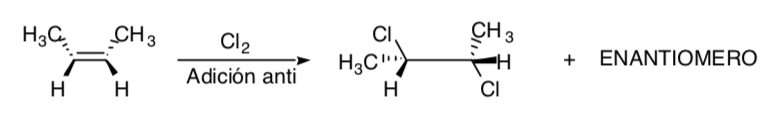
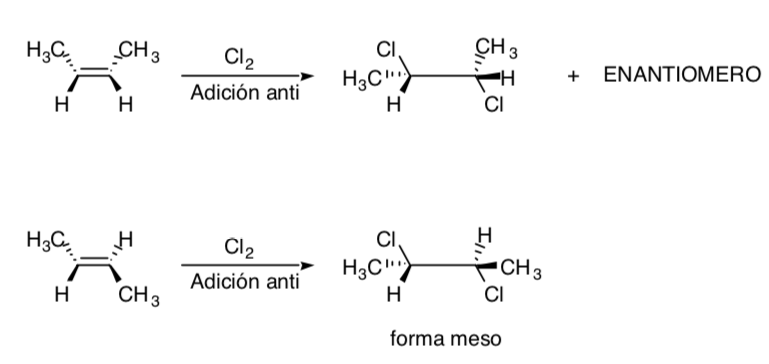
Die Chlorierung von Alkenen ist ein Beispiel für einen stereospezifischen Prozess:
STEREOSELEKTIVE STEUERUNG EINER SYNTHESE:
Die Notwendigkeit einer stereoselektiven Kontrolle bei der Schaffung neuer Chiralitätszentren zeigt sich in der sukzessiven Reduktion einer der Carbonylgruppen und der im Wieland-Miescher-Keton vorhandenen Doppelbindung. Wenn das Verfahren nicht stereoselektiv ist, werden vier Stereoisomere des Endprodukts erhalten:
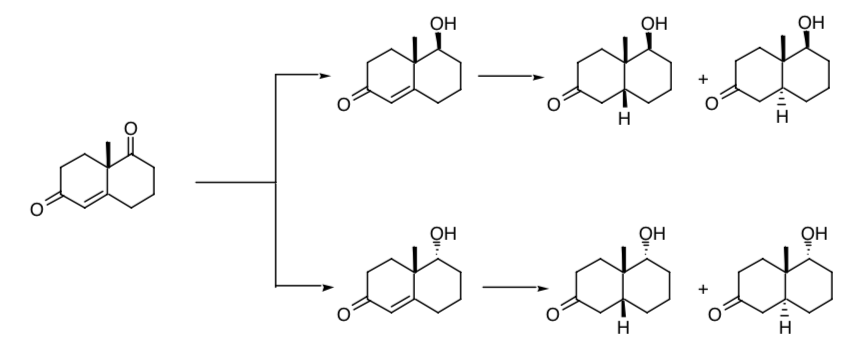
Wenn wir vom Racemat des Ketons ausgehen, erhalten wir aus dem Reduktionsverfahren acht mögliche Stereoisomere.
STEREOCHEMISCHE ÜBERLEGUNGEN:
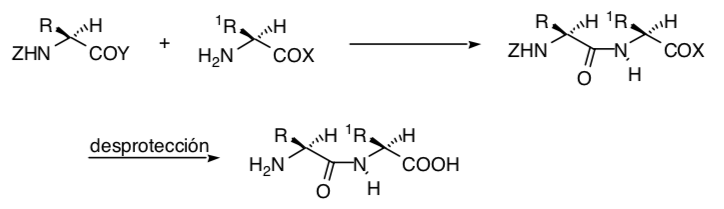
Eine Vereinfachung des stereochemischen Problems kann darin bestehen, alle Chiralitätszentren zu eliminieren und eine möglichst stereoselektive Synthese zu planen, bei der nicht nur die Konfiguration jedes Chiralitätszentrums berücksichtigt werden muss, sondern auch der Einfluss einiger Chiralitätszentren auf Andere. Wenn dieser Einfluss nicht vorhanden ist (weil sie entfernt sind), kann das Problem vereinfacht werden, indem von Struktureinheiten ausgegangen wird, die die Chiralitätszentren mit der entsprechenden Konfiguration umfassen.
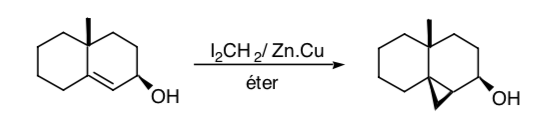
Manchmal ist es möglich, entfernte funktionelle Gruppen als Kontrollsynthons zu verwenden, wie im Fall der Simmons-Smith-Cyclopropanierung, bei der eine Hydroxylgruppe die stereoselektive Durchführung der Cyclopropanierung durch Koordination der Hydroxygruppe mit der Carbenoidspezies ermöglicht:
ÜBERLEGUNGEN ZUR SYMMETRIE:
Das Erkennen einer Symmetrie im Molekül kann sehr nützlich sein, wie im Fall von Squalen:
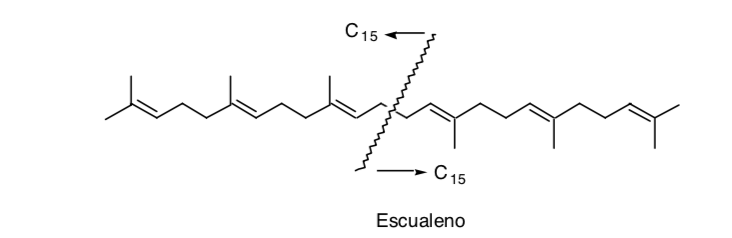
Obwohl seine Synthese in Wirklichkeit nicht durch Dimerisierung (C15 + C15), sondern durch Hinzufügen von zwei C11-Einheiten zu einer zentralen C8-Einheit (C11 + C8 + C11) durchgeführt wurde.
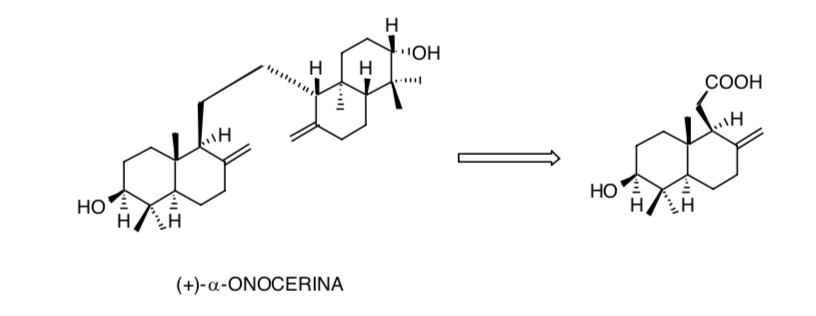
Die Berücksichtigung der Symmetrie im (+)-α-Onocerin-Molekül reduziert das Problem der Schaffung von acht Chiralitätszentren auf nur vier:
Empfohlene Quellen für weitere Informationen:
1) Guo-Qiang Lin, Yue-Ming Li, Albert SC Chan. Prinzipien und Anwendungen der asymmetrischen Synthese. Hrsg. Wiley-Interscience. Großbritannien, 2001.
2) Mark Rizzacasa und Michael Perkins. Stöchiometrische asymmetrische Synthese. Hrsg. Sheffield Academic Press. USA und Kanada. 2000.
3) Jonathan MJ Williams. Katalyse in der asymmetrischen Synthese. Hrsg. Sheffield Academic Press. USA und Kanada. 1999.
4) RA Aitken und SN Kulényi. Asymmetrische Synthese. Hrsg. Blackie Academic and Professional. Großbritannien, 1992.
5) Grossman RB Die Kunst, vernünftige organische Reaktionsmechanismen zu schreiben. Springer, NewYork. 2003
6) Normannisches ROC; Coxon JM Prinzipien der organischen Synthese. CRC Press, Boca Raton. 1993