In diesem Abschnitt sehen wir Beispiele für die Synthese von Heterocyclen durch nucleophilen Angriff auf Carbonylgruppen. Aldehyd- und Ketoncarbonyle führen zu nucleophilen Additionsreaktionen, während Carbonyle von Säurederivaten (Halogenide, Anhydride, Ester, Amide, Nitrile) zu Additions-Eliminierungs-Prozessen führen.
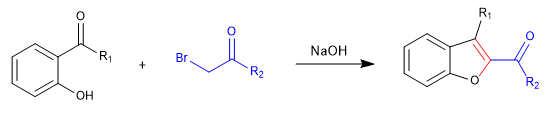
A) Wir beginnen mit der Synthese eines Benzofurans.
In der ersten Stufe verbinden wir die Reaktanten über ein S N 2 und führen schließlich zu einer Aldolreaktion.
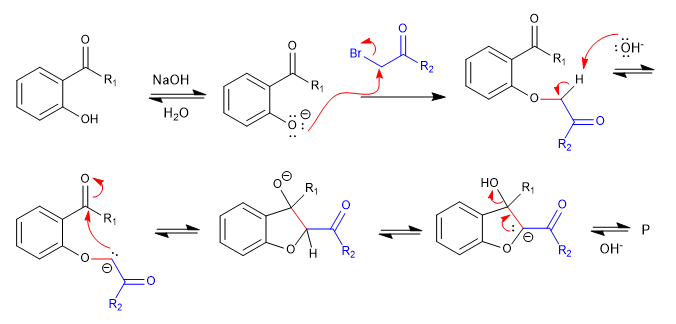
Mechanismus:
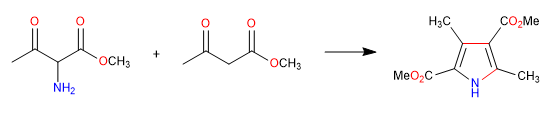
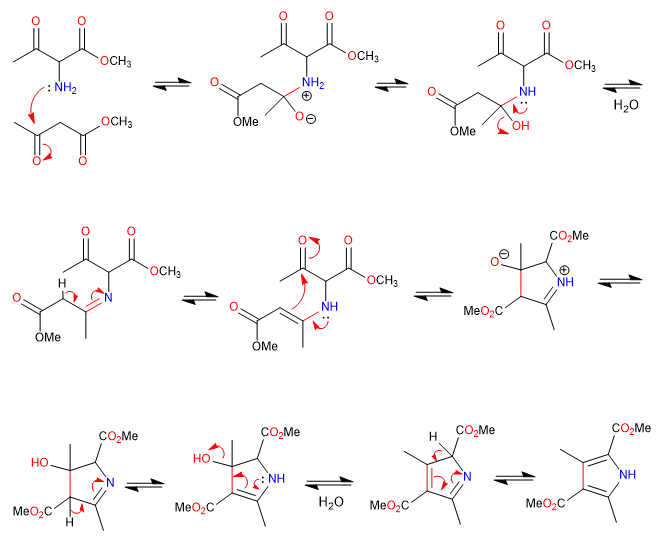
B) Wir fahren mit der Synthese eines Pyrrols durch Iminbildung und Cyclisierung mit Enaminangriff auf Carbonyl fort.
Mechanismus:
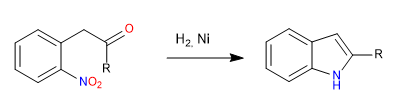
C) Erhalt von Indol durch Angriff auf nucleophile Heteroatome an Carbonyl.
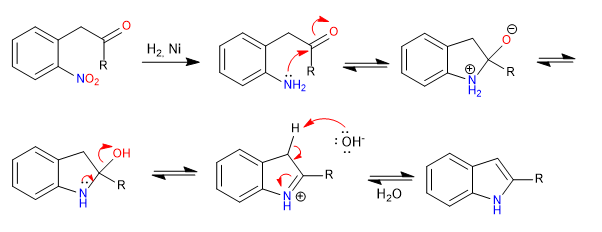
Mechanismus:
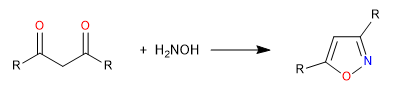
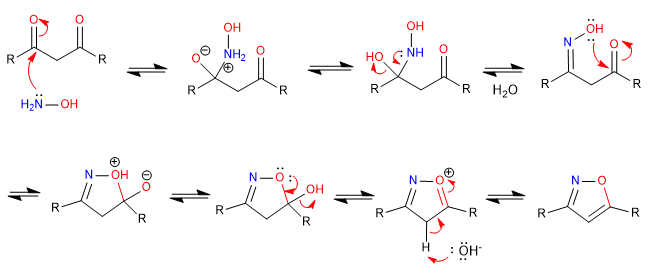
D) Wir fahren mit einem weiteren Beispiel der Cyclisierung durch Angriff von Heteroatomen auf Carbonyle fort. In diesem Fall wirkt Hydroxylamin als Nukleophil, um ein Isoxazol zu bilden.
Mechanismus:
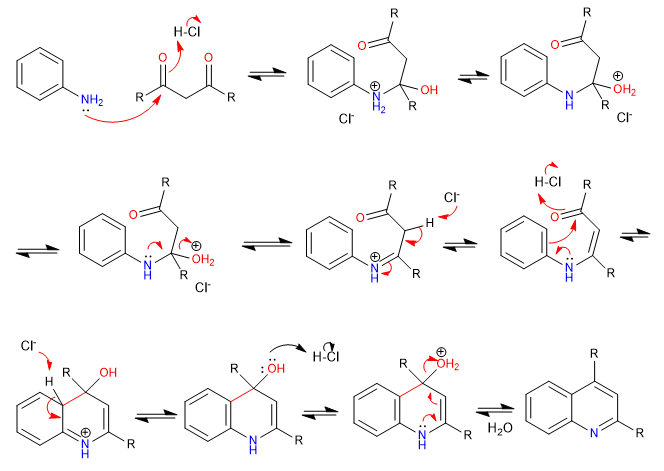
E) Cyclisierung an einer ortho-Position eines Benzolrings, um Chinolin zu ergeben.
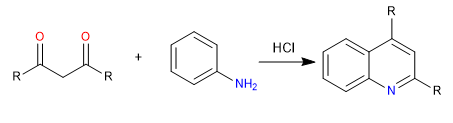
Mechanismus: